Clear Sky Science · nl
HCMV-infectie verstoort barrièrefuncties en bevordert epitheliale–mesenchymale transformatie in een cholangiocyt-organoïde model
Waarom dit verhaal over een virus in de lever ertoe doet
Het humaan cytomegalovirus is een zeer veelvoorkomend virus dat de meesten van ons bij zich dragen zonder het te weten. Bij pasgeborenen en mensen met een kwetsbaar immuunsysteem kan het echter samenhangen met ernstige lever- en galgangproblemen, waaronder een zeldzame maar verwoestende kinderziekte genaamd biliaire atresie. Deze studie gebruikt miniatuur, in het lab gekweekte menselijke galgangen om te laten zien hoe het virus deze delicate buisjes direct kan beschadigen en littekenvorming kan veroorzaken, wat kan helpen de al lang bediscussieerde verbanden tussen infectie en levenslange leverziekte te verklaren.
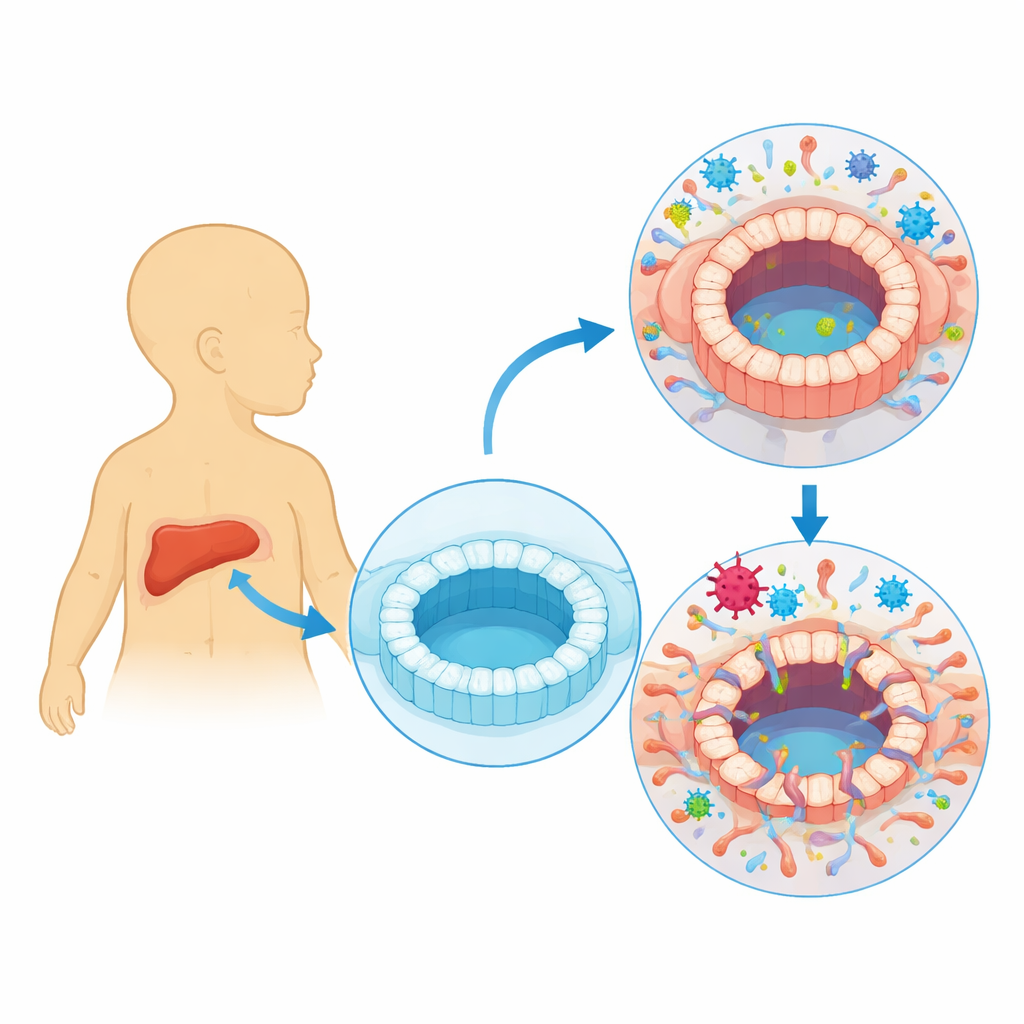
Een nadere blik op een veelvoorkomend maar stil virus
Humaan cytomegalovirus (HCMV) leeft meestal stil in ons lichaam en wisselt tussen een actieve fase, waarin het nieuwe virusdeeltjes produceert, en een stille fase, waarin het zich verbergt in bepaalde bloedcellen. Artsen merken al lang dat mensen met duidelijke HCMV-infectie galgangletsel en cholestase kunnen ontwikkelen, waarbij gal niet goed kan stromen. Veel zuigelingen met biliaire atresie, een aandoening waarbij galgangen kort na de geboorte geblokkeerd en verkleefd raken, vertonen ook tekenen van recente HCMV-infectie. Het was echter onduidelijk of het virus daadwerkelijk de cellen die de galgangen bekleden infecteert of slechts als voorbijganger aanwezig is tijdens ziekte.
Mini-galgangen bouwen in een petrischaal
Om dit te onderzoeken creëerden de onderzoekers driedimensionale “organoïden” die menselijke galgangen nabootsen. Ze begonnen met geïnduceerde pluripotente stamcellen, gereprogrammeerd uit menselijk bloed, en leidden deze naar cholangiocytachtige cellen—het type cellen dat de galgangen bekleedt. Deze cellen organiseerden zich spontaan tot holle bolletjes met een centrale holte en nauwe cel–celverbindingen, die lijken op een verkleinde galgang. Het team bracht vervolgens deze organoïden in contact met een HCMV-stam die was gemarkeerd met een fluorescent label dat oplicht wanneer het virus actief repliceert. Daardoor konden ze geïnfecteerde cellen volgen en meten hoe de organoïden in de loop van de tijd veranderden.
Hoe infectie structuur vervormt en de barrière verzwakt
Eenmaal geïnfecteerd stopten de organoïden met normaal groeien en werden ze vervormd, met verdikte en onregelmatige wanden. Sommige cellen gloeiden fel en toonden volledige virale activiteit en productie van nieuwe virusdeeltjes; andere droegen viraal genetisch materiaal op lagere niveaus, wat wijst op een meer sluimerende, latentie-achtige staat. Functionele tests lieten zien dat geïnfecteerde organoïden belangrijke galgangfuncties verloren. Ze zwollen niet meer normaal als reactie op een prikkel die afhankelijk is van ionentransportkanalen, en ze lekteerden makkelijker in een elektrische weerstandstest die de striktheid van de barrière meet. Eiwitten die normaal de ruimten tussen cellen afdichten, zoals componenten van tight junctions, namen af, en het transport van een testkleurstof in en uit de binnenholte werd abnormaal. Samen tonen deze veranderingen aan dat HCMV de galgangwand direct kan aantasten en deze lek en disfunctioneel kan maken.
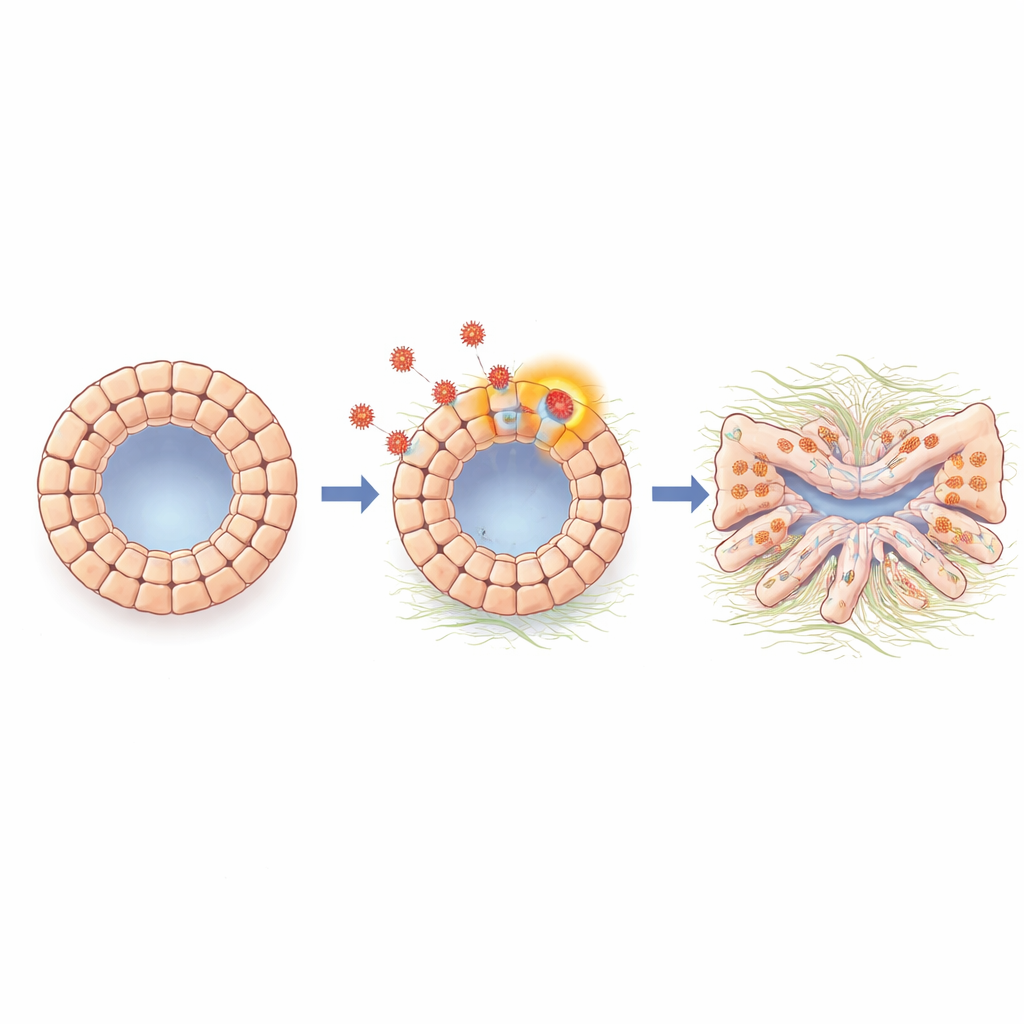
Cellen veranderen richting een littekenachtige identiteit
Verder graven analyseerden de wetenschappers genactiviteit in de organoïden zowel in bulk als op enkelcelleniveau. Ze vonden een sterke activatie van een epitheliale–mesenchymale transformatie-achtig programma, een proces waarbij nauw verbonden oppervlaktecellen hun bindingen losser maken, een mobielere, vezelachtige aard aannemen en beginenn met het produceren van moleculen die geassocieerd zijn met weefsellittekenvorming. Geïnfecteerde organoïden vertoonden verhoogde niveaus van N-cadherine en andere markers gekoppeld aan deze verschuiving, evenals genen die betrokken zijn bij fibrose en matrixproductie. Een signaalmolecuul genaamd TGF-beta, bekend om het aansturen van littekenvorming in veel organen, werd tijdens de infectie versterkt. Toen het team TGF-beta-signaleringsroutes blokkeerde met een kleinmolecuulremmer of een antilichaam, herkregen de organoïden een meer normale vorm en daalden veel van de genen gerelateerd aan littekenvorming en transitie naar nagenoeg basisniveau, wat aangeeft dat TGF-beta een belangrijke schakel is die de aanwezigheid van het virus verbindt met schadelijke celdelingen.
Van in het lab gekweekte buisjes terug naar zieke kinderen
Om te zien of deze labwaarnemingen verband houden met echte ziekte, onderzochten de onderzoekers leverweefsel van kinderen met biliaire atresie en van andere pediatrische leveraandoeningen. Met gevoelige probes detecteerden ze HCMV-DNA in cholangiocyten—de galgangcellen—in ongeveer tweederde van de biliaire atresie-monsters, maar veel minder vaak in niet-biliaire atresie-levermonsters. In dezelfde regio’s waar viraal DNA werd gevonden, vertoonden de galgangcellen hogere niveaus van TGF-beta en N-cadherine, wat overeenkomt met het transitie- en littekenpatroon dat in de organoïden werd gezien. Dit suggereert dat HCMV in ten minste een subset van kinderen galgangcellen direct infecteert en ze via activering van TGF-beta-gedreven routes naar een fibrotische staat duwt.
Wat dit betekent voor begrip en behandeling van galgangaandoeningen
In eenvoudige termen toont dit werk aan dat een veelvoorkomend virus de cellen die de galgangen bekleden kan binnendringen, hun nauwe verbindingen kan verzwakken en ze via een TGF-beta–gebaseerd signaal naar een littekenachtige, minder gespecialiseerde identiteit kan duwen. Deze veranderingen verzwakken de barrières en transportfuncties van de galgangen en kunnen bijdragen aan de geblokkeerde, fibrotische galgangen die worden gezien bij aandoeningen zoals biliaire atresie. Hoewel niet elk geval van galgangaandoening door HCMV wordt veroorzaakt, versterkt de studie het bewijs dat virale infectie bij kwetsbare zuigelingen een belangrijke factor kan zijn—en dat het richten op TGF-beta-gerelateerde routes mogelijk op termijn kan helpen kwetsbare galgangen te beschermen of te herstellen.
Bronvermelding: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Trefwoorden: cytomegalovirus, biliaire atresie, galgang-organoïden, epitheliale mesenchymale transformatie, TGF-beta signalering