Clear Sky Science · nl
Begrijpen van bevordering door alkalimetalen in waterstofatiecatalyse via Strong Metal–Base Interaction
Waarom het fijnafstellen van katalysatoren belangrijk is voor het dagelijks leven
Het omzetten van eenvoudige moleculen zoals kooldioxide en waterstof in bruikbare brandstoffen en chemicaliën is cruciaal voor schonere energie en een duurzamere industrie. Veel van de metaalkatalysatoren die deze reacties aansturen bevatten al kleine hoeveelheden alkalimetalen zoals natrium of kalium als “bevorderaars”, maar hun echte rol is verrassend onduidelijk gebleven. Deze studie onthult een verenigend principe voor hoe deze toevoegingen daadwerkelijk werken, en biedt een manier om slimmere katalysatoren te ontwerpen die reacties naar gewenste producten kunnen sturen en afval verminderen.
Een nadere blik op versterkte metaalkatalysatoren
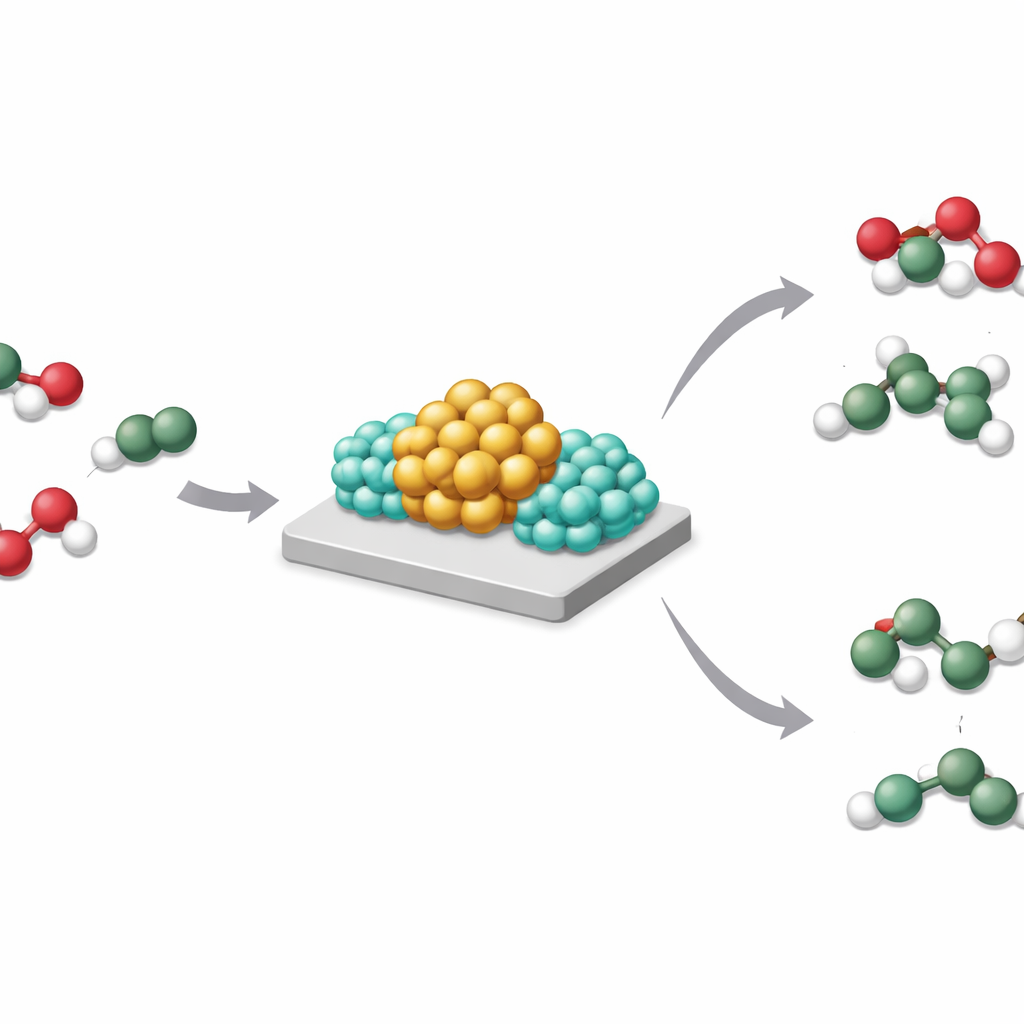
Katalysatoren op basis van overgangsmetalen zoals rhodium en nikkel staan op vaste dragers en helpen bij het breken en vormen van chemische bindingen. Al tientallen jaren voegt de industrie alkalimetalen toe om deze katalysatoren actiever, selectiever of duurzamer te maken. De gebruikelijke verklaringen richtten zich op eenvoudige geometrische effecten (verandering van de deeltjesvormen en -groottes) of directe elektrondonatie van het alkalimetaal aan het actieve metaal. In reële bedrijfsomstandigheden komen deze bevorderaars echter hoofdzakelijk voor als oxiden, niet als kale metaalatomen, waardoor eenvoudige elektronenoverdracht een onvolledig beeld geeft.
Een sterke samenwerking aan het oppervlak ontdekken
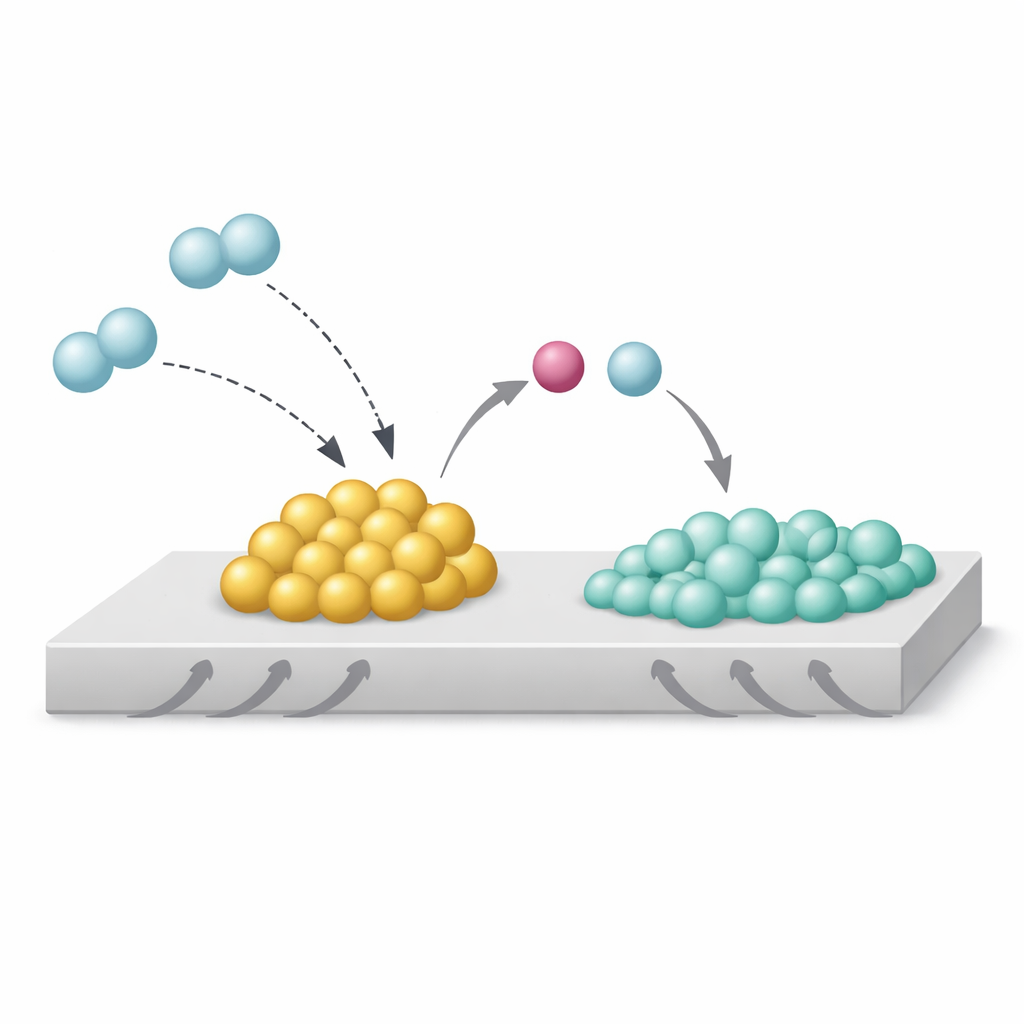
De auteurs bestudeerden een modelsysteem: rhodiumnanodeeltjes op titaandioxide, met en zonder toegevoegde natrium. Met geavanceerde elektronenmicroscopie, röntgenspectroscopie en computersimulaties vonden ze dat natrium als oxide, Na₂O, precies zit waar de rhodiumdeeltjes de drager raken. Onder waterstof creëert deze opstelling wat zij een Strong Metal–Base Interaction (SMBI) noemen. Bij deze speciale contactpunten splitst binnenkomende waterstof ongelijk: het basischere Na₂O grijpt het protonachtige deel, terwijl het rhodium het elektronenrijke partnerdeeltje vasthoudt. Deze heterolytische splitsing laat het rhodiumoppervlak ongewoon elektronrijk achter en voorkomt dat waterstof zich over de titaandioxide‑drager verspreidt, oftewel dat er ‘spillover’ optreedt.
Hoe dit verborgen effect reacties stuurt
Deze subtiele herschikking van waar waterstof en elektronen zich bevinden heeft grote gevolgen. Bij de waterstofatie van kooldioxide leidt gewoon rhodium op titaandioxide tot sterke waterstofatie tot en met methaan. Wanneer natrium wordt toegevoegd, produceert dezelfde katalysator voornamelijk koolmonoxide, een waardevolle bouwsteen, en veel minder methaan. Gelijkaardig gedrag treedt op wanneer lithium of kalium worden gebruikt, of wanneer rhodium wordt vervangen door nikkel. De auteurs tonen aan dat wanneer waterstof vrij over de drager kan overlopen, diepe waterstofatie domineert; wanneer SMBI waterstof geconcentreerd houdt bij de metaal‑base grens en van de drager weg, ontstaan mildere producten.
Verschillende dubbels¬bindingen, verschillende uitkomsten
Het team onderzocht vervolgens hoe SMBI gebruikelijke organische waterstofaties beïnvloedt die koolstof‑koolstof, koolstof‑zuurstof en stikstof‑zuurstof dubbele bindingen betreffen. Voor een koolstof‑koolstof dubbele binding in vinylacetaat maakt natriumpromotie de katalysator sneller, waarschijnlijk omdat elektronrijke rhodium die binding verzwakt terwijl zwakker gebonden waterstof er efficiënt aan additieeert. Daartegenover vertraagt dezelfde natriumtoevoeging reacties voor moleculen zoals acetofenon en nitrobenzeen, waarvan de reactieve groepen de voorkeur geven aan plaatsing op de oxide‑drager. Hier betekent de geremde waterstof‑spillover dat de drager niet genoeg waterstof ontvangt om die transformaties te drijven, wat laat zien dat niet alle dubbele bindingen evenveel voordeel halen uit dezelfde promotionele werking.
Katalysatoren ontwerpen met intentionele controle
Door experimenten en theorie te combineren betogen de auteurs dat SMBI een eenduidige manier biedt om te begrijpen hoe alkalimetalbevorderaars katalytische oppervlakken herschikken. In plaats van te fungeren als eenvoudige elektrondonoren, werken alkalioxidezouten als sterke protonvangers, dwingen ze waterstof tot een gepolariseerde splitsing en beperken ze reactieve waterstof nabij de metaal‑base interface. Dit inzicht verklaart raadselachtige trends over vele waterstofatiereacties en metalen heen, en wijst op een praktisch ontwerprichtlijn: door te regelen hoeveel en waar alkalioxide rond metaaldeeltjes wordt geplaatst, kunnen scheikundigen reacties doelbewust sturen naar specifieke producten terwijl ze activiteit en stabiliteit optimaliseren voor schonere chemische processen.
Bronvermelding: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Trefwoorden: waterstofatiecatalyse, bevorderaars van alkalimetalen, CO2‑conversie, heterogene katalysatoren, metaal‑oxide interfaces