Clear Sky Science · nl
Een allosterische remmer van het Zika-virus NS2B-NS3-protease met orale werkzaamheid in muismodellen
Een nieuwe manier om een gevaarlijk virus te slim af te zijn
Het Zika-virus stond tien jaar geleden wereldwijd in het nieuws toen infecties bij zwangere vrouwen werden gekoppeld aan baby’s met abnormaal kleine schedels en hersenschade. Toch is er nog steeds geen goedgekeurd geneesmiddel om Zika te behandelen of te voorkomen. Deze studie beschrijft een veelbelovend nieuw, pilachtig verbinding die een sleutelvirusenzym op een onverwachte manier uitschakelt en muizen beschermt tegen ernstige Zika-infectie, en wijst daarmee op een toekomstig middel dat kwetsbare mensen zou kunnen beschermen, vooral tijdens uitbraken.
Waarom Zika nog steeds van belang is
Het Zika-virus wordt voornamelijk overgedragen door Aedes-muggen en behoort tot dezelfde familie als dengue- en Westnijlvirussen. De meeste besmette mensen voelen weinig tot geen ziekteverschijnselen, maar ongeveer één op de vijf ontwikkelt klachten variërend van koorts en huiduitslag tot ernstige complicaties zoals oogschade, orgaanfalen en aandoeningen van het zenuwstelsel. Het grootste gevaar geldt voor foetussen: infectie tijdens de zwangerschap kan leiden tot microcefalie en levenslange beperkingen. Omdat er geen goedgekeurd vaccin of antivirale behandeling is, kunnen artsen alleen ondersteunende zorg bieden. Wetenschappers zien Zika daarom als een prioriteit voor pandemische paraatheid en zoeken naar geneesmiddelen die zowel kwetsbare groepen kunnen beschermen als nieuwe uitbraken kunnen indammen.
Op zoek naar verborgen zwakke plekken
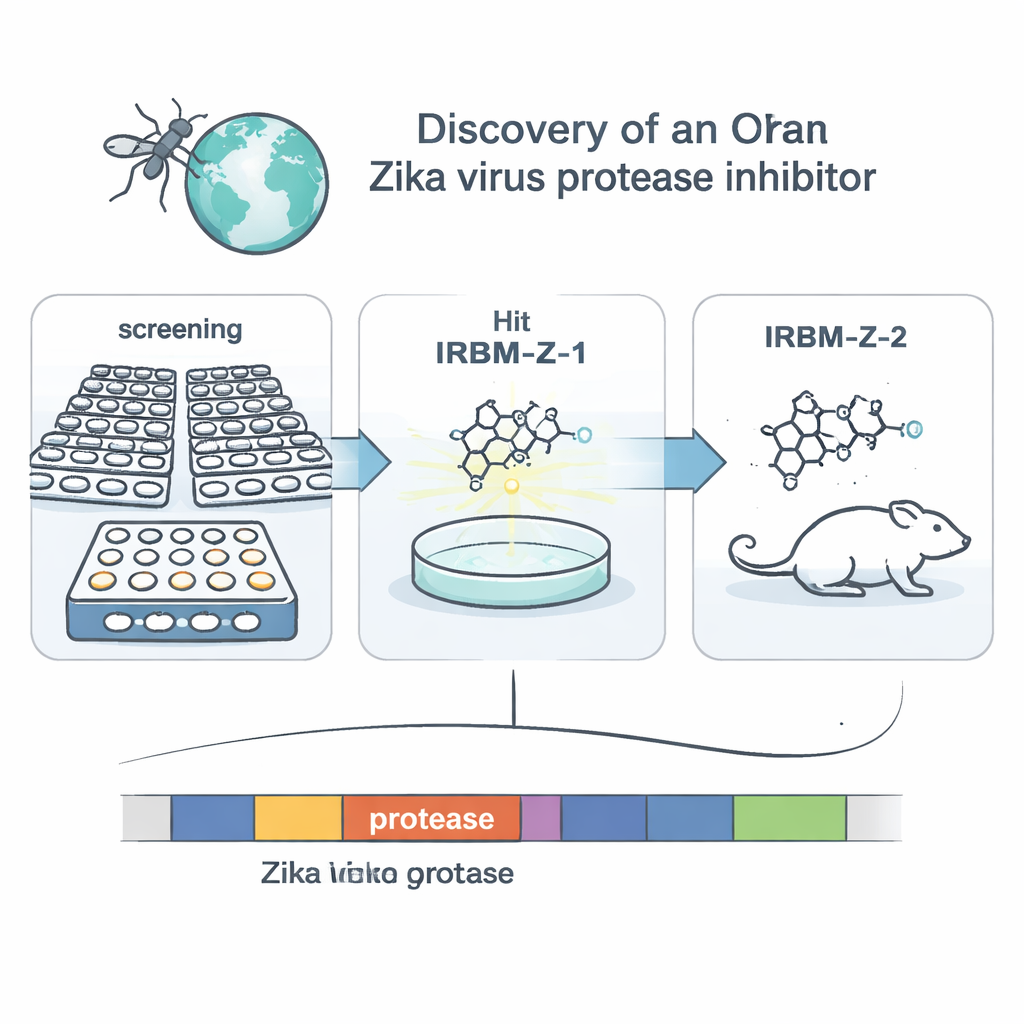
De onderzoekers richtten zich op een viraal enzym dat NS2B–NS3-protease heet. Deze moleculaire "schaar" knipt het grote startproteïne van het virus in de stukken die nodig zijn om nieuwe virussen te bouwen, waardoor het een aantrekkelijke doelwit is voor geneesmiddelen. In plaats van een medicijn te ontwerpen voor de voor de hand liggende knipplaats, gebruikte het team een celgebaseerd screeningssysteem dat Zika-replicatie nabootst in apennierscellen. Ze bouwden een gemodificeerd Zika-genoom, of replicon, dat structurele genen mist maar een luciferase-reporter draagt zodat lichtuitstoot de virale kopieergraad volgt. Na het screenen van meer dan 120.000 kleine moleculen uit een nationale chemische bibliotheek selecteerden ze diegenen die het lichtsignaal sterk verminderden zonder de cellen te schaden, en kweekten vervolgens virusreplicons die resistent werden tegen elk treffer. Dit genetische speurwerk wees de protease aan als het belangrijkste doelwit voor een familie van verbindingen, geleid door een initiële molecule genaamd IRBM-Z-1.
Het enzym vastzetten in de verkeerde vorm
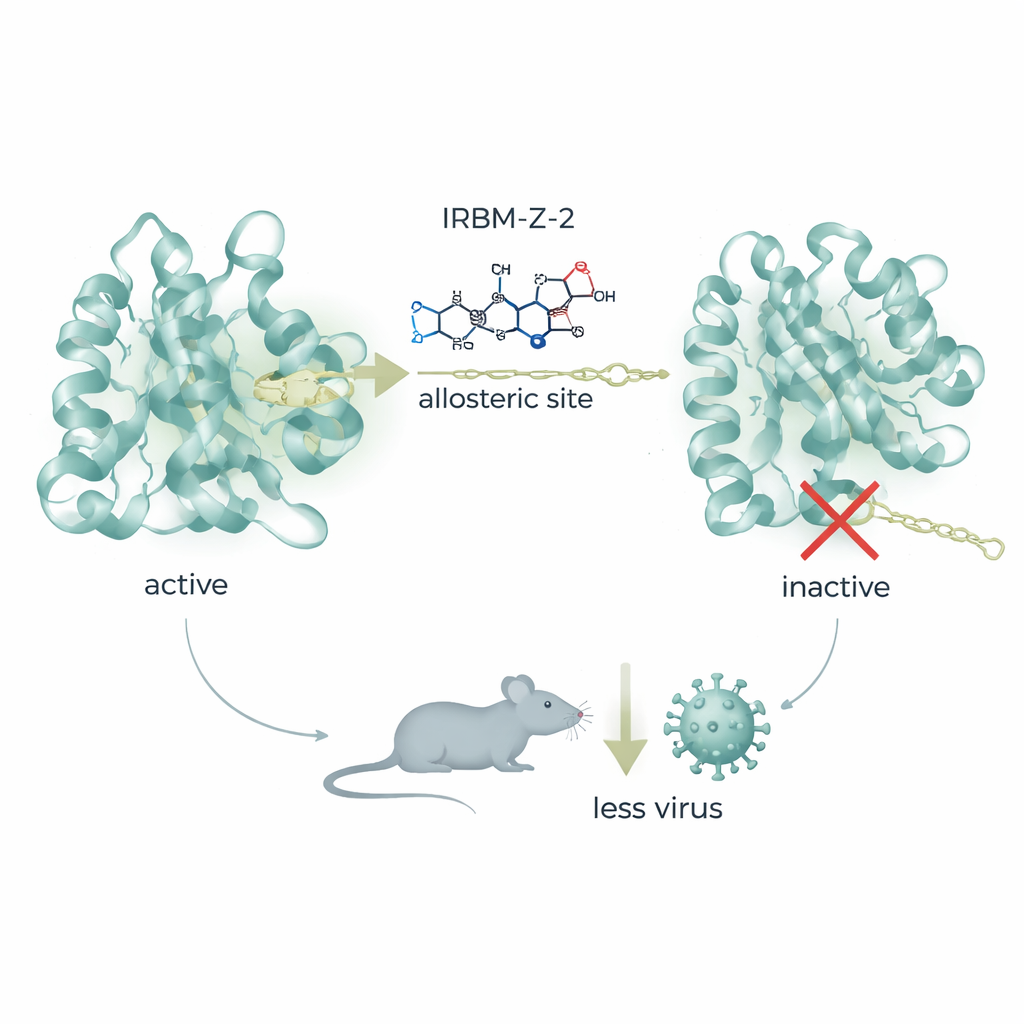
Biochemische tests toonden aan dat IRBM-Z-1 niet concurreerde met het gebruikelijke substraat bij de knipplaats. In plaats daarvan gedroeg het zich als een niet-competitieve, of allosterische, remmer—het bindt op een afzonderlijk pocket en voorkomt dat het enzym zijn actieve vorm aanneemt. Hoogresolutie-röntgenkristallografie onthulde dat de verbinding zich nestelt in een voorheen onbekend pocket ver van het katalytische centrum. Daar vormt zijn ongewone "N-acylsydnone imine"-kern een web van waterstofbruggen en stapelingsinteracties die een sleutelregio van het protease in een open, inactieve conformatie duwen. Een enkele aminozuurverandering in dit gebied, op positie 156, maakt het virus resistent, wat benadrukt hoe precies de verbinding van deze verborgen plek gebruikmaakt. Dit pocket verschilt ook van allosterische sites die in verwante flavivirussen zijn beschreven, en biedt daarmee een werkelijk nieuw aanknopingspunt voor geneesmiddelontwerp.
Van treffer tot beschermend geneesmiddel in muizen
Aan de hand van structurele inzichten verfijnde het team IRBM-Z-1 tot een krachtiger molecule genaamd IRBM-Z-2. Deze verbeterde verbinding blokkeert de Zika-protease bij nanomolaire concentraties, remt viraal replicatie krachtig in meerdere celtypen en toont activiteit tegen verwante dengue- en Westnijl-proteases terwijl humane enzymen gespaard blijven. In dierenstudies vertoonde IRBM-Z-2 gunstige "geneesmiddelachtige" eigenschappen: het was stabiel in het lichaam, had goede orale opname en handhaafde bloedspiegels ruim boven de concentraties die nodig zijn om het virus uit te schakelen, zonder duidelijke tekenen van toxiciteit. In sterk vatbare AG129-muizen geïnfecteerd met Zika verlaagde dagelijkse behandeling—zowel via injectie als oraal—de hoeveelheid viraal RNA in het bloed drastisch, voorkwam gewichtsverlies en ziekteverschijnselen, en liet alle behandelde dieren overleven, terwijl onbehandelde controles aan de infectie ten onder gingen.
Wat dit kan betekenen voor toekomstige uitbraken
Gezamenlijk introduceren deze bevindingen een nieuwe klasse van Zika-antiviralia die werken door een cruciaal viraal enzym in een inactieve houding te bevriezen in plaats van de actieve site rechtstreeks te blokkeren. Omdat IRBM-Z-2 oraal kan worden toegediend, sterke bescherming toont in strenge muismodellen en tot nu toe een schoon veiligheidsprofiel heeft, valt het op als een veelbelovende kandidaat voor verdere ontwikkeling als preventief middel—mogelijk om zwangere vrouwen, zorgverleners en reizigers te beschermen als Zika weer opduikt. Breder gezien kan het nieuw ontdekte allosterische pocket soortgelijke geneesmiddelen tegen verwante virussen inspireren en zo een nieuw front openen in de strijd tegen door muggen overgedragen ziekten.
Bronvermelding: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Trefwoorden: Zika-virus, antivirale geneesmiddelen, proteaseremmer, allosterische modulatie, door muggen overgedragen ziekte