Clear Sky Science · nl
FCHo2, niet talin, maakt inside-out-activatie van integrine ɑvβ5 mogelijk in gekromde adhesies
Hoe cellen de vorm van hun omgeving voelen
Ons lichaam is opgebouwd uit cellen die voortdurend hun omgeving vastgrijpen, trekken en duwen om te bewegen, delen of op hun plaats te blijven. Dit artikel laat zien dat cellen niet alleen voelen hoe stijf hun omgeving is — ze lezen ook de vorm ervan. Door een speciaal hechtsysteem te ontdekken dat alleen wordt geactiveerd waar het celmembraan sterk gekromd is, tonen de auteurs aan dat cellen verschillende interne "grepen" gebruiken voor vlakke versus vezelachtige omgevingen, met belangrijke gevolgen voor hoe weefsels zich vormen en hoe kanker zich verspreidt.
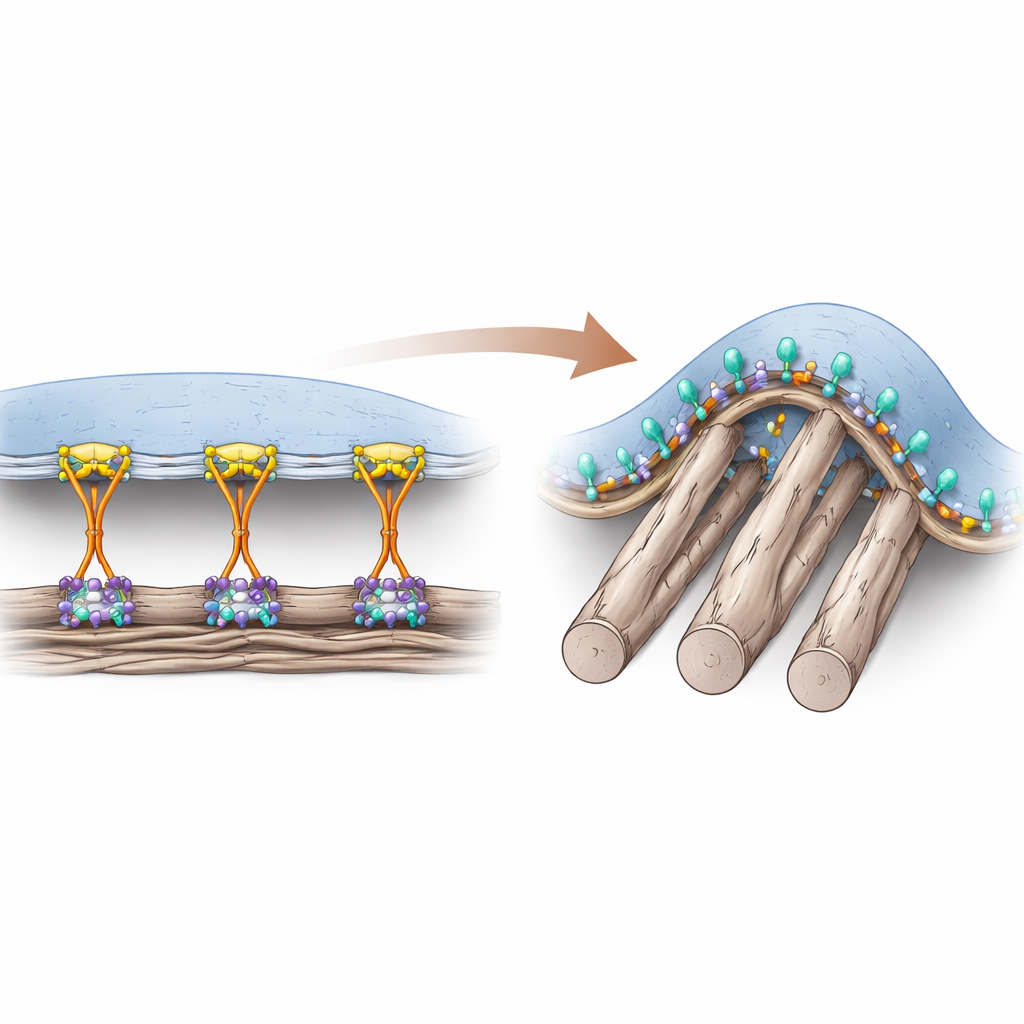
Twee manieren waarop cellen zich vasthouden
Cellen hechten zich aan het proteïnerijke materiaal om hen heen met behulp van receptoren op het oppervlak die integrines worden genoemd. Jarenlang dachten onderzoekers dat een hulp-eiwit genaamd talin absoluut noodzakelijk was om integrines van binnenuit "aan" te zetten, waardoor sterke bevestiging mogelijk wordt in klassieke ankerplaatsen die bekendstaan als focale adhesies. Deze adhesies ontstaan voornamelijk op vlakke, stijve oppervlakken en geleiden grote trekkrachten via het celcytoskelet. In levende weefsels zijn veel van de omringende vezels echter zacht en cilindrisch, waardoor gekromde contactpunten ontstaan die deze krachtintensieve structuren niet gemakkelijk ondersteunen. De auteurs vonden eerder een ander type adhesieve structuur, een zogenoemde gekromde adhesie, die precies daar verschijnt waar het membraan zich om dunne vezels heen buigt en die afhankelijk is van een specifieke integrine, αvβ5.
Gekromde grepen gebruiken een andere helper
In de nieuwe studie laat het team zien dat talin, hoewel nog aanwezig, niet de sleutelschakelaar is voor activatie van integrine αvβ5 in gekromde adhesies. In plaats daarvan neemt een krumingssensor-eiwit genaamd FCHo2 deze rol over. Met behulp van nauwkeurig geconstrueerde nano-balkjes en -pilaren om celmembranen op gecontroleerde wijze te buigen, observeerden ze dat αvβ5 sterk clustert op gekromde plekken, maar alleen wanneer FCHo2 kan binden aan een zeer korte sequentie — een HDRRE-motief — net aan de binnenkant van de cel op de β5-staart. Wanneer dit motief wordt verstoord, functioneert de integrine nog wel in focale adhesies maar kan ze geen gekromde adhesies meer vormen. Het onderdrukken van FCHo2 laat de klassieke focale adhesies grotendeels intact, maar wist de gekromde adhesies uit, terwijl het verwijderen van talin de focale adhesies sterk verzwakt maar de gekromde adhesies grotendeels ongemoeid laat.
Een enkele aminozuur-omslag als vormkeuze
Een raadsel was waarom een nauw verwante integrine, αvβ3, geen gekromde adhesies kan vormen hoewel zijn binnenstaart er zeer vergelijkbaar uitziet met die van β5. Door domeinen tussen de twee integrines te verwisselen en puntmutaties in te voeren, identificeerden de auteurs één beslissende positie in de buurt van de talin-bindingsplaats: de meeste β-integrines hebben een tryptofaan (W), maar β5 heeft uniek een tyrosine (Y766). Toen de tyrosine van β5 werd vervangen door tryptofaan, verloor de integrine haar vermogen deel te nemen aan gekromde adhesies en gedroeg ze zich meer als β3, waarbij ze alleen focale adhesies prefereerde. De omgekeerde verandering — het plaatsen van tyrosine in het β3-achtige chimera — herstelde de gevoeligheid voor krumning. Verdere experimenten met varianten die gefosforyleerde of niet-gefosforyleerde toestanden van deze tyrosine nabootsen, suggereren dat chemische modificatie van dit aminozuur de integrine kan bevoordelen naar óf vlakke, hoge-kracht focale adhesies óf gekromde, lage-kracht adhesies.
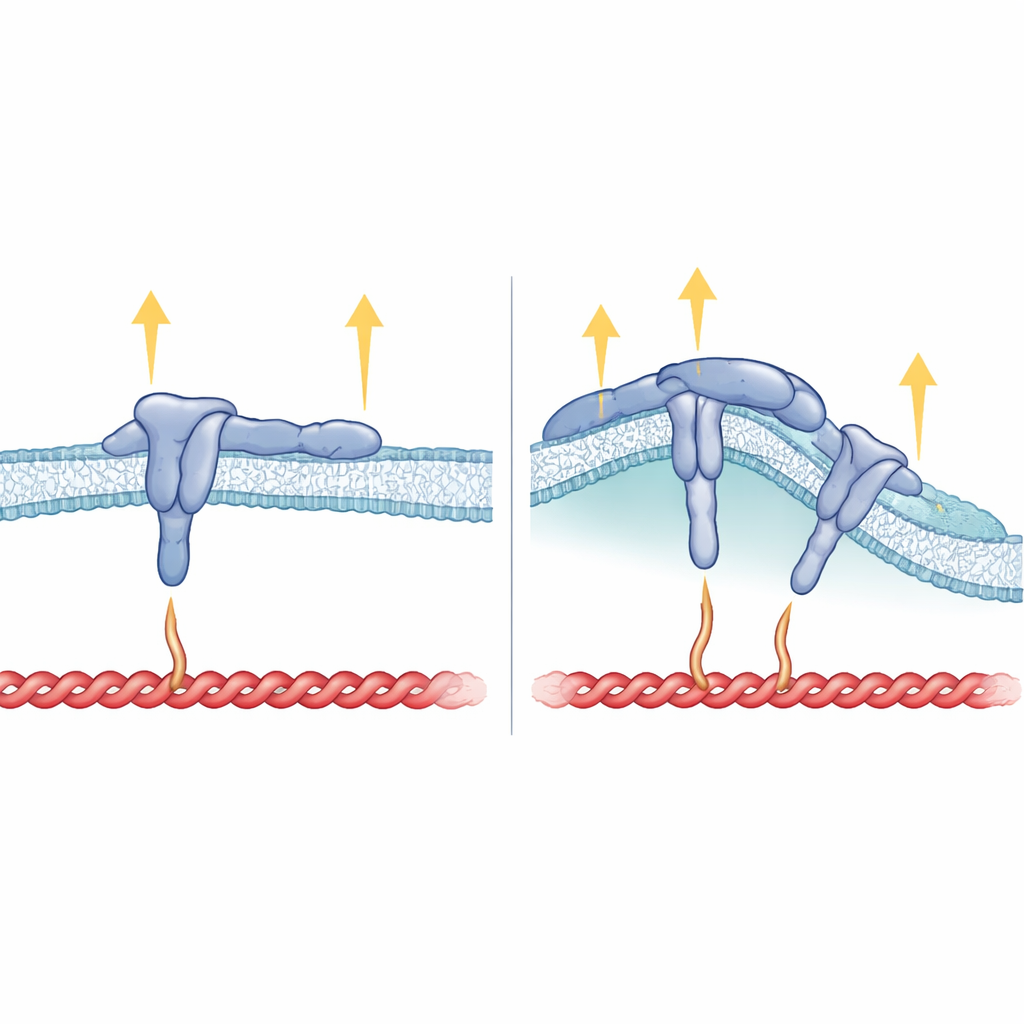
Hoe membraangevorm, integrinestructuur en kracht samenkomen
Buiten de binnenstaart bleek ook het deel van β5 dat door het membraan loopt van cruciaal belang. Toen de onderzoekers het transmembraangedeelte van β5 vervingen door dat van β3, kon de resulterende integrine nog focale adhesies vormen maar prefereerde ze geen gekromde plekken meer en volgde ze FCHo2 niet. Dit suggereert dat de manier waarop de integrine in het membraan gepositioneerd is, helpt het HDRRE-motief te oriënteren zodat FCHo2 zich kan vastklampen op gekromde regio’s en ligandgebonden, actieve αvβ5 kan stabiliseren. In gekromde adhesies lijkt talin slechts een meer afstandelijke plek op de integrinstaart te raken en draagt het geen grote spanning, wat verklaart waarom andere krachtbeluste componenten zoals vinculine, tensine en kindlin daar grotendeels afwezig zijn. In contrast grijpt talin in focale adhesies zowel nabij als verder gelegen plaatsen op de staart en het membraan, ondersteunt sterke trekkrachten en blokkeert daarmee de toegang van FCHo2 tot hetzelfde gebied.
Wat dit betekent voor celgedrag
Voor een niet-specialist is de kernboodschap van dit werk dat cellen twee afzonderlijke "gripmodi" hebben om zich aan hun omgeving vast te hechten. Op vlakke, stijve gebieden gebruiken ze talin-gedreven focale adhesies die zijn gebouwd om hard te trekken. Op zachte, vezelachtige en gekromde structuren schakelen ze over op FCHo2-gedreven gekromde adhesies die integrine αvβ5 stabiliseren met veel lagere krachten. Een kleine verandering in de sequentie van de integrine — en of die plek chemisch gemodificeerd is — helpt te beslissen welke modus wordt gebruikt. Dit dubbele systeem stelt cellen in staat zowel stijfheid als vorm in driedimensionale omgevingen te interpreteren, en beïnvloedt hoe ze migreren, weefsels organiseren en mogelijk hoe ze tijdens ziekte invasief gedrag vertonen.
Bronvermelding: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Trefwoorden: integrines, celhechting, membraan-krumning, FCHo2, cytoskelet