Clear Sky Science · nl
Een experimenteel geïnformeerd polymeermodel onthult de organisatie van genlocussen met hoge resolutie
Hoe vouwing van DNA de celidentiteit vormt
Elke cel in uw lichaam draagt in wezen hetzelfde DNA, maar zenuwcellen, huidcellen en stamcellen gedragen zich heel verschillend. Een belangrijke reden is hoe dat DNA gevouwen en verpakt is in de celkern. Deze studie introduceert een nieuwe manier om die vouwing in opmerkelijk detail “zichtbaar” te maken, en legt een verband tussen de fysieke rangschikking van DNA en of belangrijke genen aan- of uitgeschakeld zijn. Door experimenten te combineren met fysica-gebaseerde computersimulaties onthullen de auteurs verborgen klonten genetisch materiaal die lijken te functioneren als basiselementen van genoomorganisatie.
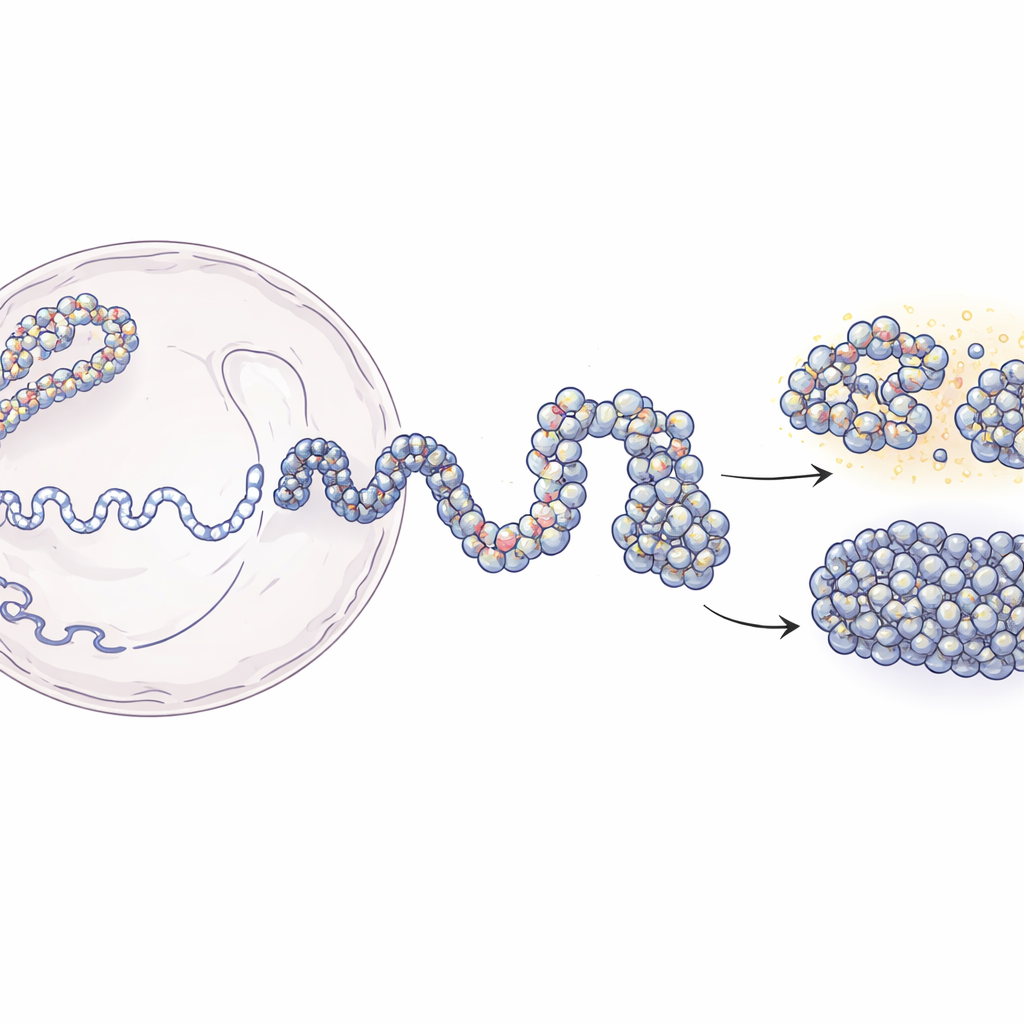
Van lange DNA-draden naar 3D-genoomkaarten
Binnenin de kern is DNA omwikkeld rond eiwitspoelen die nucleosomen worden genoemd, waardoor een kralen-aan-een-draadstructuur ontstaat die bekendstaat als chromatine. Moderne technieken zoals Hi-C en Micro-C kunnen ons vertellen welke stukjes DNA in 3D dicht bij elkaar liggen, maar ze geven meestal vage, populatiegemiddelde momentopnames. Experimentele methoden die individuele nucleosomen lokaliseren geven daarentegen scherpe lokale details, maar weinig idee van de grotere structuur. Dit werk overbrugt die kloof. De auteurs beginnen met laagresolutie contactkaarten die aangeven hoe vaak verre DNA-segmenten elkaar raken, en combineren die vervolgens met experimentele kaarten van nucleosoomposities. Met principes uit de polymeerfysica bouwen ze gesimuleerde 3D-ensembles van chromatine die passen bij de experimentele gegevens maar structuren tot op enkele tientallen DNA-basen resolueren.
Een tweestapsstrategie om chromatine te herbouwen
De modelleringsaanpak ontvouwt zich in twee hoofdfasen. Eerst gebruikt het team Hi-C-gegevens om vele mogelijke grootschalige vormen te genereren van een DNA-stretch van 200.000 basen, waarbij chromatine wordt behandeld als een flexibele keten waarvan segmenten van 5.000 basen zachtjes worden gestuurd om contacts te maken of te vermijden zoals in de experimenten waargenomen. Deze grove structuren vangen het algehele vouwpatroon dat eiwitten in de cel helpen creëren. In de tweede fase wordt elke grote parel vervangen door een veel fijnere keten bestaande uit individuele nucleosomen en de korte DNA-verbindingen daartussen. De posities van deze nucleosomen komen uit een enzym-gebaseerde mapmethode (MNase-seq) die laat zien waar ze doorgaans langs het genoom zitten. De fijnmazige ketens mogen vervolgens vouwen terwijl ze nog steeds de bredere architectuur respecteren. Wanneer de onderzoekers hun hoogresolutiemodellen weer "vervagen" naar experimentele resoluties, reproduceren ze zowel Hi-C- als Micro-C-contactkaarten met hoge nauwkeurigheid.
Het ontdekken van nucleosoom-blobs als structurele eenheden
Wanneer de auteurs inzoomden op hun gesimuleerde structuren, doemde een opvallend patroon op: nucleosomen lagen niet gelijkmatig verdeeld, maar verzamelden zich in onregelmatige clusters die de auteurs nucleosoom-blobs noemen. Deze blobs lijken op de klonterige structuren die eerder zijn gezien in superresolutie-microscoopbeelden van echte cellen. Door duizenden gesimuleerde snapshots te analyseren liet het team zien dat deze blobs verlengd zijn, niet bolvormig, en typisch meerdere dicht op elkaar gepakte nucleosomen bevatten. Cruciaal is dat contacts binnen deze blobs nauw corresponderen met de domeinachtige interactieblokken die in experimentele data worden gezien, wat aangeeft dat blobs geen willekeurige toevalligheden zijn maar fundamentele 3D-eenheden van chromatineorganisatie. De simulaties voorspellen zelfs extra subtiele domeingrenzen die experimenteel moeilijk te detecteren zijn, wat suggereert dat dit fysieke model fijnmazige kenmerken kan blootleggen die door ruis in de data worden verhuld.
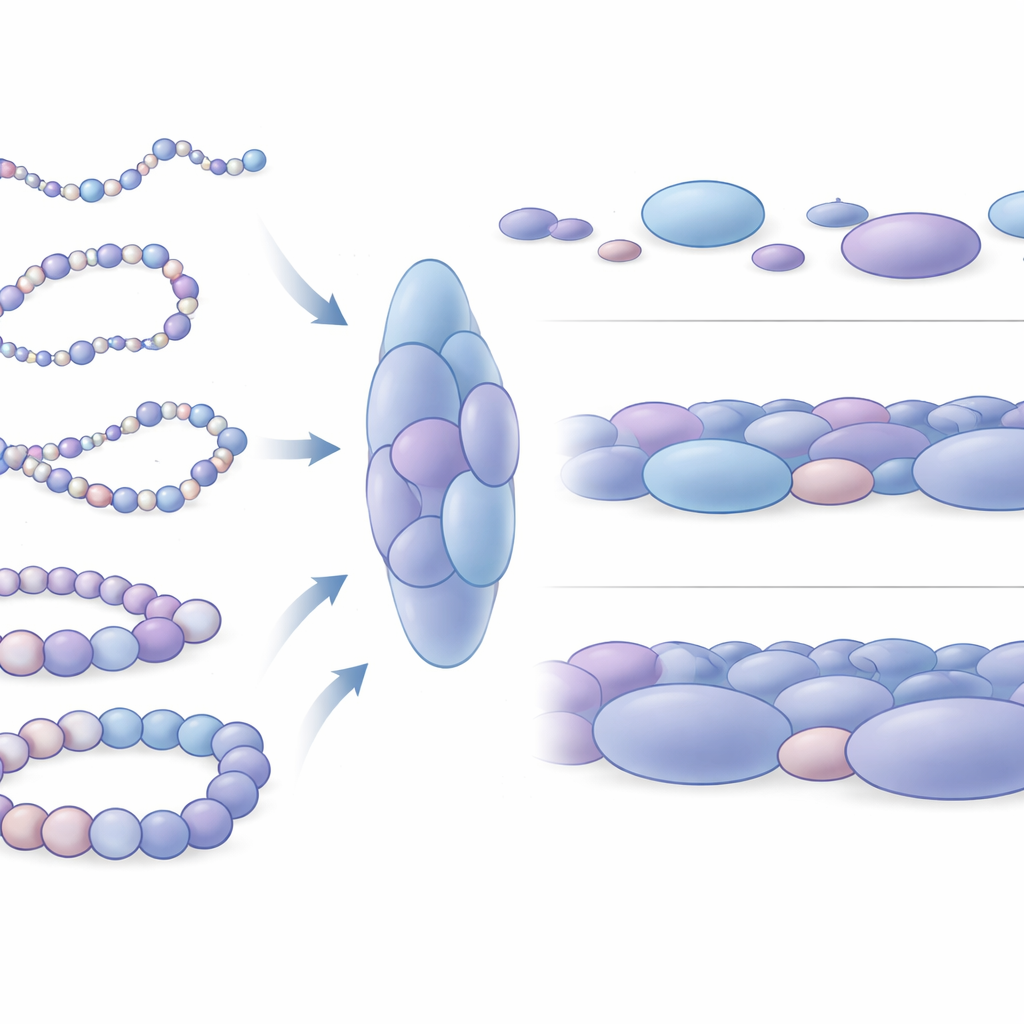
Hoe pakverschillen genactiviteit weerspiegelen
De onderzoekers vroegen zich vervolgens af hoe deze blobs verschillen rond actieve genen versus stille genen. Ze concentreerden zich op vier goed bestudeerde stukken menselijk DNA, waaronder twee genen die stamcellen helpen flexibel en ongedifferentieerd te blijven (Nanog en Lin28A) en twee ontwikkelingscontrolegenen (HoxB4 en HoxA13) die in dezelfde cellen uitgeschakeld zijn. Rond de inactieve genen waren blobs gemiddeld groter en strakker verpakt, waarbij nucleosomen vaker volledig gesloten lokale arrangementen vormden. Daarentegen waren blobs nabij actieve genen kleiner, enigszins losser en meer gevarieerd. Op grotere schaal nam het DNA rond actieve genen veel meer verschillende vormen aan en was het mechanisch buigzamer, terwijl de regio’s rond stille genen zich gedroegen als stijvere segmenten chromatine. Dit mechanische verschil beïnvloedt waarschijnlijk hoe gemakkelijk verre regelgevende DNA-elementen elkaar kunnen ontmoeten en samenwerken met genregelaars.
Waarom dit belangrijk is voor het begrijpen van gencontrole
Samen schetsen de bevindingen een beeld waarin het genoom is opgebouwd uit dynamische clusters van nucleosomen waarvan grootte, vorm en onderlinge afstand helpen bepalen of nabijgelegen genen toegankelijk zijn of opgesloten. Het nieuwe model brengt experimentele contactgegevens, nucleosoomkaarten en fysieke principes samen in één kader dat verklaart hoe stamcelgenen flexibel en interactief kunnen blijven, terwijl ontwikkelingsgenen opgesloten blijven in stijvere, compactere buurten. Voor niet-specialisten is het kernidee dat genactiviteit niet alleen door de DNA-sequentie wordt bepaald; ze hangt ook af van hoe dat DNA in driedimensionale structuren is gevouwen. Door nucleosoom-blobs als basiselementen van die vouwing te onthullen, biedt dit werk een krachtige route om microscopische genoomarchitectuur te koppelen aan grootschalige processen zoals ontwikkeling, celidentiteit en ziekte.
Bronvermelding: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Trefwoorden: vouwing van chromatine, nucleosoomclusters, 3D-genoomorganisatie, genregulatie, polymeermodelering