Clear Sky Science · nl
Nitroreductase-geïnduceerde indazoolvorming
Van eenvoudige ingrediënten naar waardevolle geneesmiddelen
Veel moderne geneesmiddelen zijn opgebouwd rond een handvol populaire moleculaire “frames” die goed passen op biologische doelwitten. Eén van deze frames, indazool genoemd, komt voor in medicijnen tegen kanker en ernstige misselijkheid. Tot nu toe vereiste de bereiding van indazolen meestal agressieve chemicaliën, hoge temperaturen en metalen die milieubelastend zijn. Deze studie laat zien hoe wetenschappers natuurlijke enzymen kunnen inzetten om indazolen zacht in water te laten ontstaan, wat de deur opent naar groenere methoden voor de productie van belangrijke farmaceutica.
Waarom deze ringvormige moleculen belangrijk zijn
Ontwerpers van geneesmiddelen hergebruiken vaak bepaalde ringvormige structuren omdat ze betrouwbaar met eiwitten in het lichaam interageren. Indazolen zijn zo’n favoriet en komen voor in goedgekeurde medicijnen voor kanker en bij door chemotherapie veroorzaakte misselijkheid. Chemici kennen al verschillende manieren om indazolen te maken, maar de gangbare routes vertrouwen op reactieve bouwstenen, sterke basen of zuren, en metaal-katalysatoren zoals koper en palladium. Deze methoden werken wel, maar ze produceren afval, vragen veel energie en vormen veiligheidsrisico’s, wat botst met de toenemende drang naar duurzame productie in de farmaceutische industrie.
Enzymen als zachte bouwvakkers
In plaats van atomen samen te dwingen met hitte en sterke reagentia, wenden de auteurs zich tot biokatalyse — het gebruik van enzymen, de natuurlijke katalysatoren, om reacties in water bij kamertemperatuur te laten verlopen. Ze richten zich op enzymen die nitroreductasen worden genoemd en die normaal helpen cellen te ontgiften van nitrohoudende verbindingen door stapsgewijze reductie. Het team redeneerde dat als een bepaalde tussenstap in dit reductiepad precies op het juiste moment vrijkomt, deze zichzelf zou kunnen vouwen en spontaan het kenmerkende indazoolringsysteem vormt. Met twee verschillende nitroreductasen tonen ze aan dat eenvoudige 2-nitrobenzylamine-startmaterialen soepel worden omgezet in indazolen met uitstekende efficiëntie, vaak boven 99% conversie, onder milde, aquatische omstandigheden.
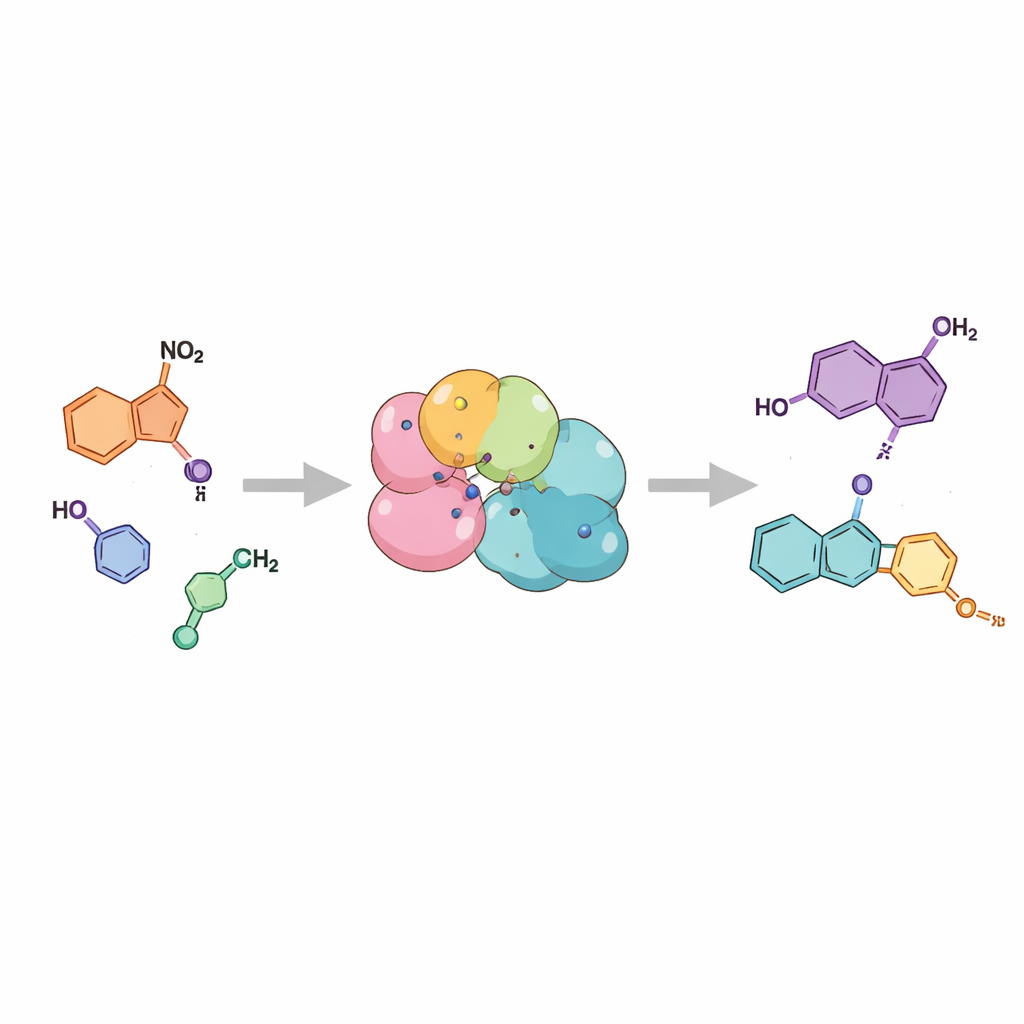
In kaart brengen wat de enzymen kunnen
Om te testen hoe algemeen deze strategie werkt, voedden de onderzoekers de enzymen met een reeks verwante startmaterialen met verschillende zijgroepen en positievariaties op de aromatische ring. Ze ontdekten dat beide enzymen een breed scala aan chemische substituties tolereerden, van kleine groepen zoals methyl tot omvangrijkere ringsystemen en diverse chloor-, broom- en methoxysubstituenten. In veel gevallen verliepen de reacties schoon naar het gewenste indazool, met geïsoleerde opbrengsten die hoog genoeg waren om praktisch te zijn. De manier waarop het startmateriaal was gedecoreerd bepaalde ook welke van twee nauw verwante indazoolvormen ontstond, een eigenschap die belangrijk is omdat beide vormen van belang kunnen zijn in geneesmiddelontwerp. Hetzelfde concept liet zich zelfs uitbreiden om een grotere verwant van indazolen te maken, cinnolines genoemd, wat de veelzijdigheid van de aanpak benadrukt.
Een tweestaps enzymatische assemblagelijn opbouwen
De indazolen in dit werk ontstaan niet direct uit speciale startmaterialen; in plaats daarvan bouwde het team een korte enzymatische assemblagelijn beginnend met goedkope bouwstenen. In de eerste stap voegt een andere klasse enzymen, een imine-reductase, een eenvoudige aldehyde en een amine samen om de benodigde 2-nitrobenzylamine te vormen. In de tweede stap zet de nitroreductase dit intermediair om in de indazoolring. Door zorgvuldig de hoeveelheden enzymen en het systeem voor het recyclen van hun cofactoren af te stemmen, voerden de auteurs deze twee-enzymkaskade op preparatieve schaal uit, startend vanaf 50 milligram aldehyde in water. Ze verkregen verschillende indazoolproducten in goede totale opbrengsten, inclusief voorbeelden met verschillende zijketens die later verder aangepast kunnen worden voor geneesmiddelenonderzoek.
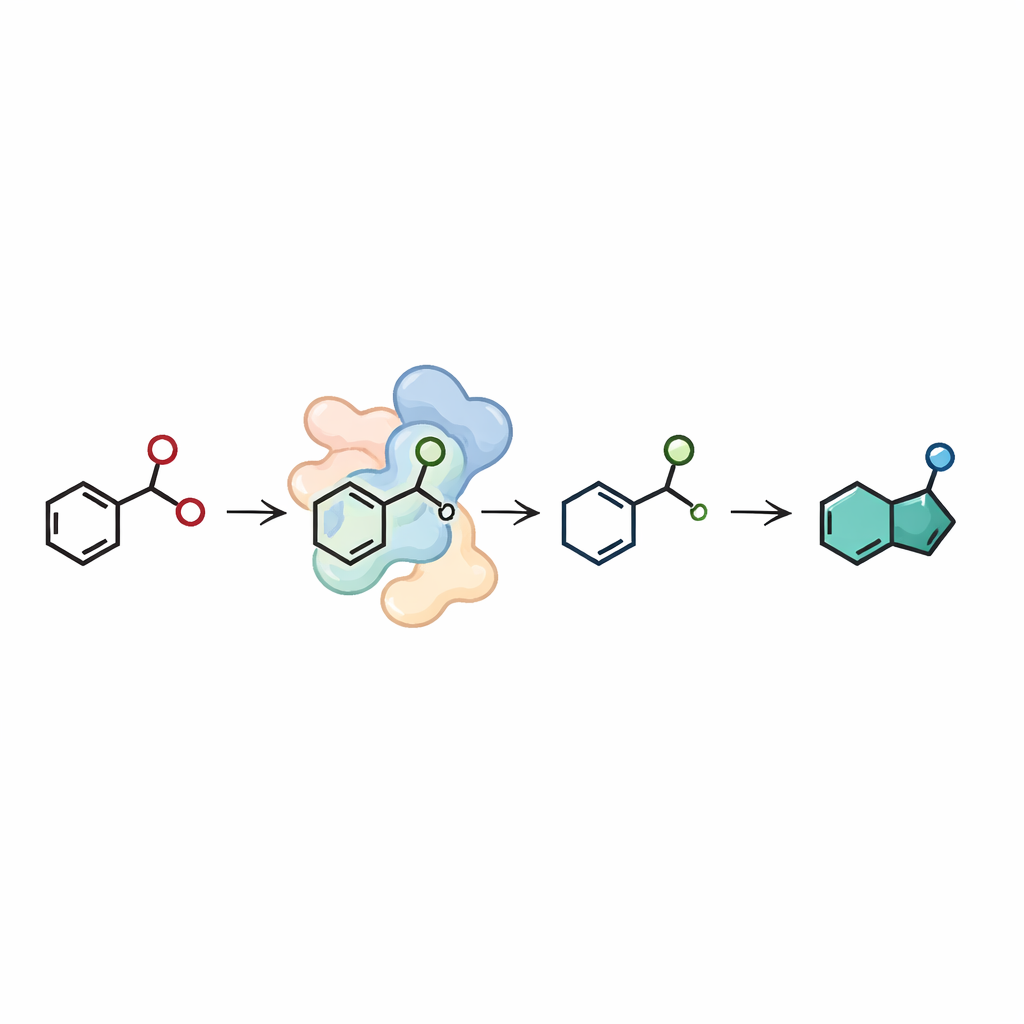
Een schonere route naar complexe geneesmiddeldingrediënten
Voor de niet-specialist is de kernboodschap dat de onderzoekers natuurlijke katalysatoren hebben geleerd een medisch belangrijk ringsysteem te assembleren op een manier die milder is voor zowel mensen als het milieu. Hun enzym-gebaseerde route vermijdt gevaarlijke stikstof–stikstofreagentia en kostbare metaal-katalysatoren, werkt in water bij gematigde temperaturen en kan worden gecombineerd met andere enzymen tot een efficiënte mini-fabriek. Dit werk voegt een krachtig nieuw instrument toe aan de gereedschapskist van de chemicus, brengt duurzame productie een stap dichterbij en levert de farmaceutische wereld veelzijdige indazoolbouwstenen voor toekomstige geneesmiddelen.
Bronvermelding: Terholsen, H., Medema, L., Chernyshova, E. et al. Nitroreductase-triggered indazole formation. Nat Commun 17, 2261 (2026). https://doi.org/10.1038/s41467-026-68926-y
Trefwoorden: biokatalyse, indazoolsynthese, nitroreductase, groene chemie, enzymkaskades