Clear Sky Science · nl
Klonaire uitbreiding van cytotoxische CD8⁺ T‑cellen bij lecanemab‑geassocieerde ARIA
Waarom dit belangrijk is voor mensen met Alzheimer
Lecanemab is een van de eerste middelen die amyloïd uit de hersenen kan verwijderen en de geheugenachteruitgang bij de ziekte van Alzheimer in bescheiden mate kan vertragen. Maar sommige patiënten die deze behandeling krijgen ontwikkelen hersenzwelling of kleine hersenbloedingen, veranderingen die op MRI‑scans zichtbaar zijn en samengebracht worden onder de term amyloid‑gerelateerde beeldvormingsafwijkingen (ARIA). Deze studie onderzoekt een cruciale vraag voor patiënten en familie: wat gebeurt er in het immuunsysteem wanneer ARIA optreedt, en zou een eenvoudige bloedtest ooit kunnen helpen voorspellen wie het meest risico loopt?
De belofte en het risico van een nieuwe Alzheimer‑behandeling
Lecanemab is een antilichaam dat via een infuus wordt toegediend en zich richt op ophopingen van een eiwit genaamd amyloïde‑beta, een kenmerk van de ziekte van Alzheimer. Door het lichaam te helpen amyloïde te verwijderen, kan het cognitieve achteruitgang enigszins vertragen. Maar dit voordeel gaat gepaard met een veiligheidsprobleem: sommige mensen ontwikkelen ARIA, wat gebieden van hersenzwelling of puntvormige bloedingen kan omvatten. Deze bijwerkingen vereisen frequente MRI‑controle en kunnen beperken wie de geneesmiddel ontvangt. Niet iedereen is even kwetsbaar—dragers van een genvariant genaamd APOE4 lopen een hoger risico—maar genen alleen verklaren niet waarom ARIA optreedt, vooral vroeg na aanvang van de behandeling. Omdat lecanemab via de bloedbaan wordt toegediend, redeneerden de auteurs dat nauwkeurige bestudering van immuuncellen in het bloed vroegtijdige waarschuwingssignalen of zelfs mechanismen zou kunnen onthullen die de behandeling koppelen aan vaatschade in de hersenen. 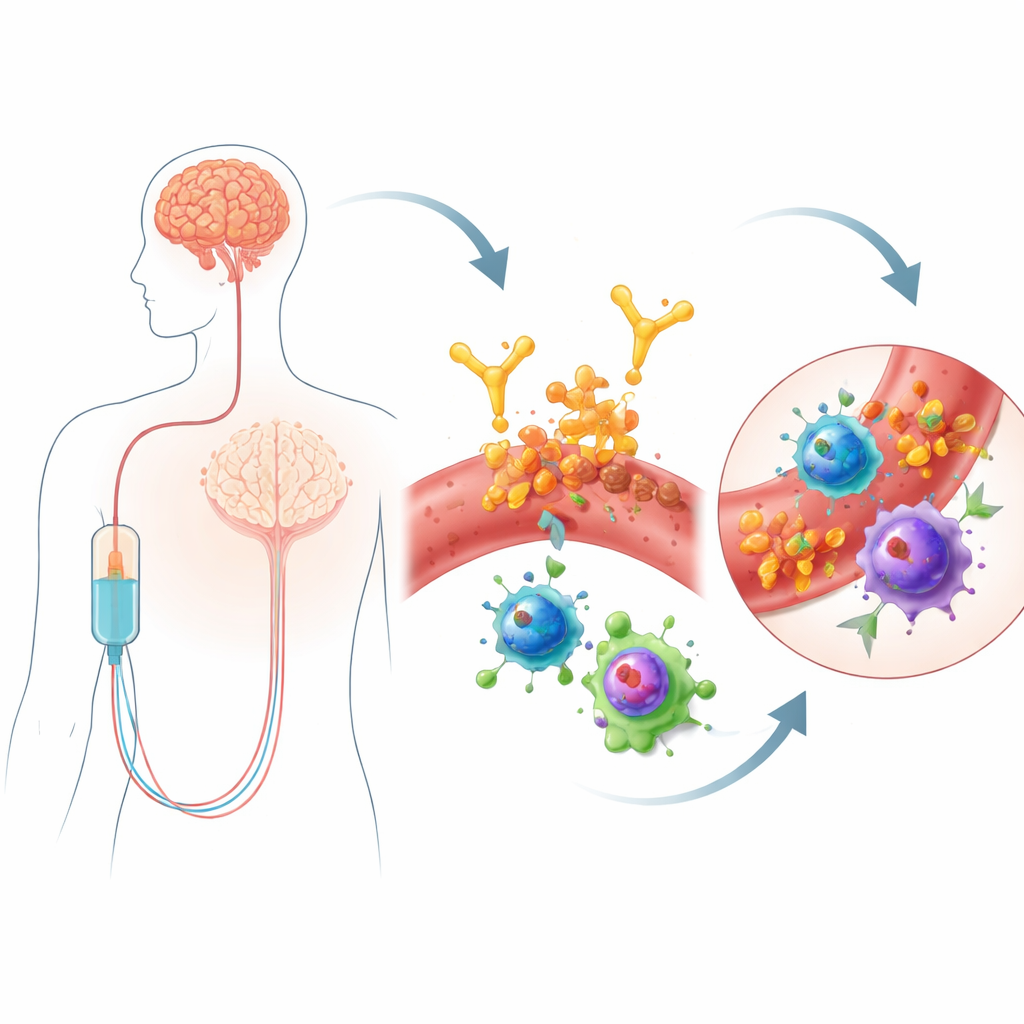
Immuuncellen volgen bij patiënten met en zonder ARIA
De onderzoekers bestudeerden zes mensen met Alzheimer die lecanemab ontvingen bij een regionaal geheugenpand. Drie ontwikkelden verschillende vormen van ARIA, en drie overeenkomstige patiënten (vergelijkbaar in leeftijd, geslacht, APOE‑genotype en aantal infusen) deden dat niet. Bloed werd afgenomen vlak voor de infusen, en het team gebruikte een intensieve "multi‑omische" aanpak: single‑cell RNA sequencing om te lezen welke genen in duizenden individuele immuuncellen aan stonden, antilichaamgebonden tags om celtypen te definiëren, sequencing van T‑cellenreceptoren om klonen te volgen, en gerichte metabolomica om honderden kleine moleculen betrokken bij celmetabolisme te meten. Dit stelde hen in staat niet alleen vast te stellen welke celtypen aanwezig waren, maar ook hoe actief ze waren, welke brandstoffen ze gebruikten en of specifieke T‑cel‑families zich uitbreidden als reactie op een trigger.
Uitbreiding van sterk bewapende killer‑T‑cellen
Er kwam een duidelijk patroon naar voren bij de patiënten die ARIA ontwikkelden. Vergeleken met de controles hadden zij een hoger aandeel CD8 "killer"‑T‑cellen en minder CD4 helper‑T‑cellen. Binnen de CD8‑pool vielen twee subgroepen op: effector‑geheugencellen en een terminaal gedifferentieerde vorm bekend als TEMRA‑cellen. Deze TEMRA‑cellen zijn als veteraan‑soldaten—hooggespecialiseerd voor aanval, met sterke machinerie om doelcellen te doden. Bij ARIA‑positieve patiënten waren TEMRA‑cellen talrijker, meer klonaal uitgebreid (wat betekent dat bepaalde T‑cel‑families waren vermenigvuldigd) en droegen ze genprogramma’s geassocieerd met cytotoxiciteit, migratie door bloedvaten en tekenen van chronische stimulatie. Vergelijkbare T‑celtoestanden zijn waargenomen bij veroudering, chronische infecties, multiple sclerose en in het ruggenmergvocht van mensen met Alzheimer, waar ze zich nabij bloedvaten en het hersenoppervlak kunnen ophopen.
Metabole herprogrammering en kruisgesprek met andere immuuncellen
Het team vond ook dat deze CD8‑effectorcellen hun metabolisme hadden heringesteld. In plaats van voornamelijk te vertrouwen op efficiënte energieproductie in mitochondriën, schakelden ze over naar glycolyse, een snellere maar minder efficiënte manier om energie te genereren die korte, intensieve activiteit ondersteunt. Metabolietmetingen in bloedcellen bevestigden dit: niveaus van lactaat en pyruvaat waren verhoogd, terwijl belangrijke componenten van de citroenzuurcyclus verlaagd waren, een patroon typisch voor inflammatoire immuuncellen. Monocyten, een ander type witte bloedcel, toonden complementaire veranderingen. Bij ARIA‑positieve patiënten zetten monocyten genen aan voor antigeenpresentatie, hechting aan andere cellen en productie van chemokinen—chemische signalen die T‑cellen aantrekken. Computationele modellering van ligand‑receptorparen suggereerde dat monocyten sterkere activatie‑ en homingsignalen naar CD8‑effectorcellen zonden, waardoor een omgeving ontstond die deze killer‑cellen aanmoedigt om de wanden van bloedvaten te benaderen.
Adrescodes die T‑cellen naar hersenvaten leiden
Aangezien deze studie alleen bloedmonsters nam, raadpleegden de auteurs een onafhankelijke single‑cell dataset van hersenen van lecanemab‑behandelde patiënten om te onderzoeken of dezelfde T‑celprogramma’s gekoppeld zijn aan vasculaire niches in de hersenen. Toen zij hun CD8‑subsets op deze hersenkaart projecteerden, lieten de TEMRA‑ en effector‑geheugencellen van ARIA‑positieve patiënten transcriptie‑"adrescodes" zien—combinaties van hechtingsmoleculen en chemokine‑receptoren—die overeenkwamen met endotheelcellen (bloedvatcellen) in de zieke hersenen. Deze signaturen suggereren dat de uitgebreide killer‑T‑cellen niet alleen sterk bewapend en metabool opgepept zijn, maar ook klaargemaakt om naar en in wisselwerking te treden met gestresseerde hersenbloedvaten op plaatsen van amyloïde‑clearance. 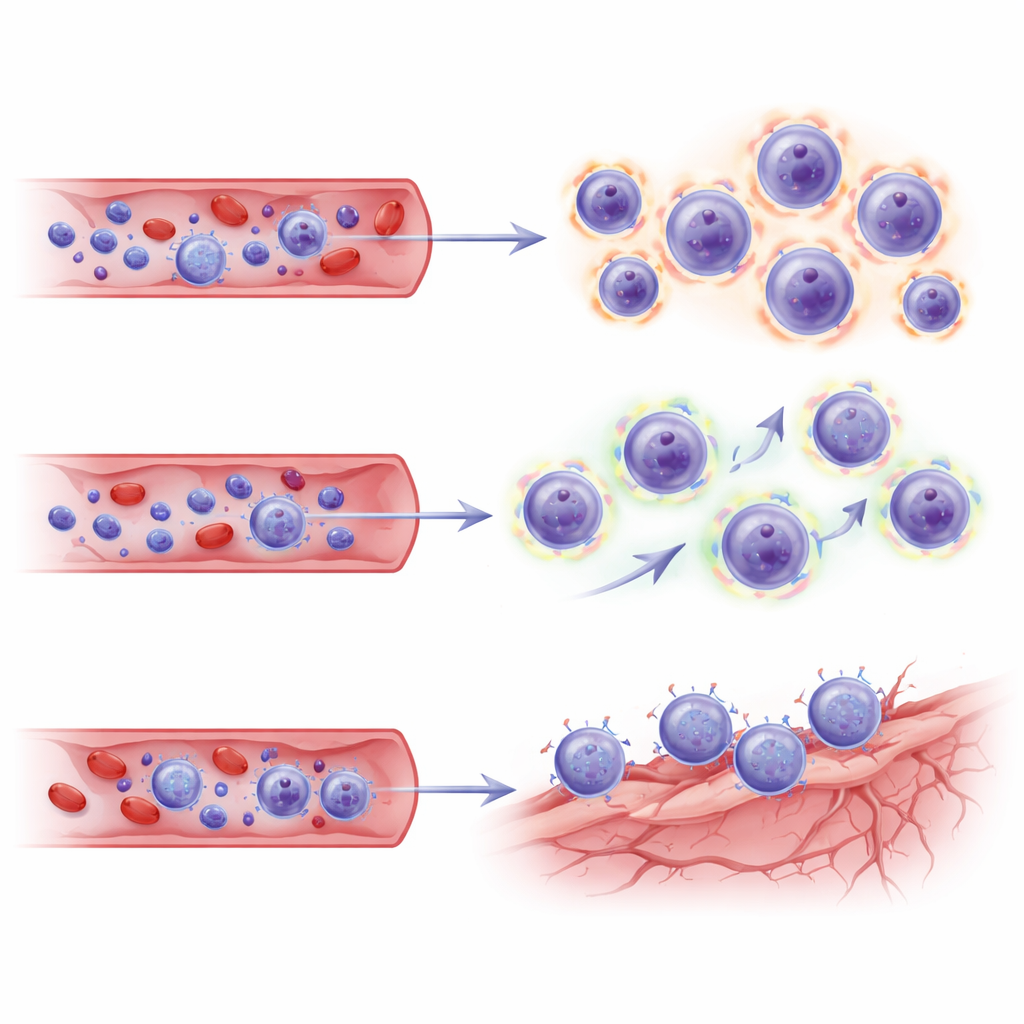
Wat dit zou kunnen betekenen voor patiënten en toekomstige zorg
Al met al schetst deze kleine maar gedetailleerde studie ARIA als meer dan een passieve bijwerking van amyloïde‑verwijdering. In plaats daarvan lijkt het gekoppeld aan een gecoördineerde immuunrespons in het bloed: uitbreiding en metabole activatie van specifieke killer‑T‑celklonen, versterkte signalering vanuit monocyten en moleculaire kenmerken die interactie met hersenbloedvaten bevorderen. Het werk bewijst niet dat deze cellen ARIA veroorzaken—immuunveranderingen kunnen een reactie op vaatschade zijn in plaats van de bron ervan—maar het levert toetsbare hypothesen en een blauwdruk voor bloedgebaseerde biomarkers. In de toekomst kan het meten van de overvloed en de metabole staat van CD8 TEMRA‑cellen, samen met sleutel‑signaalmoleculen, helpen patiënten met het hoogste ARIA‑risico te identificeren, controleschema’s te sturen of zelfs gerichte strategieën te inspireren om deze immuunrespons tijdelijk terug te schroeven terwijl de voordelen van amyloïde‑verwijderende therapieën behouden blijven.
Bronvermelding: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Trefwoorden: Ziekte van Alzheimer, lecanemab, immuuncellen, hersenslagaders, bijwerkingen van behandeling