Clear Sky Science · nl
TMEM63-eiwitten fungeren als mechanisch geactiveerde, door cholesterol gemoduleerde lipide-scramblasenzijn die bijdragen aan membraan-mechanische veerkracht
Hoe cellen intact blijven onder fysieke stress
De cellen in ons lichaam worden voortdurend geknepen, uitgerekt en geschud, of het nu in kloppende harten, werkende spieren of tumoren die door weefsel duwen is. Deze studie onthult hoe een familie membraaneiwitten, OSCA/TMEM63 genoemd, cellen helpt zulke zware mechanische krachten te doorstaan door de vetten in hun buitenste laag te herschikken. Inzicht in dit ingebouwde schokdemper-systeem kan nieuwe invalshoeken geven voor aandoeningen van gehoor, zenuwisolatie en zelfs de verspreiding van kanker.
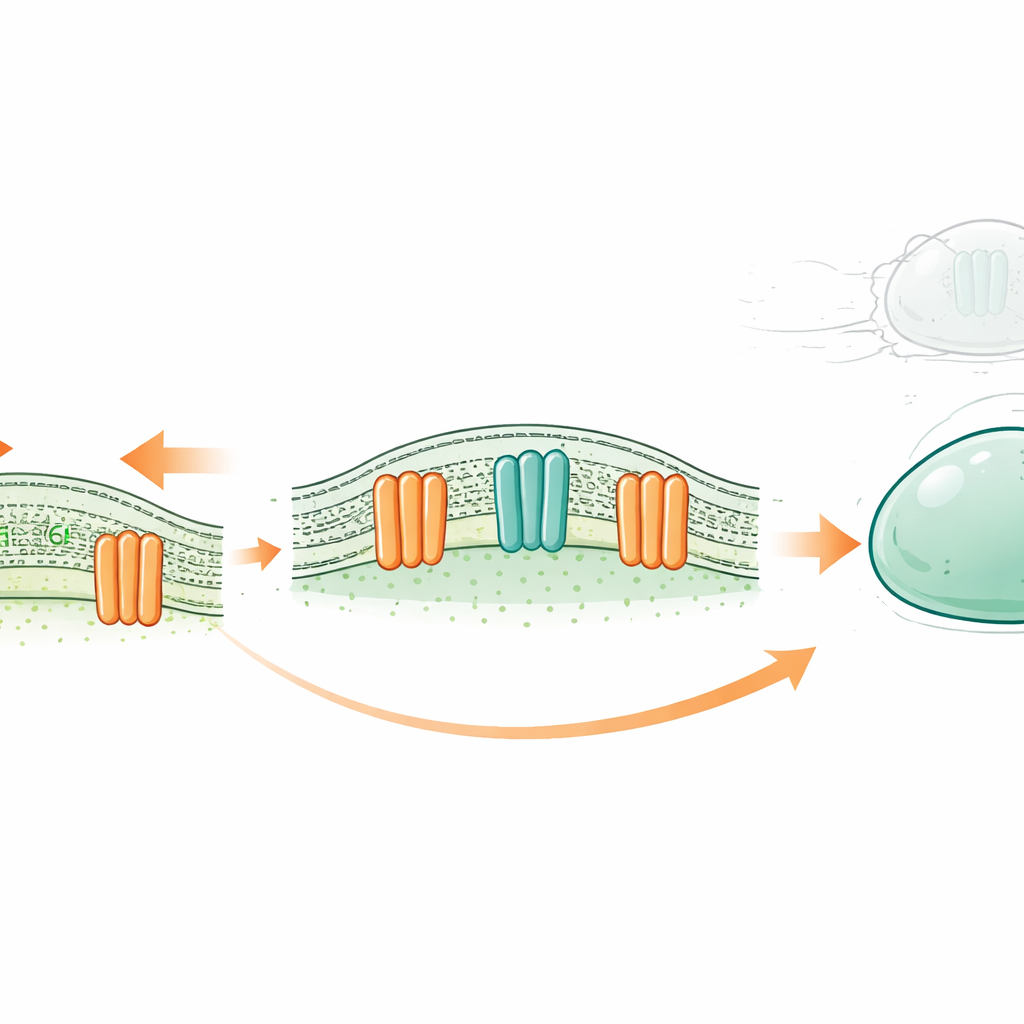
Een nieuw soort cellulaire schokdemper
Elke cel is omhuld door een dun, olieachtig membraan dat uit twee lagen vetachtige moleculen — lipiden — bestaat. Traditioneel werd aangenomen dat bepaalde membraaneiwitten alleen optreden als ionkanalen: kleine kleppen die geladen deeltjes doorlaten als reactie op prikkels zoals rek. De OSCA/TMEM63‑familie, aanwezig van planten tot mensen, staat bekend om te openen bij membraanspanning. Eerder structureel werk suggereerde dat, in tegenstelling tot klassieke ionkanalen, hun poriën deels door lipiden worden bekleed. Dat riep een prikkelende mogelijkheid op: zouden deze kanalen ook kunnen fungeren als ‘scramblasenzijn’, waarbij lipiden tussen de binnen- en buitenlaag van het membraan worden omgedraaid wanneer de cel onder kracht staat?
Het zien van lipiden die door het membraan flippen
Om deze gedachte te toetsen combineerden de auteurs computersimulaties met reductionistische labsystemen gebouwd uit gezuiverde componenten. In simulaties werden open versies van verschillende OSCA‑ en TMEM63‑eiwitten ingebed in modelmembranen. Lipidemoleculen bewogen spontaan door een groef in deze eiwitten van de ene kant van de dubbellaag naar de andere, en vormden een gordel die de twee bladen verbond terwijl er een met water gevulde weg voor ionen overbleef. In parallelle experimenten bouwde het team reusachtige kunstmatige ‘belletjes’ (vesikels) met fluorescerende lipiden en specifieke eiwitten. Wanneer een extern middel de fluorescentie aan de buitenkant doofde, kon elke verdere daling van het signaal alleen worden verklaard door lipiden die van de binnenlaag naar buiten flipten. Vesikels met OSCA1.1, OSCA1.2, OSCA2.2 of TMEM63A/B lieten dit extra verlies van fluorescentie zien, wat wijst op actieve scrambling, terwijl controlekanalen die lipiden niet scramblen dat niet lieten zien.
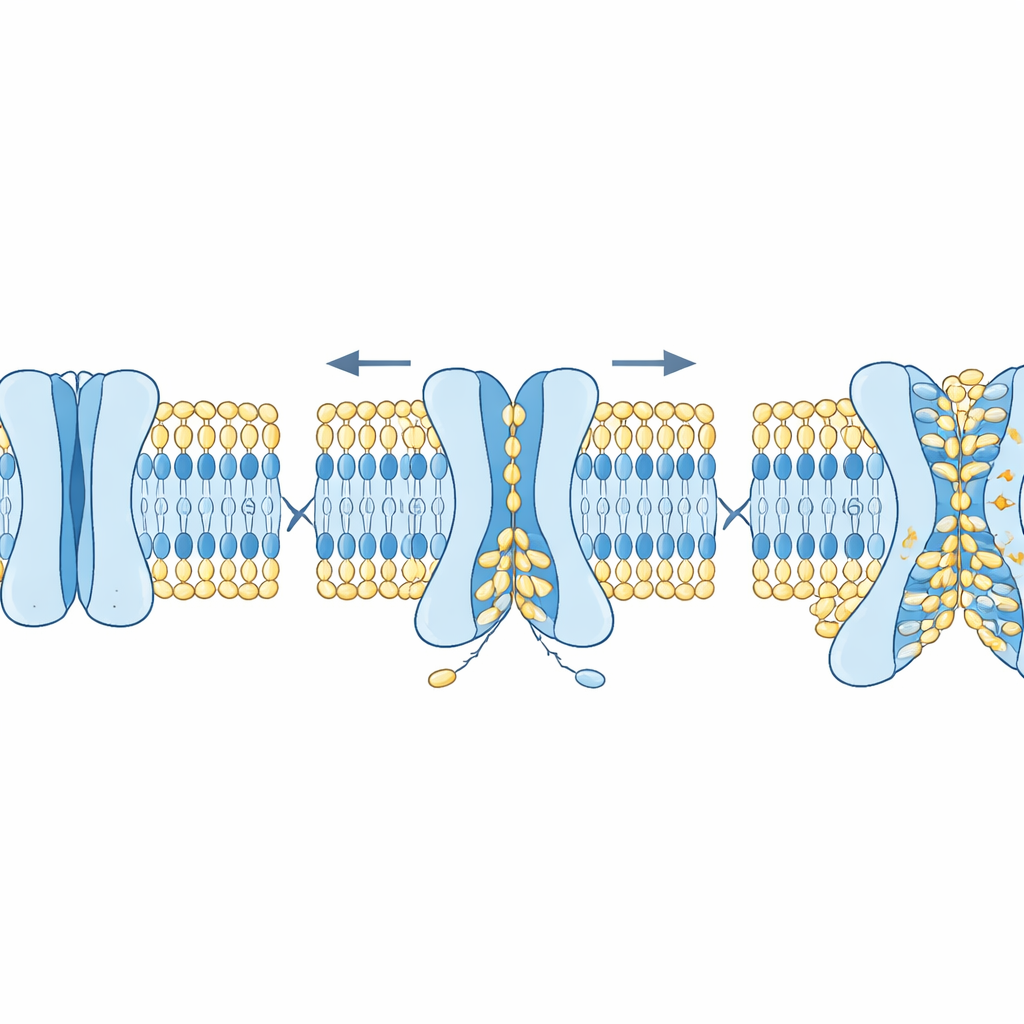
Hoe structuur en cholesterol het proces afstemmen
De onderzoekers vroegen vervolgens welke eigenschappen van TMEM63‑eiwitten dit dubbele gedrag beheersen. Met AlphaFold2 genereerden ze vele plausibele vormen van menselijke TMEM63‑eiwitten, van gesloten tot steeds opener. Simulaties toonden dat een handvol omvangrijke aminozuren als ‘knelpunten’ in de groef fungeert. Eén residu beperkt vooral de ionenstroom, terwijl andere de lipidebeweging blokkeren. Het muteren van het ionenkneepunt verhoogde de elektrische geleiding zonder de lipidescrambling veel te veranderen, terwijl het muteren van het lipidehek ertoe leidde dat lipiden makkelijker flipten en zelfs dat cellen ‘eet mij’-signalen op hun oppervlak toonden zonder extra stimulus. Een andere belangrijke regulator was cholesterol, een verstevigend bestanddeel van celmembranen. Het toevoegen van cholesterol aan modelmembranen vertraagde de lipidescrambling aanzienlijk en stabiliseerde de gesloten toestand van TMEM63A, zowel in simulaties als in cryo‑elektronenmicroscopie‑structuren waar cholesterol in specifieke bindingplaatsen van het eiwit paste.
Mechanische kracht als de aan‑schakelaar
Als cholesterol normaal gesproken scrambling binnen cellen onder controle houdt, wat zet het dan op het juiste moment aan? Het team gebruikte ringvormige suikermoleculen die cyclodextrinen heten om selectief lipiden uit membranen te trekken en zo de spanning te verhogen zonder cholesterol te verwijderen. In vesikels ter grootte van cellen activeerde toevoeging van cyclodextrine lipidescrambling door TMEM63A alleen wanneer het eiwit aanwezig was, wat bewijst dat mechanische spanning op zichzelf het flippen kan triggeren. Vergelijkbare benaderingen in levende cellen lieten zien dat milde cholesterolverwijdering op zichzelf niet genoeg was; een daaropvolgende mechanische uitdaging was nodig om sterke scrambling te zien. Wanneer cellen die waren aangepast om TMEM63A te produceren herhaaldelijk werden uitgerekt, maakten ze snel bepaalde lipiden aan hun buitenkant zichtbaar — een kenmerk van scrambling — terwijl cellen zonder deze eiwitten veel minder veranderden.
Cellen beschermen tegen scheuren
Naast het flippen van lipiden veranderde mechanisch geactiveerde scrambling het fysieke gedrag van membranen onder extreme belasting. In kunstmatige vesikels die aan hoge krachten werden blootgesteld, barstten die zonder scramblasenzijn vaak, terwijl vesikels met TMEM63A of een bekend scramblase krompen, dunne buisjes vormden en grotendeels intact bleven. In een menselijke hersenkanker-celijn die van nature TMEM63A en TMEM63B tot expressie brengt, maakte het verlagen van de niveaus van een van beide eiwitten cellen gevoeliger voor ruptuur bij sterke mechanische stress. Samen ondersteunen deze bevindingen een model waarin OSCA/TMEM63‑eiwitten fungeren als kleppen die bij spanning opengaan en tijdelijk het gebruikelijke verschil tussen de binnen‑ en buitenzijde van het membraan vervagen. Door lipiden snel te laten herverdelen helpen ze de spanning te egaliseren en katastrofale scheuring te voorkomen.
Wat dit betekent voor gezondheid en ziekte
In eenvoudige bewoordingen toont dit werk aan dat sommige rekgevoelige kanalen meer doen dan elektrische signalen geleiden: ze reorganiseren ook de buitenste huid van de cel om die te helpen overleven als hij wordt samengedrukt. TMEM63‑eiwitten komen naar voren als mechanisch geactiveerde lipide‑scramblasenzijn waarvan de activiteit fijn wordt afgestemd op de membraansamenstelling, met name cholesterol. Dit mechanisme van mechanische veerkracht kan belangrijk zijn waar cellen grote krachten ondervinden, van geïsoleerde zenuwvezels en geluidssensorische cellen in het oor tot kankercellen die zich door dicht weefsel bewegen. Het begrijpen en uiteindelijk manipuleren van deze dubbele ionkanaal–scramblasefunctie zou nieuwe wegen kunnen openen om kwetsbare weefsels te beschermen — of om moeilijk te doden kankercellen juist fragieler te maken.
Bronvermelding: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Trefwoorden: mechanogevoelige ionkanalen, lipidescrambling, celmembraanmechanica, cholesterolregulatie, TMEM63 OSCA-eiwitten