Clear Sky Science · nl
Een neurotoxisch cryptisch peptide voortkomend uit TDP-43-afhankelijke cryptische splicing van PKN1
Verborgen bedreigingen binnen hersencellen
Veel hersenziektes, waaronder amyotrofische laterale sclerose (ALS) en de ziekte van Alzheimer, gaan gepaard met ophopingen van een eiwit genaamd TDP-43. Wetenschappers weten dat wanneer dit eiwit niet goed functioneert, neuronen essentiële boodschappen verliezen en uiteindelijk afsterven. Deze studie onthult een verrassende wending: falen van TDP-43 kan er ook toe leiden dat hersencellen een eerder onbekend, toxisch mini-eiwit aanmaken, dat op zijn beurt geheugencircuits beschadigt. Inzicht in deze verborgen speler kan nieuwe wegen openen voor diagnose en behandeling van slopende vormen van dementie.
Hoe een cellulaire proeflezer RNA op orde houdt
In neuronen fungeert TDP-43 als een proeflezer voor RNA, de tussentijdse boodschappen tussen DNA en eiwitten. Het bindt aan specifieke korte sequenties en blokkeert de invoeging van dwalende "extra stukjes" in deze boodschappen. Wanneer TDP-43 verloren gaat of verkeerd gelokaliseerd raakt, zoals bij ALS en veel Alzheimer‑gevallen, kunnen deze extra stukjes—cryptische exons genoemd—insluipen in RNA. Tot nu toe veroorzaakten de meeste bekende cryptische exons gewoonlijk een verlies van normaal eiwit doordat het bericht instabiel werd en snel werd afgebroken. Of zulke gebeurtenissen ook nieuwe, schadelijke eiwitten konden genereren, was onduidelijk.
Een cryptische splice creëert een toxisch fragment
De auteurs richtten zich op een gen genaamd PKN1, dat helpt de interne structuur en signaalstroom van neuronen te behouden. Met celmodellen waarin TDP-43 was gereduceerd, ontdekten ze een eerder ongekend cryptisch exon, doopte het PKN1‑5a1, ingevoegd tussen twee normale segmenten van het PKN1-RNA. Deze insertie introduceert een vroeg stopsein, waardoor een verkort RNA ontstaat. Opmerkelijk genoeg ontsnapt een deel van dit foutieve bericht aan het kwaliteitscontrolesysteem van de cel en wordt vertaald tot een stabiel fragment van het PKN1-eiwit dat slechts de eerste 207 aminozuren bevat. Het team noemde dit verkorte product PKN207. Ze toonden aan dat TDP-43 dit foutje normaal voorkomt door te binden aan meerdere UG-rijke regio’s die het cryptische exon omringen; wanneer die binding verloren gaat, wordt het exon ingebouwd en wordt PKN207 geproduceerd.
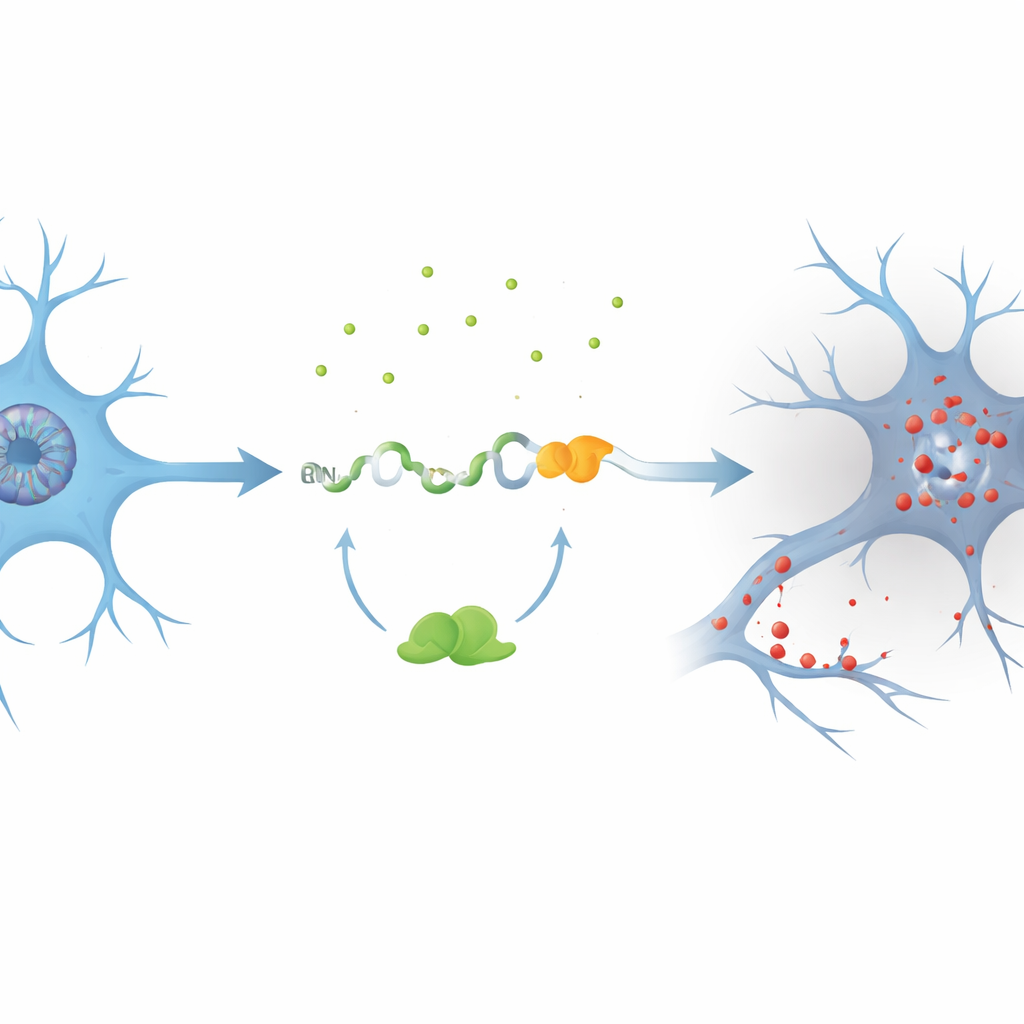
Bewijs uit patiëntenhersenen en grote datasets
Om te onderzoeken of dit fenomeen in menselijke ziekte voorkomt, doorzochten de onderzoekers RNA-sequencinggegevens van honderden ALS‑hersenen en ruggenmergmonsters. Ze vonden wijdverspreide activatie van het PKN1‑5a1 cryptische exon in regio’s die bekend zijn als getroffen door TDP-43-pathologie, zoals de motorische cortex en het ruggenmerg, maar niet in het relatief gespaarde cerebellum. Vervolgens ontwikkelden ze zeer specifieke antilichamen die alleen de unieke staart van PKN207 herkennen, niet het volledige PKN1-eiwit. In hippocampusweefsel van Alzheimerpatiënten die ook abnormale, gefosforyleerde TDP-43 vertoonden, detecteerden deze antilichamen een duidelijke band die overeenkomt met PKN207, terwijl zo’n band afwezig was in controlemateriaal. Extra Alzheimer‑datasets bevestigden dat het cryptische exon al in vroege ziektefasen wordt aangezet, wat suggereert dat deze moleculaire fout lang voordat symptomen duidelijk worden kan beginnen.
Een mini-eiwit met grote impact op geheugen
Het vinden van PKN207 in zieke menselijke hersenen riep de cruciale vraag op: is het schadelijk? Om dit te testen gebruikten de onderzoekers virussen om de productie van ofwel normaal PKN1 ofwel PKN207 specifiek in de hippocampus—een hersengebied dat essentieel is voor geheugen—van jonge muizen aan te jagen. Maanden later toonden beide groepen muizen een verslechterd leervermogen in de Morris watermaze: ze zwommen langer om een verborgen platform te vinden. Hun hersenvocht bevatte hogere niveaus van een structureel eiwit, neurofilament light chain, een merker voor axonaal letsel. In gekweekte neuronen leidde verhoogde expressie van PKN207 tot celschade, gemeten door lekkage van een enzym dat membraanschade signaleert. Gedetailleerde eiwitprofilering van de hippocampus onthulde brede veranderingen in paden die verband houden met synaptische sterkte (long‑term potentiation) en bekende neurodegeneratieve ziekten, met bijzonder sterke verstoring van moleculen die efficiënt signaaltransport en een gezonde zenuwvezel‑scaffold ondersteunen.
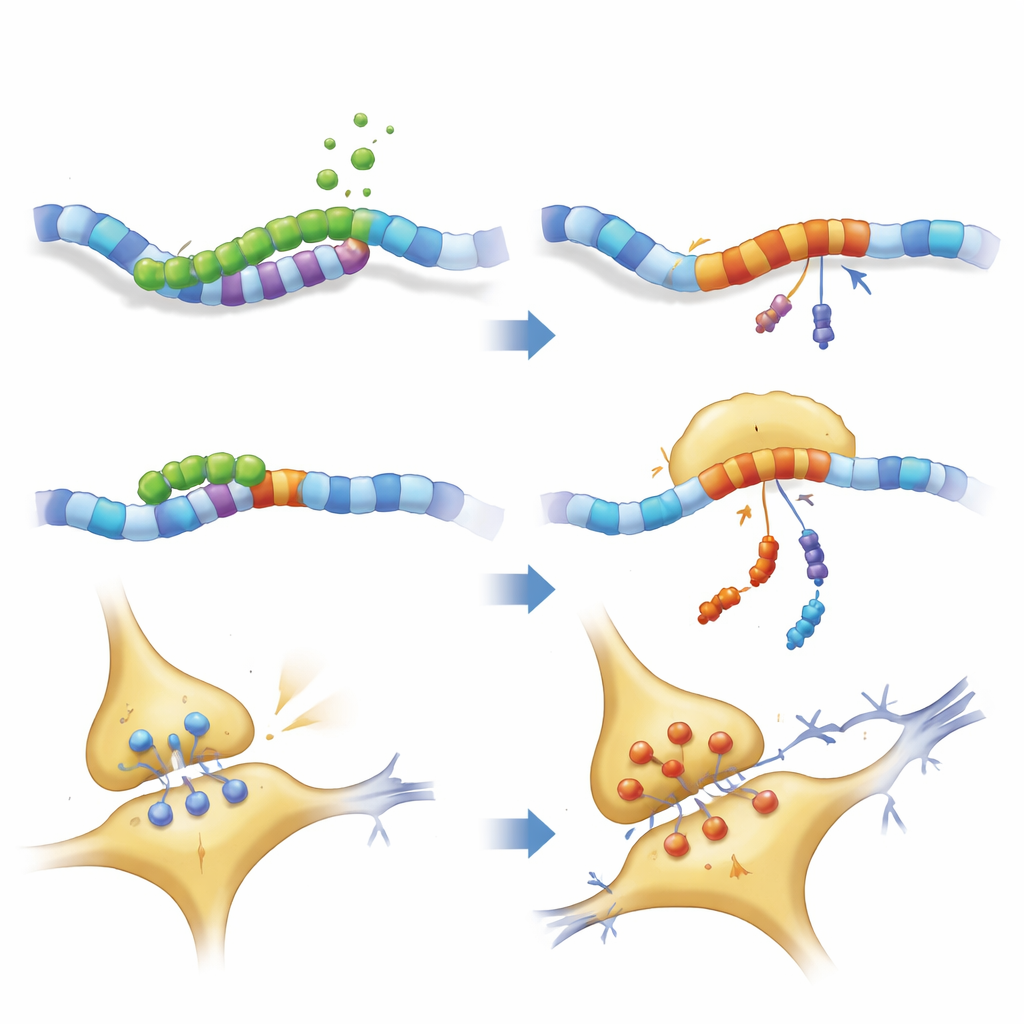
Hoe het fragment de hersenbedrading verstoort
Nadere inspectie van de neuronale structuur toonde dat zowel het volledige PKN1 als PKN207 het neurofilamentnetwerk verstoorden dat axonen hun vorm geeft en helpt bij transport van lading. Belangrijke motor- en scaffold-eiwitten waren verminderd, terwijl sommige neurofilamentelementen zich ophoopten, wat wijst op verkeersopstoppingen en mogelijke aggregatie. Elektrische opnamen van hippocampale plakjes bevestigden dat muizen die PKN207 tot expressie brachten verzwakte long‑term potentiation hadden—het proces waarbij synapsen sterker worden na herhaalde activiteit en een breed geaccepteerde cellulaire basis voor leren en geheugen. Hoewel PKN207 het enzymdomein van PKN1 mist, was de aanwezigheid ervan voldoende om de verstorende effecten van het volledige eiwit te imiteren en soms te overtreffen, wat impliceert dat de gedeelde N‑terminus op zichzelf de neuronale homeostase kan verstoren.
Waarom deze ontdekking van belang is voor hersenziekten
Dit werk voegt een nieuwe laag toe aan ons begrip van aan TDP-43 gerelateerde aandoeningen. In plaats van alleen maar te leiden tot verlies van essentiële RNA’s, kan falen van TDP-43 ook een stabiel, toxisch micro-eiwit voortbrengen dat synapsen en cognitie ondermijnt. Het cryptische PKN1‑5a1 exon en zijn peptideproduct PKN207 komen nu naar voren als potentiële biomarkers van vroege TDP-43-dysfunctie en als kandidaatdoelen voor therapieën die splicing corrigeren of het schadelijke fragment blokkeren. Breder gezien suggereert de studie dat andere verborgen exons mogelijk op vergelijkbare wijze ziekte‑veroorzakende peptiden voortbrengen, wat onderzoekers wijst op een rijke—en eerder over het hoofd geziene—landkaart van moleculaire daders in neurodegeneratie.
Bronvermelding: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Trefwoorden: TDP-43, cryptische splicing, PKN1, neurodegeneratie, Alzheimer en ALS