Clear Sky Science · nl
FOX-eiwitten tegenwerken regelen epigenetisch de lytisch‑latente balans van het herpesvirus
Waarom verborgen herpesvirussen ertoe doen
Veel mensen dragen levenslang herpes simplex‑virussen bij zich, vaak zonder het te weten. Deze virussen kunnen jarenlang stil zitten in zenuwcellen en vervolgens plotseling opspelen, wat koortsblaasjes, oogziekten of ernstigere problemen bij mensen met een verzwakt immuunsysteem kan veroorzaken. Wat het virus meestal laat slapen en wat het weer activeert, is lange tijd een mysterie geweest. Deze studie onthult een sleutelonderdeel van dat regelsysteem: een touwtrekkerij tussen twee tegengestelde groepen menselijke eiwitten die viraal DNA herschikken en bepalen of herpes stil blijft of nieuwe virussen gaat produceren.
Twee cellulaire teams die in tegengestelde richting trekken
De auteurs richtten zich op een grote familie van menselijk DNA‑bindende eiwitten, de FOX‑eiwitten, die normaal onze eigen genen helpen reguleren tijdens ontwikkeling en stofwisseling. Door veel FOX‑familieleden te testen in zenuwachtige cellen, ontdekten ze twee duidelijke kampen. De ene groep (inclusief eiwitten zoals FOXF1) versterkte sterk de replicatie van herpes simplex‑virus type 1 (HSV‑1) en verschillende verwante “alfa”‑herpesvirussen. Een andere groep (FOXK1 en FOXK2) deed het tegenovergestelde en onderdrukte viraalgroei krachtig. Deze balans was niet in elk celtype hetzelfde: niet‑neurale cellen en gestreste neuronen produceerden vaker meer van de activerende FOX‑eiwitten, terwijl rustende sensorische neuronen zeer weinig van die activerende eiwitten maakten maar juist hoge niveaus van de repressieve FOXK‑eiwitten hadden.
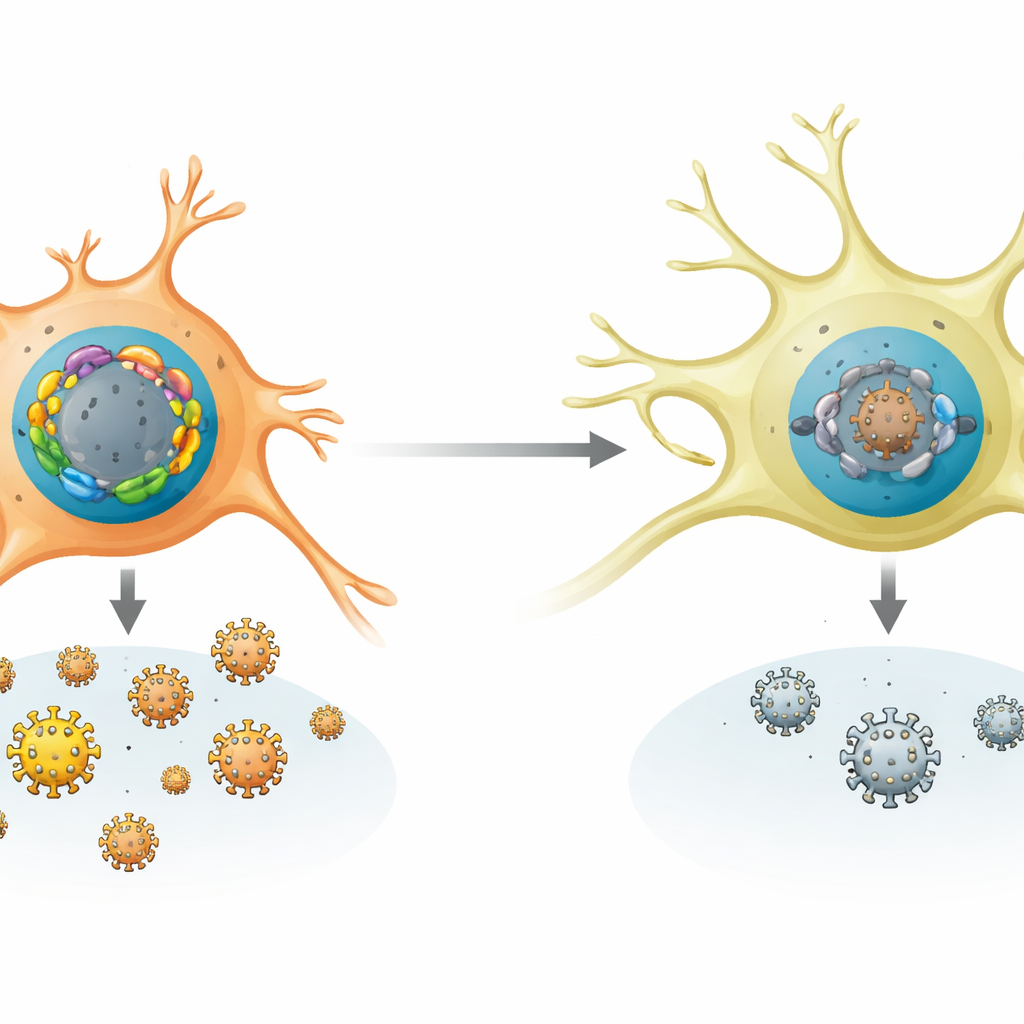
Hoe zenuwcellen de stille toestand bevoordelen
Het team vergeleek FOX‑genactiviteit in vele menselijke en muiscellen en in geïnfecteerde dieren. Sensorische neuronen, de natuurlijke verblijfplaats voor latente HSV‑1, vertoonden een patroon dat stilte bevordert: sterke expressie van FOXK1 en FOXK2 en zwakke expressie van de meeste activerende FOX‑genen. Bij muizen verhoogden vroege infectie en latere stresssignalen zoals hitte of weefselschade selectief de niveaus van meerdere activerende Fox‑genen zonder de repressieve exemplaren te verlagen. In gekweekte muisneuronen en in levende muizen maakte het verwijderen of onderdrukken van FOXK‑eiwitten het voor HSV‑1 gemakkelijker om te repliceren en uit latentietoestand te heractiveren. Omgekeerd was het forceren van neuronen om extra activerende FOX‑eiwitten te produceren al voldoende om reactivatie te veroorzaken, zelfs zonder chemische triggers, wat laat zien hoe gevoelig de virale toestand is voor deze FOX‑balans.
Viraal DNA vastgrijpen en open- of dichtmaken
Om het onderliggende mechanisme te begrijpen, brachten de onderzoekers in kaart waar FOX‑eiwitten op het virale genoom zitten. Ze ontdekten dat zowel de activerende FOXF1 als de repressieve FOXK1 zich wijd verspreid aan HSV‑1‑DNA binden, niet alleen aan een paar specifieke sequentiemotieven. Deze binding berust op een geconserveerd deel van de FOX‑eiwitten dat de DNA‑backbone vastgrijpt in plaats van individuele letters, waardoor ze zich bijna overal kunnen hechten. Eenmaal geplaatst rekruteren de twee eiwitkampen verschillende moleculaire partners die chromatine, de combinatie van DNA en zijn verpakkingsproteïnen, herstructureren. Activerende FOX‑eiwitten, vooral FOXF1, associëren met CBP en P300, enzymen die acetylgroepen aan histonen toevoegen en chromatine losser maken. Dit maakt viraal DNA toegankelijker en verhoogt vroege, tussenliggende en late virale genactiviteit. FOXK1 werkt daarentegen samen met factoren zoals SIN3A en MAX die gekoppeld zijn aan histondeacetylatie en genrepressie, waardoor viraal chromatine strakker wordt en genen uitgeschakeld blijven.
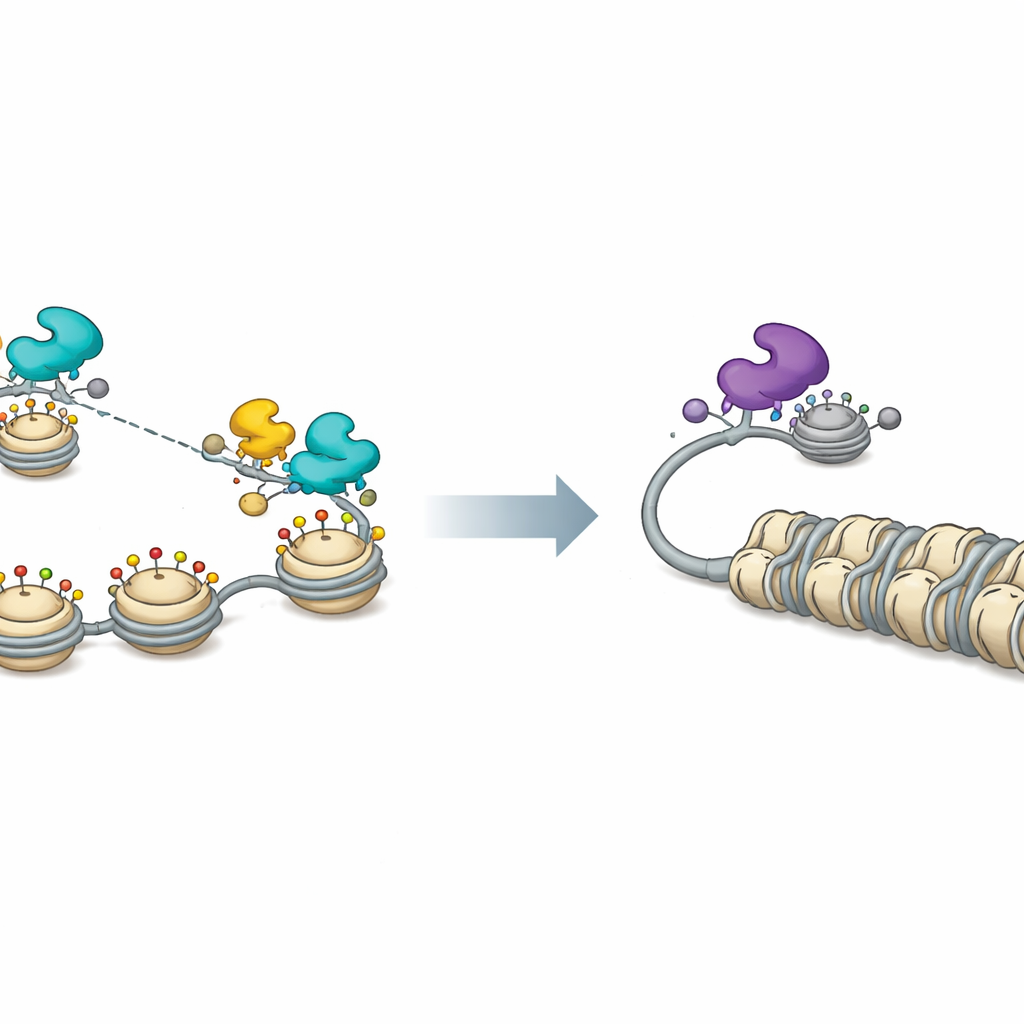
Een chromatineschakelaar voor virale slaap en wakkerheid
Meting van viraal chromatine bevestigde dit beeld. Wanneer FOXF1 aanwezig was, werden histonen op viraal DNA verwijderd of chemisch gemarkeerd op manieren die geassocieerd zijn met open, actief chromatine, en nam de algemene toegankelijkheid van virale promoterregio’s op het genoom toe. FOXF1‑expressie verspreidde ook kleine kernstructuren genaamd PML‑kernlichamen die normaal helpen viraal DNA te onderdrukken. Het blokkeren van CBP en P300 wist veel van deze activerende effecten uit en verminderde FOXF1‑gedreven virale genexpressie. Aan de repressieve kant toonden de onderzoekers aan dat FOXK1‑geassocieerde partners en histondeacetylase‑activiteit belangrijk waren om HSV‑1‑replicatie laag te houden; chemische remming van deacetylases verhoogde zowel virusproductie als verzwakte FOXK1‑gemedieerde onderdrukking.
Wat dit betekent voor het beheersen van levenslange infectie
Gezamenlijk suggereren de resultaten dat het antwoord op de vraag of HSV‑1 actief of sluimerend is sterk afhangt van de samenstelling van FOX‑eiwitten in de gastneuronen. Rustende sensorische neuronen bevoordelen van nature de repressieve, door FOXK gedomineerde staat, waardoor het virus in een diep stille, chromatine‑gecompacteerde vorm wordt geduwd. Stress of andere omstandigheden die activerende FOX‑eiwitten verhogen kunnen deze balans kantelen, viraal chromatine openen en de lytische cyclus weer laten starten. Door deze epigenetische touwtrekkerij bloot te leggen, benadrukt de studie nieuwe benaderingen waarmee wetenschappers mogelijk ooit herpesvirussen steviger in onschadelijke latentietoestand kunnen duwen of, alternatief, ze onder gecontroleerde omstandigheden uit hun schuilplaats kunnen forceren zodat ze kunnen worden geëlimineerd.
Bronvermelding: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Trefwoorden: latentie van herpes simplex‑virus, FOX transcriptiefactoren, viraal chromatine, epigenetische regulatie, virale reactivatie