Clear Sky Science · nl
Het uitbreiden van het DNA‑beschadigende potentieel van kunstmatige metallo‑nucleasen met click‑chemie
Slimmere moleculaire scharen bouwen
Chemotherapie werkt vaak door het DNA van kankercellen te beschadigen, maar de huidige middelen zijn soms grove instrumenten die ook gezond weefsel schaden. Deze studie onderzoekt een nieuwe klasse van hoogst programmeerbare “moleculaire scharen” gemaakt van koper en kleine organische onderdelen die met click‑chemie aan elkaar geklikt worden. Door hun vorm en de manier waarop ze aan DNA vastgrijpen te verfijnen, streven de onderzoekers ernaar middelen te creëren die genetisch materiaal preciezer doorsnijden, wat paden opent naar toekomstige antikanker‑ en antibacteriële behandelingen.
Een driearmige snijder in elkaar klikken
Het team gebruikt kopergecatlyseerde click‑chemie, een met een Nobelprijs bekroonde methode bekend om haar betrouwbaarheid, om een familie moleculen samen te stellen die Tri‑Click (TC) liganden worden genoemd. Elk TC‑molecuul is een driearmig knooppunt dat drie koperionen tegelijk kan binden en zo een compact cluster vormt dat DNA kan aanvallen. Door verschillende chemische “donor”groepen aan het uiteinde van elke arm te verwisselen—gebaseerd op stikstof, zuurstof of zwavel—testten de wetenschappers systematisch hoe subtiele structurele veranderingen koperbinding, DNA‑herkenning en biologische activiteit beïnvloeden. Van de verschillende nieuwe ontwerpen vielen versies met platte, ringvormige stikstofdonoren op als bijzonder veelbelovend voor sterk DNA‑grip.
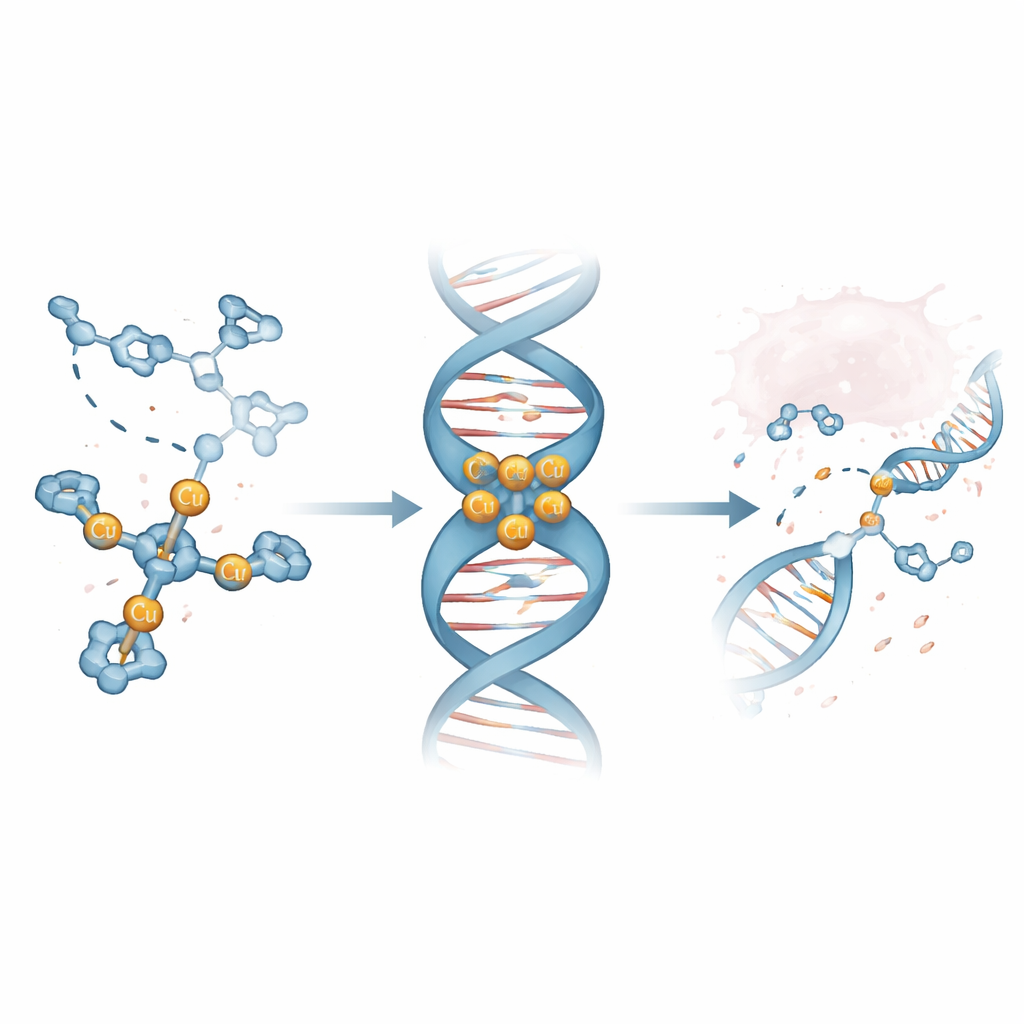
Het leidende molecuul dat van DNA‑groeven houdt vinden
Met massaspectrometrie en optische methoden toonden de onderzoekers aan dat één complex, Cu3‑TC‑Py genoemd, betrouwbaar een driekopercluster vormt dat stabiel is in oplossing. Competitie‑experimenten met fluorescente kleurstoffen gebonden aan kalfs‑thymus‑DNA lieten zien dat Cu3‑TC‑Py deze kleurstoffen bij zeer lage concentraties verdringt, wat wijst op sterke DNA‑binding. Vervolgtesten op korte, haarspeldvormige DNA‑stukjes toonden dat dit complex de voorkeur heeft om in de minor groove te nestelen—de smallere groeve die rond de DNA‑dubbelhelix loopt—en dat het vooral voorkeur heeft voor reeksen rijk aan G‑ en C‑basenparen. High‑resolution computermodellen ondersteunden dit beeld en toonden het driearmige complex in de groeve, met zijn positieve ladingen die het negatief geladen DNA omklemmen en de helix subtiel samenpersen.
Van strakke binding naar DNA‑instorting en breuk
Op enkelmolecuulniveau volgde het team lange DNA‑strengen die opgesloten zaten in nanoformaten kanalen terwijl ze interageerden met Cu3‑TC‑Py. Bij lage doses concurreerde het complex met een uitrekkende kleurstof en verdrong deze terwijl het in de groeven bond. Bij hogere doses begon het DNA te krimpen en condenseerde het uiteindelijk volledig, wat overeenkomt met sterke elektrostatische aantrekking tussen het kopercluster en het DNA‑backskelet. Toen plasmide‑DNA aan het complex werd blootgesteld in aanwezigheid van een reductor, veranderden de strengen van hun inheemse gekronkelde vorm naar gerelaxeerde en vervolgens volledig lineaire vormen, een patroon dat duidt op zowel enkelstrengs als dubbelstrengs breuken. Verdere testen met radicalevangers betrokken kortlevende zuurstofsoorten—zoals superoxide, singlet zuurstof en hydroxylradicalen—als de werkelijke snijgereedschappen die nabij het gebonden complex werden gegenereerd.
DNA aanvallen in kanker‑ en bacteriecellen
Voorbij gezuiverd DNA onderzochten de onderzoekers hoe Cu3‑TC‑Py zich gedraagt binnen levende cellen. In panelen van kankercellen vertoonden de vrije liganden met stikstofrijke aromatische groepen veel sterkere remming van celgroei dan eerdere ontwerpen, en het volledig gevormde kopercomplex was nog krachtiger, waarbij het meerdere kankecellijnen in micromolaire concentraties deed afsterven. Metingen van intracellulair koper toonden aan dat Cu3‑TC‑Py koper efficiënt in cellen brengt en een ophoping van beschadigd DNA veroorzaakt, gedetecteerd met een reparatie‑geassisteerde beeldvormingstechniek die letsels langs uitgerekte genomische strengen markeert. In bacteriën liet microscopie zien dat behandeling snel het compacte bacteriële chromosoom verstoorde, het DNA door de cel verspreidde en de ernstige fragmentatie nabootste die wordt gezien bij een sterk DNA‑beschadigend antibioticum, consistent met wijdverspreide genetische destructie.
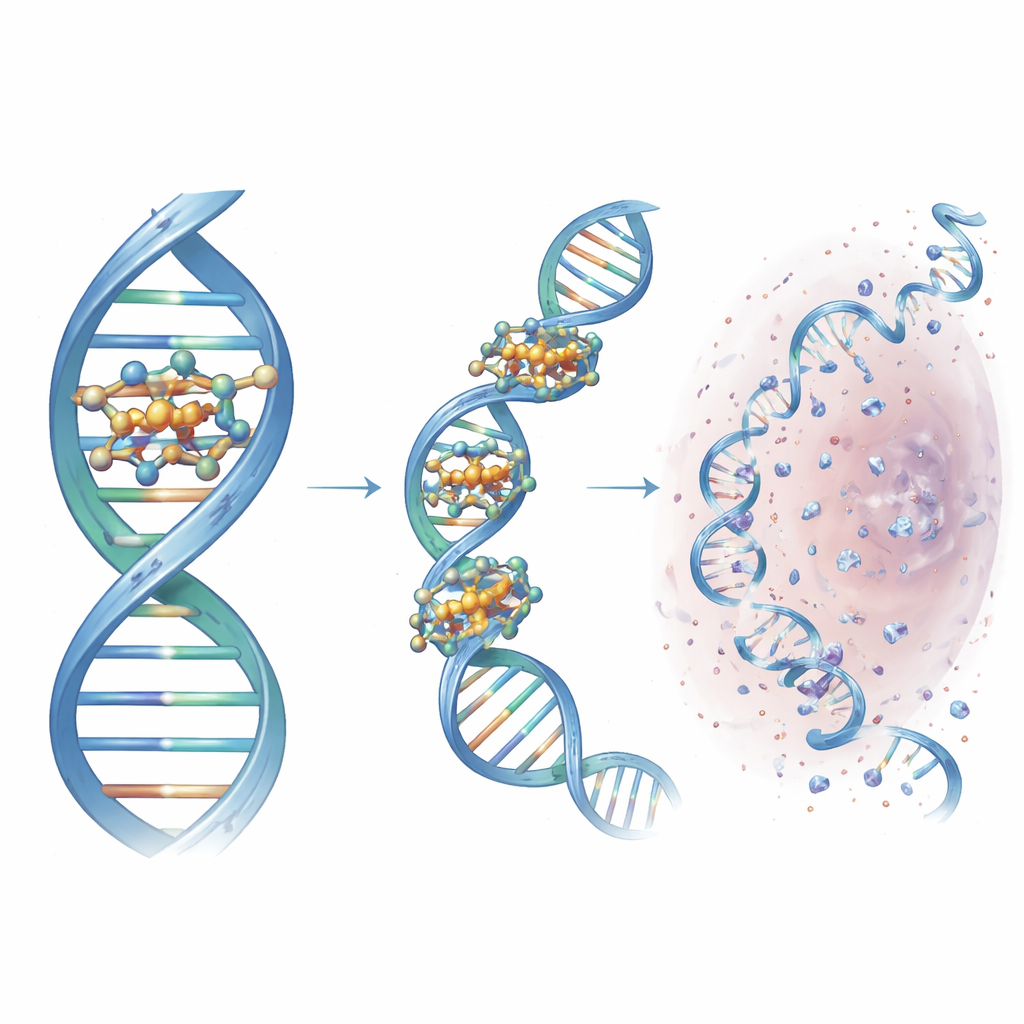
Waarom deze ontwerperscharen ertoe doen
Voor de niet‑specialist is de kernboodschap dat de onderzoekers een eenvoudig, modulair click‑chemie‑skelet hebben omgevormd tot een fijn afgestemde DNA‑snijmachine. Door de juiste ringvormige stikstofgroepen te kiezen, creëerden ze een compact kopercluster dat in een specifieke groeve van DNA dockt, de strengen naar elkaar toe trekt en lokaal reactieve zuurstofsoorten genereert die de dubbelhelix doorsnijden. Deze leidende verbinding, Cu3‑TC‑Py, beschadigt DNA efficiënt in zowel kankercellen als bacteriën en laat zien hoe rationeel ontwerp de werking van metaalgebaseerde medicijnen kan verscherpen. Hoewel er nog veel werk nodig is voor klinisch gebruik, schetst de studie ontwerprichtlijnen voor volgende‑generatie moleculaire scharen die op een dag meer gerichte kankertherapieën en nieuwe antimicrobiële strategieën kunnen bieden.
Bronvermelding: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Trefwoorden: click‑chemie, DNA‑schade, kopercomplexen, antikanker middelen, kunstmatige nucleasen