Clear Sky Science · nl
Evolutionaire herbestemming van een metabool thiolasecomplex maakt antibiotica-biosynthese mogelijk
Hoe alledaagse microben hun chemie opnieuw uitvinden
Veel van de antibiotica en geneesmiddelen waarop we vertrouwen, worden stilletjes geproduceerd door bacteriën. Deze kleine chemici gebruiken enzymen — moleculaire machines — om complexe verdedigingsverbindingen op te bouwen. Deze studie onthult hoe een kernmetabool enzymcomplex, oorspronkelijk bedoeld voor basale celhuishouding, evolutionair is omgebouwd in orale bacteriën om een krachtig antibioticum te maken. Begrijpen hoe deze transformatie plaatsvond, toont niet alleen hoe de natuur nieuwe chemie uitvindt, maar biedt ook aanwijzingen voor het ontwerpen van volgende-generatie geneesmiddelen en biokatalysatoren.
Van basaal metabolisme naar chemisch wapen
Alle levende cellen zijn afhankelijk van een set geconserveerde enzymen die hun centrale stofwisseling regelen, zoals het afbreken van vetten en het opbouwen van essentiële moleculen. Eén dergelijke groep, de thiolase-superfamilie genoemd, helpt normaal gesproken bij het verwerken van kleine energierijke moleculen zoals acetyl-CoA en ondersteunt vitale routes voor de synthese van lipiden en andere celcomponenten. De auteurs ontdekten dat in meerdere orale Streptococcus-soorten een driedelig thiolase-gebaseerd complex — bestaande uit eiwitten verwant aan HMGS, ACAT en een derde hulp-eiwit — zijn oorspronkelijke metabole rol heeft losgelaten. In plaats daarvan voltooit dit complex nu de biosynthese van een antibioticum genaamd reutericycline A, dat deze bacteriën helpt concurreren in de drukke omgeving van de mond.
Een nieuw type enzymreactie op een antibioticumscaffold
Door het Streptococcus-complex in het laboratorium te herconstituteren en het een chemisch gesynthetiseerde voorloper van reutericycline A te voeren, lieten de onderzoekers zien dat het complex een ongebruikelijke koolstof–koolstof- bindingsvormende reactie uitvoert die bekendstaat als Friedel–Crafts C-acylatie. In plaats van een acetylgroep aan zuurstof te hechten, zoals veel enzymen doen, plaatst het deze groep rechtstreeks op een koolstofatoom van een pyrrolidine-2,4-dionring — een belangrijk onderdeel van het reutericycline-scaffold. Het complex accepteert zowel natuurlijke acetyl-donoren zoals acetyl-CoA als verschillende kunstmatige donoren, en kan de reactie zelfs in omgekeerde richting uitvoeren door de gecreëerde binding te verbreken. Deze flexibiliteit breidt het bekende repertoire van biologische acyltransferasen uit en suggereert hoe zulke enzymen zouden kunnen worden aangepast om diverse chemische producten te bouwen.
Het herbestemmen van een geconserveerd eiwitskelet
Met behulp van cryo-elektronenmicroscopie met hoge resolutie bepaalde het team de driedimensionale structuur van het Streptococcus-complex, aangeduid als SmaATase. Ondanks zijn nieuwe functie behoudt SmaATase een opvallende architectonische gelijkenis met een verwant complex in archaea dat participeert in de mevalonaatroute voor de opbouw van isoprenoïde lipiden. Beide zijn grote multimerische assen opgebouwd uit herhalende modules en beschikken over een gedeelde holte waar de cofactor CoA kan binden en tussen actieve plekken kan bewegen. Echter, sleutelresiduen die essentieel zijn voor de oorspronkelijke metabole reactie ontbreken of zijn veranderd in de bacteriële variant. Biochemische tests bevestigen dat SmaATase het voorouderlijke product HMG-CoA niet langer kan maken en in plaats daarvan acetyl-CoA uitsluitend gebruikt als donor voor zijn nieuwe kleine-molecuulsubstraten.
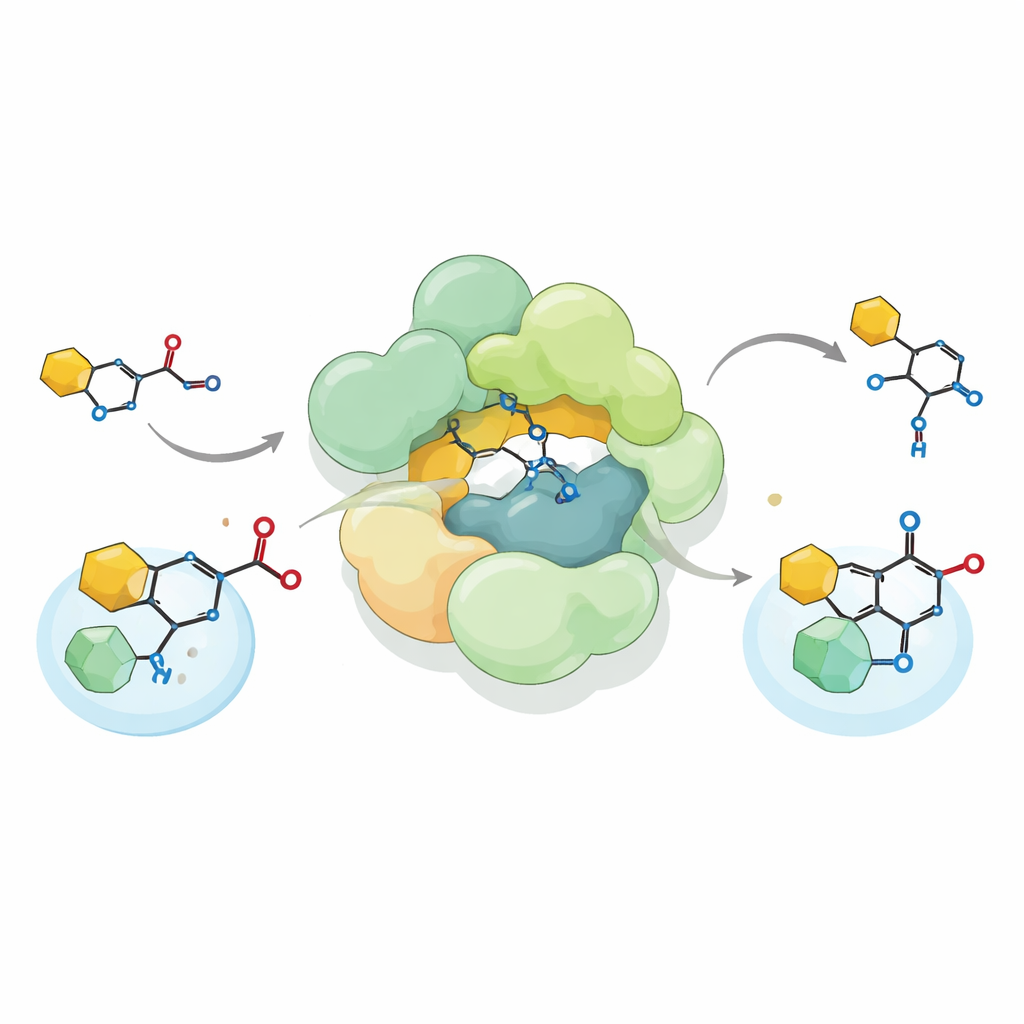
Een evolutionair spoor van metabolisme naar antibiotica
Om te begrijpen hoe zo’n herbestemming zich mogelijk heeft ontvouwd, vergeleken de auteurs sequenties en activiteiten van verwante complexen in veel bacteriën en archaea. Ze identificeerden meer dan duizend genclusters die hetzelfde trio enzymtypes bevatten. Sommige ondersteunen nog steeds klassieke thiolasechemie; andere, zoals die in Pseudomonas, voeden verschillende kleine-molecuulantibiotica. Een representatief complex uit Pseudomonas fluorescens lijkt zich halverwege dit evolutionaire traject te bevinden: de HMGS-achtige domein is uitgeschakeld, maar de ACAT-achtige eenheid voert nog een meer conventionele reactie uit op CoA-gebonden substraten. In SmaATase en zijn Pseudomonas-tegenhanger die de gewasbeschermende verbinding DAPG maakt, hebben verdere veranderingen rond het actieve centrum de enzymen afgestemd op het herkennen van niet-standaard acceptoren zoals aromatische ringen of tetraminezuur-kernen.
Waarom een kleine acetylgroep een groot verschil maakt
Uiteindelijk is de biologische meerwaarde van deze moleculaire make-over duidelijk. Toen het team de geacetyleerde antibiotica reutericycline A en DAPG testte tegen een reeks Gram-positieve bacteriën, toonden deze moleculen sterke dodelijke activiteit, terwijl hun ongeacetyleerde voorlopers veel zwakker of bijna inactief waren. Die kleine acetylgroep, op precies de juiste plaats geplaatst door het herbestemde enzymcomplex, verandert een bescheiden scaffold in een krachtig wapen, waardoor Streptococcus in de mond of Pseudomonas rondom plantenwortels hun buren kan overtreffen. Dit werk laat zien hoe evolutie bestaande enzymkaders met minimale maar strategische mutaties kan hergebruiken, routine metabole machines kan ombouwen tot gespecialiseerde middelen voor chemische verdediging — en biedt een blauwdruk voor ingenieurs die nieuwe koolstof–koolstof-bindingsvormende katalysatoren willen ontwerpen voor geneesmiddelenontdekking en synthetische biologie.
Bronvermelding: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Trefwoorden: enzym-evolutie, biosynthese van natuurlijke producten, antibioticumchemie, metabole herbestemming, Friedel-Crafts-acylatie