Clear Sky Science · nl
Menselijke iPSC-gebaseerde modellering van longfibrose onthult dat remming van p300/CBP de alveolaire overgangsceltoestand onderdrukt
Waarom littekenvorming in de longen ons allemaal raakt
Idiopathische longfibrose (IPF) is een meedogenloze ziekte waarbij de longen geleidelijk veranderen in littekenweefsel, waardoor elke ademhaling zwaarder wordt. De huidige medicijnen kunnen dit proces slechts vertragen en veroorzaken vaak vervelende bijwerkingen. Deze studie maakt gebruik van geavanceerde stamcel- en genomische technieken om vernauwde longen in het laboratorium na te bootsen en stelt een eenvoudige maar cruciale vraag: kunnen we een schakel vinden die beschadigde longcellen wegstuurt van een schadelijke toestand en terug naar genezing?
Een in de lab gekweekte kijk in een littekenlong
Om IPF te bestuderen, bouwden de onderzoekers miniatuurlongen van menselijke geïnduceerde pluripotente stamcellen (iPSC's). Deze iPSC's werden gestuurd om alveolaire cellen te worden—de cellen die de kleine luchtzakjes bekleden waar zuurstof het bloed binnenkomt—and werden samen gekweekt met longfibroblasten, de bindweefselcellen die littekens vormen. In een zachte gel ingebed, gedroegen deze “alveolaire organoïden” zich veel als echt longweefsel. Bij blootstelling aan het chemotherapeuticum bleomycine, een bekende trigger voor longaantasting, trokken de gels samen doordat fibroblasten eraan trokken, wat het weefselcontractieproces in fibrose nabootste.
Met dit systeem screende het team een bibliotheek van 264 kleine moleculen en mat automatisch hoeveel elk middel de gelcontractie verhinderde, waarbij een deep-learning beeldanalysetool zorgde voor objectieve metingen. Veel verbindingen hadden geen effect, maar één familie stak duidelijk boven de rest uit: remmers van de eiwitten p300 en CBP, die helpen bepalen hoe DNA wordt verpakt en welke genen worden aangezet. Alle acht p300/CBP-gerichte verbindingen in de bibliotheek verminderden contractie bij lage doses, wat dit pad benadrukt als een veelbelovende knop om fibrose te beïnvloeden. 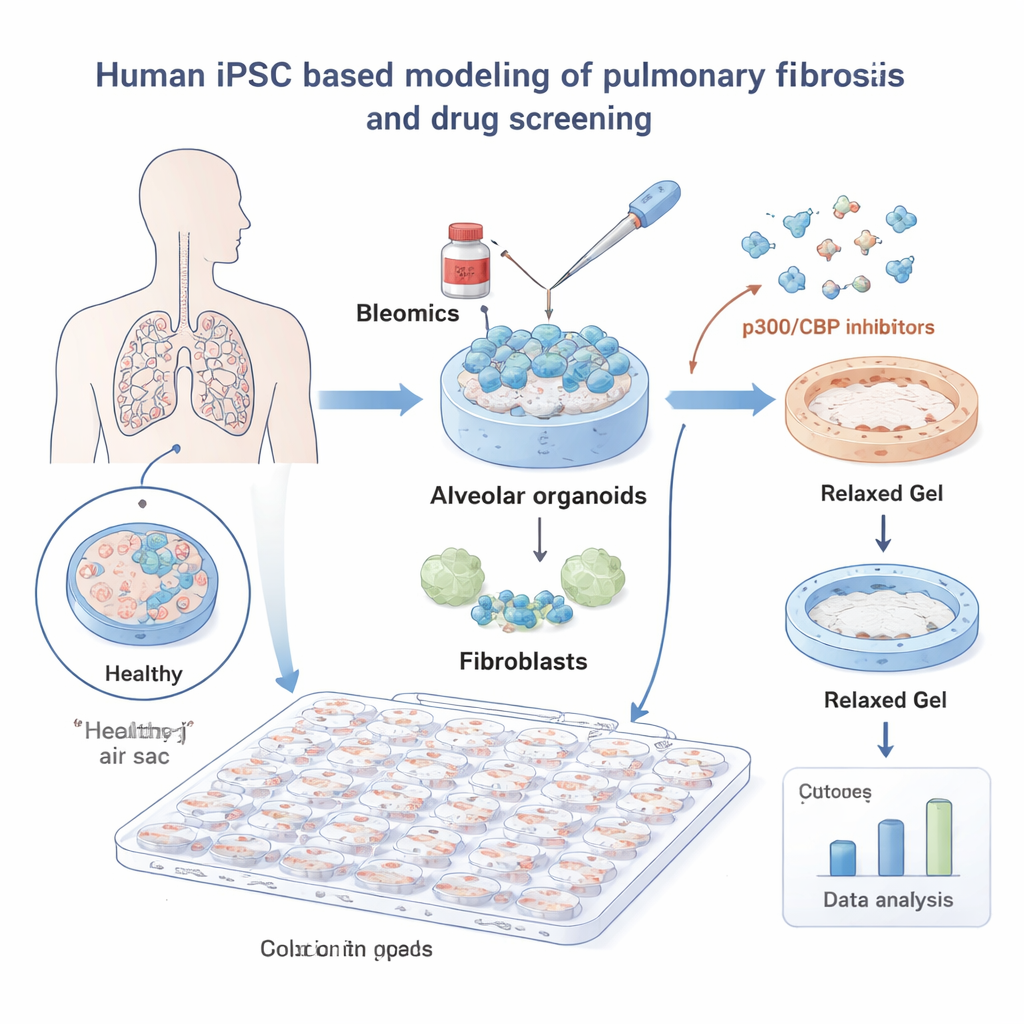
De boosdoeners: transitionele longcellen
Recent werk heeft een problematisch “tussen”celtype aan het licht gebracht in zieke longen, genoemd de alveolaire transitionele celtoestand. Normaal rijpen ondersteunende cellen, bekend als AT2-cellen, uit tot ultradunne AT1-cellen die de luchtzakjes bedekken en gaswisseling mogelijk maken. Bij IPF blijven AT2-cellen echter vaak steken in deze transitionele toestand, waarbij ze stress- en herstelgenen tot expressie brengen terwijl ze er niet in slagen de transitie naar volledig functionele AT1-cellen te voltooien. Deze transitionele cellen clusteren in fibrotische gebieden en communiceren intens met fibroblasten, maar het was onduidelijk of ze louter een bijproduct van schade zijn of actieve aandrijvers van littekenvorming.
Door RNA-sequencing en profiling van open chromatine in hun organoïden te gebruiken, toonden de auteurs aan dat de transitionele cellen die in hun model ontstonden nauw overeenkwamen met die in longen van IPF-patiënten. Deze geïnduceerde transitionele cellen vertoonden gendetektes van stress, ontsteking en matrixhermodellering en activeerden sterk metgekweekte volwassen longfibroblasten. Cruciaal was dat bij blokkering van p300/CBP de markers van de transitionele toestand daalden, de AT2-identiteit beter behouden bleef en de activatie van fibroblasten afnam. Met andere woorden, de middelen vergiftigden niet breedweg cellen; ze voorkwamen selectief dat AT2-cellen vast kwamen te zitten in deze schadelijke tussentoestand.
De moleculaire schakelaars ontrafelen
Om te begrijpen hoe p300/CBP deze beslissingsroute vormgeeft, onderzocht het team chemische merken op histonen—eiwitten die helpen bij de verpakking van DNA. Een specifiek merkteken, H3K27-acetylatie, wordt vaak door p300/CBP geplaatst bij actieve enhancers en promotors. In transitionele cellen droegen regio's nabij stressrespons- en pro-fibrotische genen sterke H3K27-acetylatie en waren ze verrijkt voor bindingsplaatsen van transcriptiefactoren zoals AP-1 en HNF1B. Wanneer cellen werden behandeld met p300/CBP-remmers, namen deze acetylmerken op die plaatsen af en daalde de expressie van veel pro-fibrotische genen. Het direct blokkeren van AP-1, of het verlagen van AP-1 en HNF1B met kleine interfererende RNA's, beperkte eveneens het transitionele programma en de organoïdecontractie, en koppelde dit drietal—p300/CBP, AP-1 en HNF1B—aan de motor die fibrotisch herstructureren aandrijft.
Buiten het schaaltje testte de studie één remmer, CBP30, in muizen met bleomycine-geïnduceerde longaantasting. Dieren die CBP30 kregen, hadden minder transitionele epitheelcellen, minder activatie van littekenvormende myofibroblasten en verminderde expressie van fibrosemarkers. Deze kruisvalidatie tussen menselijke stamcelmodellen en een diermodel versterkt het idee dat p300/CBP niet slechts een laboratoriumartefact is maar een echte regulator van longlittekenvorming. 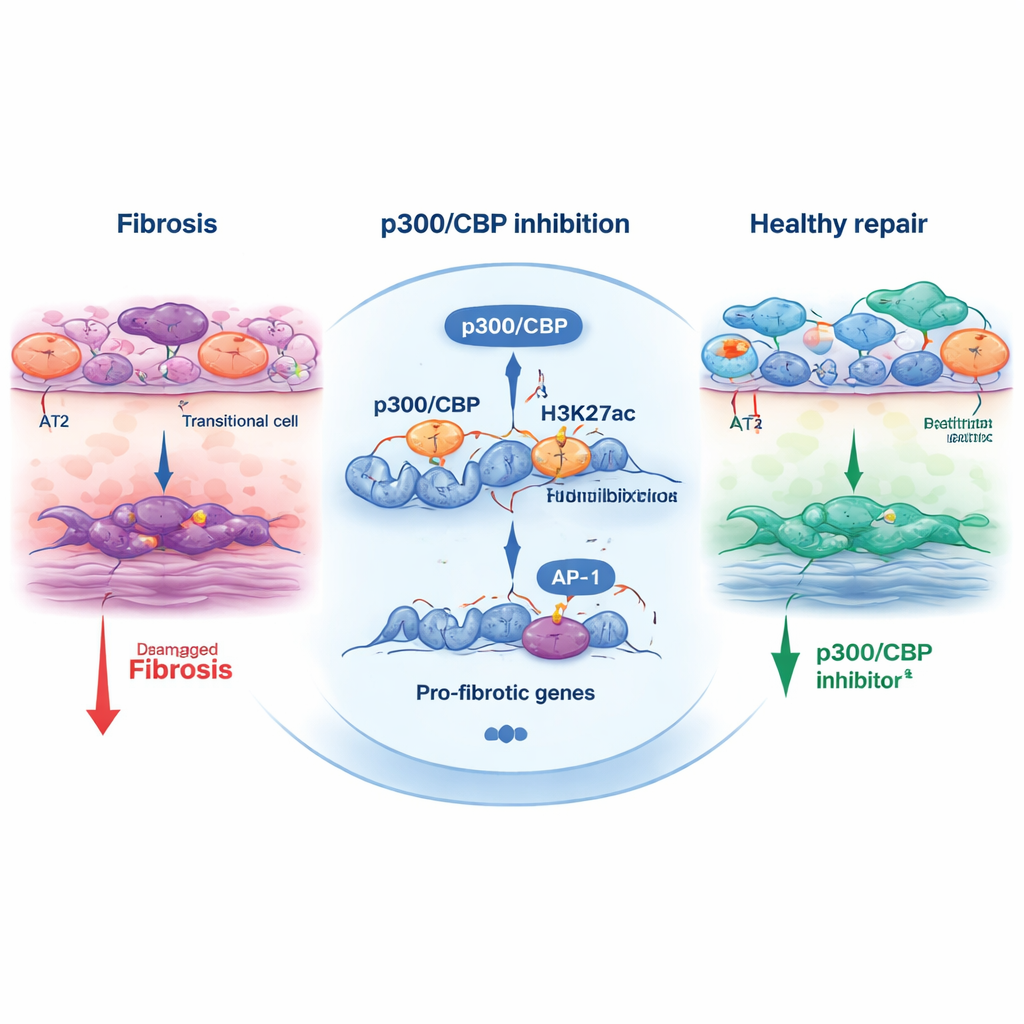
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de belangrijkste conclusie dat de auteurs een realistisch menselijk model van fibrotische longen hebben opgebouwd en het gebruikten om een nieuw geneesmiddeldoelpunt in de schijnwerpers te zetten. Hun werk suggereert dat longlittekenvorming deels wordt aangedreven door een omkeerbare, stress-geïnduceerde transitionele celtoestand die het omliggende weefsel op het verkeerde been zet. Door p300/CBP terug te draaien, zou het mogelijk zijn deze toestand te dempen, alveolaire cellen op een gezonde ontwikkelingsroute te houden en de signalen te verminderen die fibroblasten in overdrive brengen. Hoewel p300/CBP-remmers nog moeten worden geoptimaliseerd voor veiligheid en klinisch getest, wijst deze studie op therapieën die de fundamentele cellulaire miscommunicatie in IPF aanpakken in plaats van slechts de gevolgen te vertragen.
Bronvermelding: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
Trefwoorden: idiopathische longfibrose, alveolaire organoïden, p300/CBP-remmers, transitionele epitheelcellen, longstamcellen