Clear Sky Science · nl
Plasmiden ontwerpen met synthetische replicatie-oorsprongen
Waarom het herschrijven van microbieel DNA ertoe doet
Veel van de instrumenten achter moderne biotechnologie, van de productie van insuline tot geavanceerde genregulatorische schakelingen, vertrouwen op kleine DNA-cirkelvormen die plasmiden worden genoemd. Deze genetische werkpaarden brengen gemodificeerde genen in bacteriën, maar hun basisontwerp is al decennia nauwelijks veranderd. Deze studie laat zien dat het hart van plasmiden—de sequenties die cellen vertellen wanneer en hoe vaak ze gekopieerd moeten worden—volledig opnieuw kunnen worden uitgedacht. Door deze "kopieermotor" helemaal opnieuw op te bouwen, creëren de auteurs plasmiden die gemakkelijker af te stemmen, te combineren en te programmeren zijn, wat de weg vrijmaakt voor flexibelere diagnostiek, bioproductie en synthetische biologie.
Oude gereedschappen met verborgen beperkingen
Plasmiden zijn van nature geëvolueerd als mobiel DNA en stellen bacteriën in staat eigenschappen te delen, zoals antibioticaresistentie of nieuwe manieren om voedingsbronnen af te breken. In het lab lenen ingenieurs deze plasmiden om nuttige genen te dragen, maar de meeste vertrouwen op een paar klassieke ontwerpen die in de jaren tachtig werden ontdekt. Die oude ontwerpen verbergen een kluwen van overlappende genetische onderdelen die regelen hoeveel kopieën van een plasmide in elke cel aanwezig zijn en of verschillende plasmiden vreedzaam naast elkaar kunnen bestaan. Omdat die onderdelen aan elkaar vastzitten, kan het veranderen van één eigenschap onvoorspelbaar een andere beschadigen. Als gevolg daarvan zitten wetenschappers vast aan een beperkt assortiment plasmiden met vaste kopieaantallen en beperkte compatibiliteit, wat de complexiteit van ontworpen systemen beperkt.
De kopieermotor vanaf nul herbouwen
De onderzoekers concentreerden zich op een veelgebruikte replicatie-oorsprong uit de pMB1-plasmidenfamilie. In zijn natuurlijke vorm gebruikt deze oorsprong een fijn afgestemd samenspel tussen twee RNA’s—één die de DNA-replicatie start en een andere die die activiteit blokkeert—om het aantal plasmiden onder controle te houden. Het team "refactoreerde" dit systeem: ze haalden overlappende genen uit elkaar, schakelden een verborgen promotor uit en plaatsten belangrijke elementen op aparte, schone genetische cassettes. Dit alleen al toonde dat de kernfunctie van de oorsprong behouden kon blijven terwijl het ontwerp werd vereenvoudigd, waardoor een rommelig, door evolutie gevormd onderdeel veranderde in iets meer als een modulair mechanisme met toegankelijke componenten.
Synthetische bedieningsknoppen inbouwen
Met de oorspronkelijke regellogica blootgelegd vervingen de auteurs die door volledig synthetische regelaars. Ze koppelden de replicatieprimer aan ontworpen RNA-schakelaars die werken als dimmers: kleine controlerende RNA’s kunnen deze schakelaars omzetten zodat de productie van de primer wordt toegestaan of geblokkeerd en daarmee de plasmidreplicatie wordt geregeld. Door verschillende schakelaars te kiezen en ze te combineren met promotoren van uiteenlopende sterkte, stemden ze het kopieaantal van plasmiden af over meer dan twee grootteordes. Ze onderzochten ook verschillende fysieke lay-outs van de controlecassettes op het DNA en ontdekten ordeningen die de stabiliteit verbeterden en het mogelijk maakten het replicatiegebied te verkleinen tot een compact, functioneel kernstuk terwijl natuurlijke hulpsystemen werden toegevoegd die problematische plasmidenverstrengeling voorkomen.
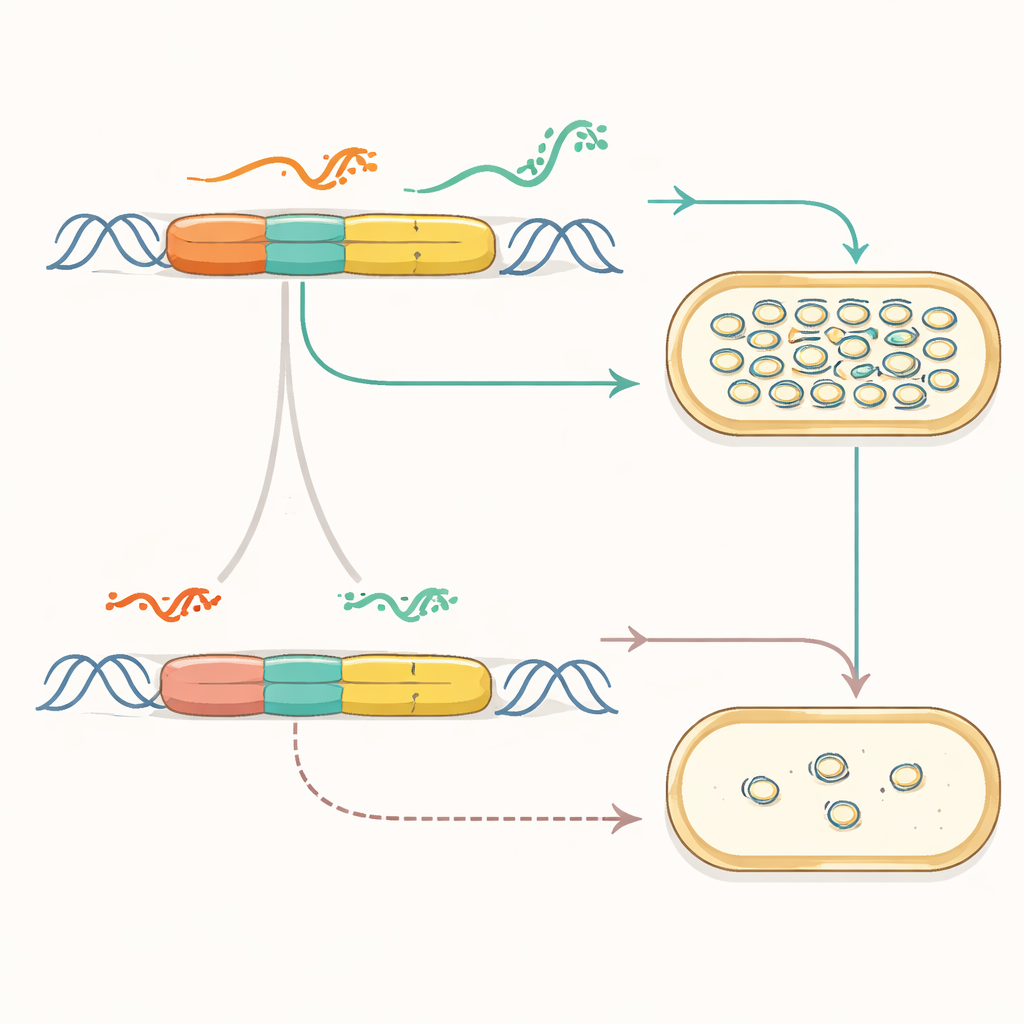
Chemische signalen omzetten in DNA-aantallen
Zodra de kopieermotor modulair was, lieten de onderzoekers zien dat deze aan externe signalen gekoppeld kon worden. Ze verbonden de synthetische oorsprong met inductibele promotoren en RNA-structuren genaamd riboswitches, die van vorm veranderen als reactie op kleine moleculen. In deze nieuwe plasmiden zorgde het toevoegen van een chemische stof zoals IPTG of cumaat ervoor dat het plasmidekopieaantal—en daarmee een rapportagesignaal—stijgt of daalt. Meerdere signalen konden worden gecombineerd zodat de ene chemische stof de kopie stimuleerde terwijl een andere deze remde. De onderzoekers bouwden zelfs paren plasmiden, elk reagerend op een verschillende chemische stof, en volgden hun veranderende kopieaantallen in dezelfde cel met DNA-sequencing, waardoor plasmideaantallen effectief een streepjescode van omgevingsgeschiedenis werden.
Veel aangepaste plasmiden in één cel
Een belangrijke test van deze aanpak was of meerdere onafhankelijk gecontroleerde plasmiden samen konden bestaan. Met behulp van een bibliotheek van orthogonale RNA-regelaars bouwde het team zes verschillende plasmiden, elk met zijn eigen synthetische oorsprong en antibiotische marker, en introduceerde alle zes tegelijk in E. coli. Whole-plasmid sequencing over meerdere dagen bevestigde dat alle zes aanwezig bleven, hoewel hun relatieve abundantie verschoof. Pogingen om hetzelfde te doen met zes conventionele plasmiden mislukten, wat benadrukt hoe het refactoreerde ontwerp en de toegevoegde stabiliteitssystemen de nieuwe plasmiden compatibeler en robuuster maken wanneer ze samen in één cel aanwezig zijn.
Wat dit betekent voor toekomstige biotechnologie
Voor de niet-specialist is de conclusie eenvoudig: de auteurs hebben plasmiden veranderd van rigide, one-size-fits-all instrumenten in een aanpasbaar platform. Hun synthetische replicatie-oorsprongen werken als plug-and-play motoren waarvan snelheid, gevoeligheid en ingangen naar wens gekozen kunnen worden. Dit maakt het mogelijk bacteriën te bouwen die chemische blootstellingen registreren als veranderingen in DNA-kopieaantal, veel genetische routes parallel te testen door ze over meerdere plasmiden te verdelen, of groei en productie fijn af te wegen in industriële stammen. Hoewel er nog enkele stabiliteitstrade-offs bestaan, toont dit werk aan dat de kernmechanica van plasmidreplicatie niet langer ontoegankelijk is voor engineering, en opent het nieuwe mogelijkheden voor innovatie in synthetische biologie.
Bronvermelding: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Trefwoorden: synthetische plasmiden, replicatie-oorsprong, RNA-regelaars, kopieaantalcontrole, synthetische biologie