Clear Sky Science · nl
Gecorrigeerde alcoholoxidases katalyseren transesterificatie in waterige media zonder concurrerende hydrolyse
Waarom dit enzymverhaal ertoe doet
Veel alledaagse producten, van medicijnen en voedingsaroma’s tot biodiesel, rusten op een eenvoudige chemische binding die een ester heet. Het efficiënt, goedkoop en milieuvriendelijk maken en aanpassen van deze esters is een belangrijk doel in groene chemie. Het probleem is dat water, het ideale oplosmiddel vanuit veiligheid- en duurzaamheidsoptiek, deze reacties meestal saboteert door esters net zo snel af te breken als ze gevormd worden. Deze studie onthult een ontworpen enzym dat in staat is esters in water te bouwen terwijl het het omringende water bijna volledig negeert, wat een route opent naar schonere industriële chemie.
Een bekend enzym voor een nieuwe taak
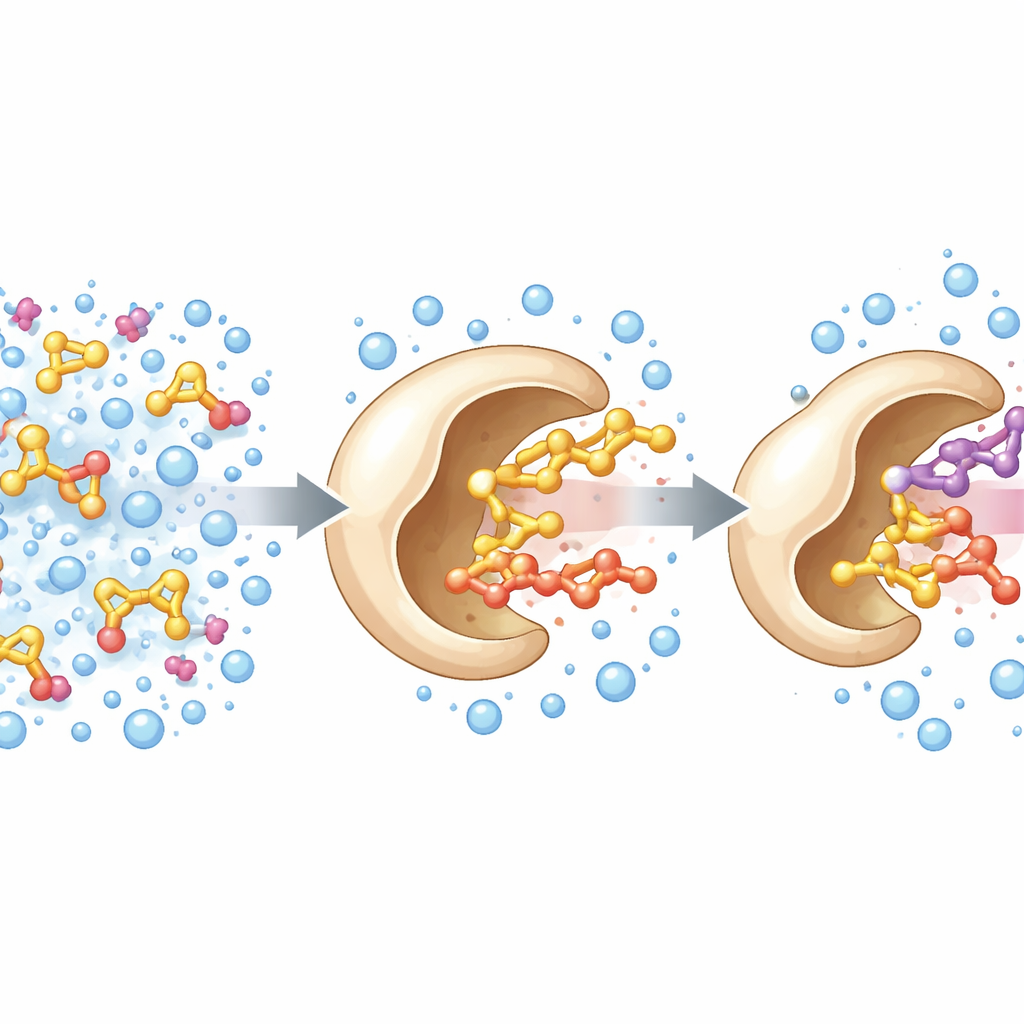
De onderzoekers begonnen met een bekend enzym, een alcoholoxidase uit een houtrotend fungus. In de natuur gebruikt dit enzym een flavin-cofactor om elektronen van kleine alcoholen zoals methanol af te halen. Het team wilde het bereik van het enzym uitbreiden zodat het grotere, volumineuzere alcoholen aankon, die relevanter zijn voor fijnchemicaliën en aroma’s. Met de driedimensionale structuur van het enzym als leidraad richtten ze zich op drie aminozuren die een soort poort vormen naar het actieve centrum. Door deze posities te randomiseren en de resulterende varianten te screenen, ontdekten ze een triple-mutant — genoemd PcAOx-VPN — die grotere alcoholen zoals benzylalcohol efficiënt kon verwerken terwijl veel van de oorspronkelijke activiteit tegen kleine alcoholen zoals methanol verloren ging.
Onverwachte vaardigheid: esters maken in water
Bij tests van PcAOx-VPN in mengsels ontworpen om olieachtige substraten op te lossen, zagen de onderzoekers extra pieken in hun analytische metingen. Deze bleken geacetyleerde producten te zijn: het enzym droeg een acylgroep over van een geactiveerde ester-donor naar alcoholen, een reactie bekend als transesterificatie. Opmerkelijk was dat dit plaatsvond in een waterig buffer, iets wat normaal gesproken leidt tot hevige concurrerende hydrolyse, waarbij water het ester aanvalt en afbreekt. Hier koppelde PcAOx-VPN alcoholen en acyl-donoren zoals vinylacetaat efficiënt aan elkaar om nieuwe esters te vormen, vaak met opbrengsten boven 80% en met slechts bescheiden nevenreacties. Hetzelfde enzym kon werken op een breed scala aan alcoholen, inclusief rechtketen-, aromatische, chirale en zwavelbevattende voorbeelden, en liet in meerdere gevallen een duidelijke voorkeur zien voor één spiegelbeeldvorm boven de andere.
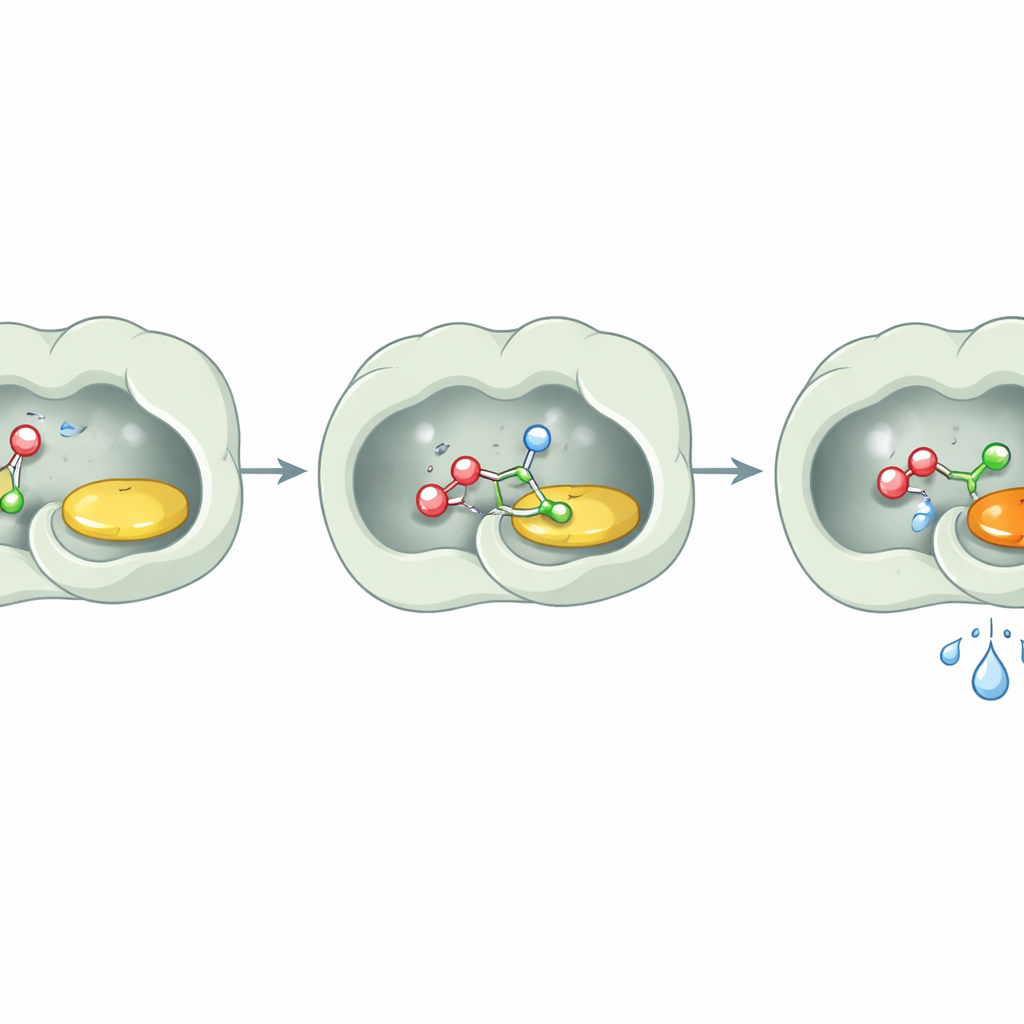
Het water buiten de deur houden
Een belangrijke verrassing was wat het enzym niet deed: het hydrolyseerde esters niet merkbaar. Zelfs na lange incubaties met estersubstraten en water liet PcAOx-VPN ze grotendeels intact tenzij een aanvullende acyl-donor werd toegevoegd. Structurele studies bieden een eenvoudige verklaring. Het actieve centrum is bekleed met overwegend olieachtige, aromatische aminozuren die een sterk hydrofoob pocket creëren. Gedetailleerde analyse toonde geen watermoleculen nabij de flavin-cofactor, en computationele hulpmiddelen bevestigden dat het kanaal naar het actieve centrum ook onvriendelijk is voor water. In wezen bouwt het enzym een kleine droge kamer binnen een waterige wereld. Alcoholen en geactiveerde esters kunnen binnenkomen en reageren, maar watermoleculen worden buiten gehouden, zodat ze nooit de kans krijgen het product af te breken.
Hoe de reactie waarschijnlijk binnenin werkt
Mechanistische experimenten en mutatieanalyse toonden aan dat twee aminozuren, een histidine en een asparagine, centraal staan in zowel de natuurlijke oxidatiefunctie van het enzym als in zijn nieuwe transesterificatievermogen. De histidine fungeert als base en helpt een proton van het binnenkomende alcohol af te trekken om het reactiever te maken, terwijl de asparagine de resulterende geladen toestand stabiliseert. Samen bevorderen ze de aanval van het alcohol op de acyl-donor om een kortstondig intermediair te vormen dat instort tot het gewenste ester. De geoxideerde toestand van de flavin-cofactor is ook vereist: onder zuurstofvrije omstandigheden, wanneer de flavin gereduceerd wordt, stopt de transesterificatie en hervat pas weer wanneer lucht wordt teruggebracht. Opmerkelijk is dat wanneer dezelfde trio mutaties in verwante oxidases uit andere schimmels werd ingebracht, ook die enzymen robuuste transesterificatie-activiteit kregen, wat suggereert dat dit gedrag gegeneraliseerd kan worden.
Wat dit betekent voor groenere chemie
Voor niet-specialisten is de kernboodschap dat de auteurs een bekend enzym een nieuwe truc hebben geleerd: nuttige esters rechtstreeks in water bouwen, terwijl ze de neiging van water om het werk ongedaan te maken effectief negeren. Door een droge, olie-vriendelijke pocket in een eiwit uit te hollen en een paar sleutelaminozuren bij te stellen, creëerden ze een katalysator die alcoholen boven water prefereert als reactanten. Omdat hetzelfde ontwerpbeginsel werkt in verwante enzymen, zou deze benadering uitgebreid kunnen worden naar een familie van katalysatoren voor het maken van aroma’s, geuren, fijnchemicaliën en mogelijk biobrandstoffen in veiligere, meer duurzame processen die minder afhankelijk zijn van agressieve organische oplosmiddelen en meer op water vertrouwen.
Bronvermelding: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Trefwoorden: enzyme engineering, biocatalysis, green chemistry, ester synthesis, flavoproteins