Clear Sky Science · nl
PRMT3-gemedieerde post-translationele aanpassing aan vasten reguleert metabole flexibiliteit
Waarom het tijdstip van eten en brandstof in het lichaam ertoe doen
Veel mensen proberen vasten of tijdgebonden eten om af te vallen of hun bloedsuiker te verbeteren, maar de uitkomsten zijn wisselend. Deze studie kijkt onder de motorkap van onze stofwisseling om te begrijpen waarom. Met focus op buikvet bij muizen en op menselijke monsters, ontdekken de onderzoekers een moleculaire schakelaar die vetweefsel helpt beslissen of het brandstof verbrandt of opslaat, en tonen aan hoe zowel het tijdstip van eten als een geneesmiddel die schakelaar kunnen omschakelen richting betere gezondheid.
Een flexibele motor in ons vet
Ons lichaam functioneert het best wanneer het soepel kan schakelen tussen het verbranden van vet tijdens vasten en het verbranden van suiker na maaltijden. Deze “metabole flexibiliteit” gaat vaak verloren bij obesitas, waardoor het lastiger wordt schommelingen in energie-aanbod en -vraag op te vangen. Het team bestudeerde visceraal wit vet — het diepe buikvet dat sterk geassocieerd wordt met diabetes en hartziekten — en vond dat specifieke chemische labels op eiwitten, methylgroepen genoemd, veranderen met voeden en vasten. Bij zowel muizen als mensen hopen twee van die labels, MMA en ADMA, op in visceraal vet naarmate het lichaamsgewicht en de body mass index stijgen, wat suggereert dat ze aanwijzingen zijn voor een trage, minder aanpasbare stofwisseling.
Een voedingssignaal dat de stofwisseling verstijft
De onderzoekers richtten zich op een enzym in vetcellen genaamd PRMT3, dat deze methyllabels toevoegt. Bij muizen stijgen de PRMT3-niveaus in visceraal vet ’s nachts wanneer de dieren eten en dalen ze overdag tijdens het vasten, nauw aansluitend bij het patroon van MMA en ADMA. Dit ritme hangt af van insuline en een sleutelsignaleiwit, AKT: wanneer voedsel of geïnjecteerde insuline AKT activeert, wordt PRMT3 aangezet en sterker gemodificeerd, wat op zijn beurt het aantal gemethyleerde eiwitten verhoogt. Het blokkeren van AKT of het direct remmen van PRMT3 effent snel dit methylatiesignaal, en kan zelfs het effect van een veel langere vastenperiode nabootsen.
Vetcellen omprogrammeren van opslag naar verbranding
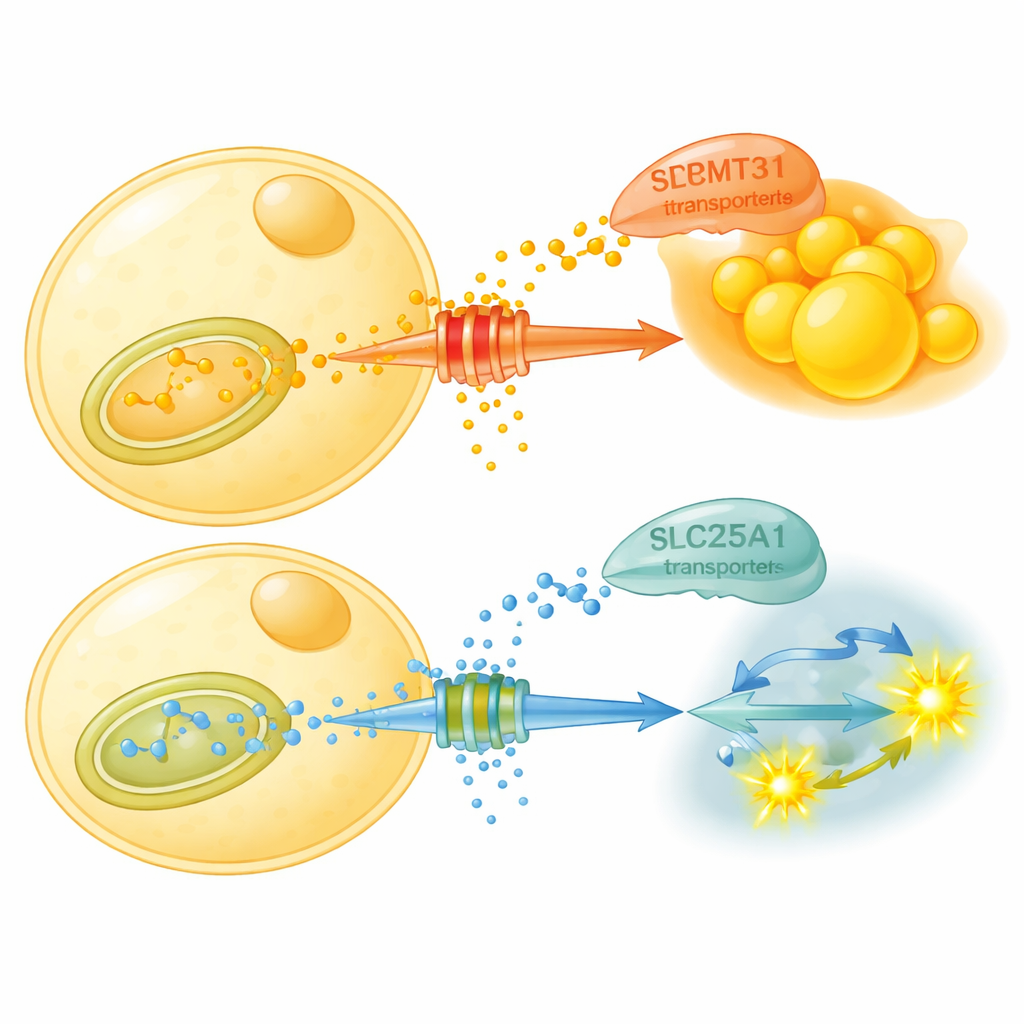
Wat doet deze chemische etikettering precies? De studie toont aan dat PRMT3 een transportereiwit genaamd SLC25A1 in de mitochondriën — de energiecentrales van de cel — stabiliseert. SLC25A1 vervoert citrate, een belangrijk metaboliet, uit de mitochondriën naar het cytosol waar het de aanmaak van nieuw vet voedt. PRMT3 methyleert twee specifieke arginineplaatsen op SLC25A1, waardoor de transporter stabieler wordt en citrate-export en vetopbouw worden aangemoedigd. Wanneer PRMT3 wordt geblokkeerd, dalen SLC25A1-niveaus, neemt citrate-export af en verschuiven vetcellen naar het afbreken van suiker in plaats van het maken van meer vet. Bij muizen op een vetrijk dieet vermindert een PRMT3-remmend middel het lichaamsvet, verbetert de glucoseregulatie en verhoogt een maat genaamd de respiratoire uitwisselingsverhouding, wat aantoont dat de dieren gemakkelijker overschakelen op het verbranden van koolhydraten.
Vastschema’s en genetische aanpassingen wijzen naar hetzelfde pad
De onderzoekers vroegen zich vervolgens af of gangbare vastpatronen dezelfde schakelaar gebruiken. Onder een 16:8 tijdgebonden voedingsschema — 16 uur vasten en 8 uur eten — verloren muizen gewicht en gingen ze beter om met glucose zonder in totaal minder te eten. Hun visceraal vet vertoonde lagere niveaus van PRMT3, SLC25A1 en gemethyleerde eiwitten, en hun brandstofgebruik werd flexibeler, vooral ’s nachts wanneer ze normaal eten. Opmerkelijk was dat het toedienen van het PRMT3-remmende middel op specifieke tijden van de dag veel van dezelfde voordelen opleverde als het 16:8-schema. Het genetisch verwijderen van SLC25A1 alleen in vetcellen beschermde muizen ook tegen dieet-geïnduceerde hoge bloedsuiker en leververvetting, wederom door het bevorderen van suikerafbraak en energieverbruik in vet, zelfs zonder afname van vetmassa.
Wat dit betekent voor toekomstige therapieën
Gezamenlijk suggereren de bevindingen dat diep buikvet een timing-gevoelige schakelaar bevat, gecontroleerd door insuline, AKT, PRMT3 en SLC25A1, die bepaalt of ons lichaam metabolisch lenig blijft of vastloopt in een opslagmodus. Tijdgebonden eten lijkt deze schakelaar richting flexibiliteit te duwen door PRMT3 en de downstream-effecten te verlagen. Een geneesmiddel dat PRMT3 remt kan veel van deze voordelen bij obese muizen reproduceren, wat wijst op een toekomstige therapie die de metabole voordelen van vasten toegankelijker maakt. Voor dagelijkse lezers is de boodschap dat wanneer we eten, niet alleen wat we eten, kan hervormen hoe ons vetweefsel met brandstof omgaat — met belangrijke gevolgen voor gewicht, bloedsuiker en de lange termijn gezondheid.
Bronvermelding: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Trefwoorden: metabole flexibiliteit, tijdgebonden voeding, visceraal vet, proteïnemethylatie, glucosemetabolisme