Clear Sky Science · nl
Een DNA-gebaseerd nanodevice detecteert purinerge signalering en stuurt een immuunschakelaar aan voor het oplossen van ontsteking
Het alarmsysteem van het lichaam stiller zetten
Wanneer ons weefsel beschadigd raakt, lekken cellen een golf van chemische “alarmsignalen” die immuuncellen aantrekken om infecties te bestrijden en afval op te ruimen. Deze reactie is essentieel, maar als het alarm te hard of te lang loeit, kan het schadelijke ontsteking in de longen, nieren en andere organen veroorzaken. Deze studie beschrijft een piepklein, programmeerbaar DNA-gebaseerd apparaatje dat kan waarnemen wanneer het alarmsignaal te sterk is en het zachtjes terugschroeft, zodat het immuunsysteem kan overschakelen van aanval naar herstel.
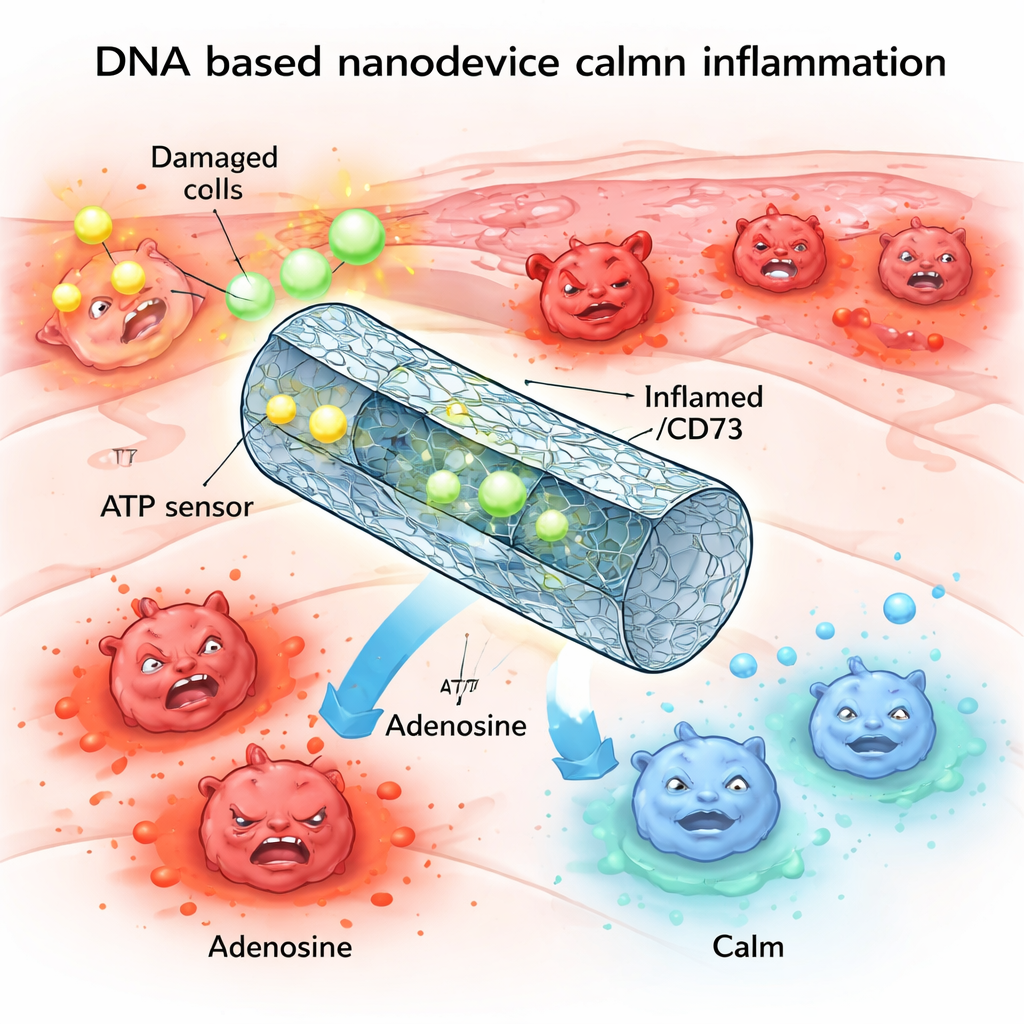
Een chemisch alarm dat te ver kan gaan
Een van de belangrijkste alarmsignalen van het lichaam is ATP, vooral bekend als de “energiemunt” binnen cellen. Bij beschadiging of stress lekt grote hoeveelheden ATP uit beschadigde cellen naar de omgeving. Dat extracellulaire ATP fungeert daar als een noodsignaal, bindt aan receptoren op immuuncellen en duwt ze naar een zeer ontstekingsbevorderende toestand. Onder gezonde omstandigheden breken enzymen op celoppervlakken overtollig ATP snel af tot adenosine, een verwante stof met een kalmerend, ontstekingsremmend effect. Maar bij veel chronische of ernstige ontstekingsziekten werkt dit afbraaksysteem niet goed, blijven ATP-niveaus hoog en adenosine laag, en raken weefsels verstrikt in een vicieuze cirkel van schade.
Een slimme DNA‑buis bouwen
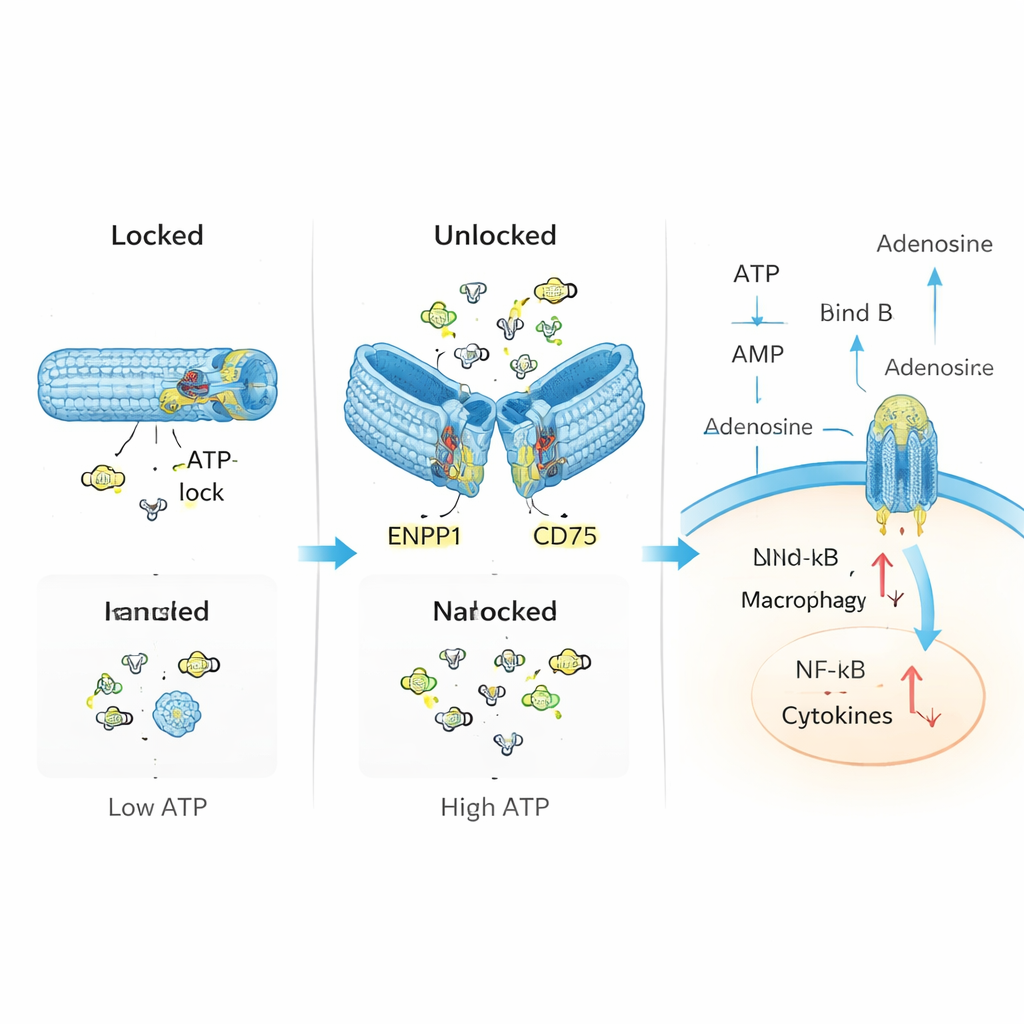
De onderzoekers wilden dit natuurlijke regelsysteem imiteren en herstellen met DNA-nanotechnologie. Ze bouwden een holle buis van DNA, gevouwen als origami, en voorzagen die van twee hoofdcomponenten: “sensoren” die ATP herkennen en enzymen die ATP omzetten in adenosine. In de rusttoestand wordt de buis gesloten gehouden door korte DNA-segmenten die tegelijk als ATP-sensoren fungeren. Wanneer ATP-niveaus boven een bepaalde drempel stijgen die kenmerkend is voor beschadigd weefsel, bindt ATP aan deze segmenten, waardoor de buis opengaat en de enzymen ENPP1 en CD73 binnenin blootlegt. Deze verteren vervolgens het overtollige ATP en produceren adenosine, waardoor de lokale chemische balans geleidelijk verschuift van gevaar naar herstel.
Aantonen dat de schakelaar werkt
In gecontroleerde laboratoriumtests bevestigde het team dat hun DNA-buis gesloten blijft bij lage ATP-concentraties maar betrouwbaar opengaat wanneer ATP overvloedig aanwezig is, vergelijkbaar met een noodklep. Eenmaal ontgrendeld zet het apparaatje continu ATP om in tussentijdse producten en uiteindelijk in adenosine, zonder merkbaar de activiteit van de enzymen te schaden. In immuuncellen die werden blootgesteld aan hoge ATP-concentraties verminderde dit nanodevice toxische bijproducten in mitochondriën, verlaagde het de activatie van ontstekingsroutes zoals NF-κB en het NLRP3-inflammasoom, en versterkte het signalen gekoppeld aan de kalmerende werking van adenosine. Met andere woorden: het apparaatje ruimde niet alleen ATP op; het herprogrammeerde actief het gedrag van cellen van ontstekingsbevorderend naar regelgevend.
Meeliften naar plaatsen van beschadiging
Een slimme schakelaar ontwerpen is één ding; hem op de juiste plaats in het lichaam krijgen is iets anders. Om dit afleveringsprobleem op te lossen bevestigden de onderzoekers hun DNA-buizen aan het oppervlak van circulerende monocyten, een type witte bloedcel dat van nature naar ontstoken weefsels trekt. Met een cholesterol‑gekoppelde DNA‑anker „parkeerden" ze grote aantallen nanodevices op het membraan van elke cel, waar de apparaten grotendeels aan het oppervlak bleven in plaats van door de cel te worden opgenomen. In muismodellen van acute long‑ en nierbeschadiging stapelden deze gedecoreerde monocyten zich veel efficiënter op in beschadigde organen dan vrije deeltjes, en de nanodevices reageerden nog steeds specifiek op hoge ATP in het beschadigde weefsel.
Weefsels helpen herstellen
Bij muizen met chemisch geïnduceerde long‑ of nierbeschadiging verminderde behandeling met het DNA‑apparaat weefselschade, ophoping van immuuncellen en ontstekingsboodschappermoleculen. De versie gedragen door monocyten werkte het best en bood sterkere bescherming dan zowel het vrije apparaat als de enzymen afzonderlijk. Diepergaand genetisch en metabolisch onderzoek van longweefsel toonde aan dat deze aanpak niet alleen ontstekingsgenen dempte maar ook verstoorde energiemetabolismen in cellen hielp herstellen. Belangrijk is dat de apparaten weinig toxiciteit toonden en geen schadelijke immuunreacties veroorzaakten in gezonde dieren.
Waarom dit belangrijk is voor toekomstige therapieën
Voor niet‑specialisten is de kernboodschap dat dit werk een programmeerbare, moleculaire „thermostaat" voor ontsteking aantoont. Gemaakt van DNA en natuurlijke enzymen, detecteert het nanodevice wanneer een gevaarsignaal te sterk is en zet het dat automatisch om in een kalmerend signaal, waardoor immuuncellen tot bedaren komen en weefsels kunnen herstellen. Hoewel het zich nog in een vroeg experimenteel stadium bevindt, suggereert deze strategie een nieuwe klasse behandelingen die niet simpelweg immuunroutes overal blokkeren, maar in plaats daarvan lokaal chemische signalen op plaatsen van beschadiging herstellen, wat mogelijk precieze controle over schadelijke ontsteking bij veel ziekten biedt.
Bronvermelding: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Trefwoorden: DNA-nanodevice, extracellulair ATP, ontsteking, adenosinesignalering, nanogeneeskunde