Clear Sky Science · nl
Anti-TLR2-immunotherapie moduleert de overdracht van α-synucleïne van neuron naar oligodendrocyt in muis- en menselijke modellen
Waarom dit onderzoek ertoe doet
Multiple system atrophy (MSA) is een zeldzame maar snel voortschrijdende hersenaandoening die Parkinson-achtige bewegingsproblemen combineert met evenwichts- en autonome uitval, zoals bloeddrukdaling. Artsen kunnen de symptomen verlichten, maar op dit moment het ziekteproces zelf niet tot staan brengen. Deze studie onthult hoe een verkeerd gevouwen eiwit zich tussen hersencellen verspreidt en de "isolatie" van hersenbedrading beschadigt, en laat zien dat een gerichte antilichaambehandeling dit proces kan onderbreken in dier- en celmodellen. Het werk wijst op een concrete, geneesmiddelachtige strategie die mogelijk op termijn niet alleen de symptomen behandelt maar de loop van MSA kan veranderen.
Hoe de hersenbedrading misgaat
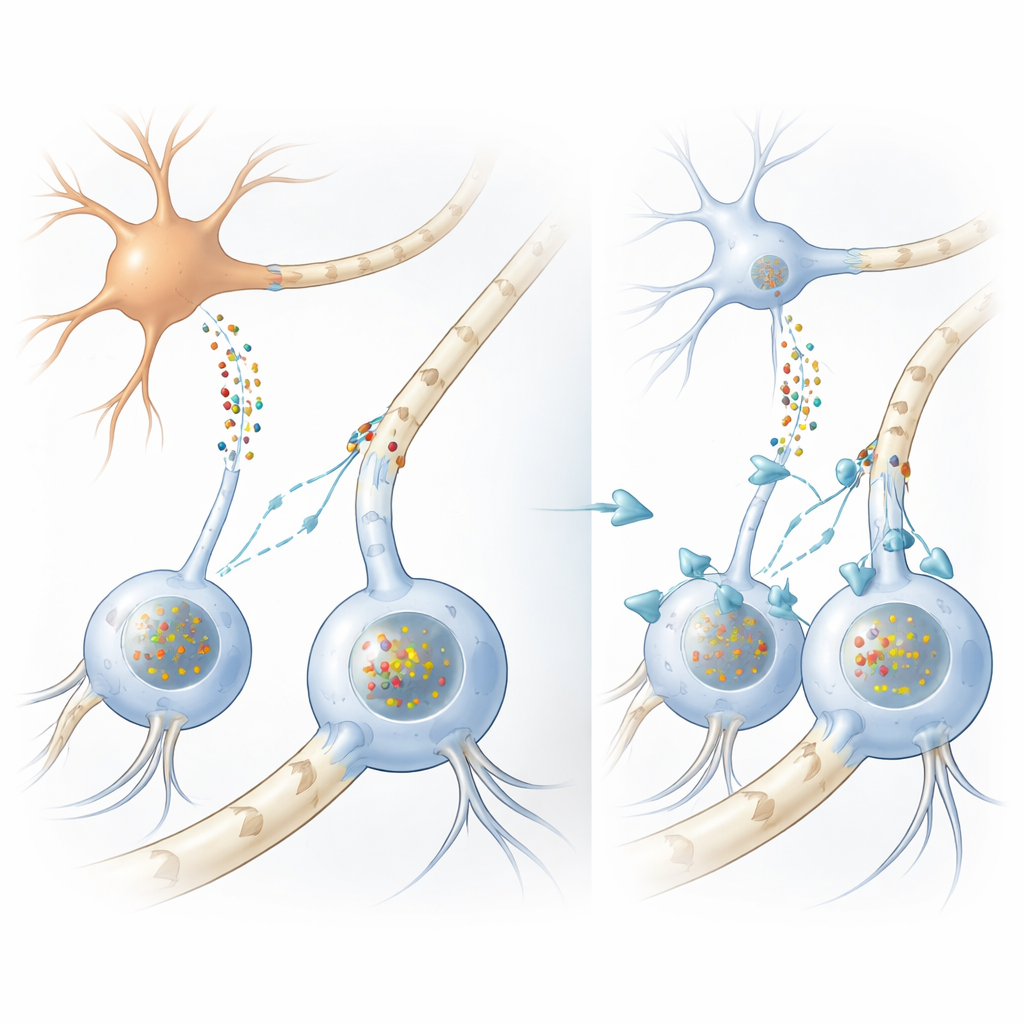
Bij veel bewegingsstoornissen, waaronder de ziekte van Parkinson, hopen zich klonters op van een eiwit genaamd alpha-synucleïne in zenuwcellen. Bij MSA echter vormen de opvallendste ophopingen zich in ondersteunende cellen, oligodendrocyten, die normaal axonen omwikkelen met vette myelinescheden die elektrische signalen versnellen. Vreemd genoeg produceren oligodendrocyten zelf maar zeer weinig alpha-synucleïne, wat een langbestaand raadsel oproept: waar komen die massieve eiwitophopingen in deze cellen vandaan? De auteurs bevestigden eerst, met menselijk hersenweefsel en grootschalige RNA-analyses, dat oligodendrocyten inderdaad veel minder alpha-synucleïne produceren dan neuronen, wat het idee versterkt dat het schadelijke eiwit van buitenaf moet komen.
Eiwit overgedragen van neuron naar ondersteunende cel
Om dit te testen bouwde het team verschillende complementaire modellen. In kweek schiepen ze menselijke oligodendrocytachtige cellen uit neurale stamcellen en dompelden die in medium verzameld van neuronachtige cellen die waren geconstrueerd om grote hoeveelheden alpha-synucleïne vrij te geven. De ondersteunende cellen namen dit eiwit op en ontwikkelden klonters die sterk leken op de gliale inclusies die in MSA-hersenen worden gezien, compleet met dezelfde chemische merkers en hulpeiwitten. Toen de onderzoekers keken naar een muizenstam die menselijke gemuteerde alpha-synucleïne alleen in neuronen produceert, vonden ze opnieuw menselijke eiwitklonters in oligodendrocyten in het witte stofgebied, hoewel die cellen het menselijke gen niet tot expressie brachten. Samen tonen deze experimenten aan dat alpha-synucleïne van neuronen naar oligodendrocyten kan bewegen en daar ziekteachtige inclusies kan vormen.
De poort op het celoppervlak
Vervolgens onderzochten de wetenschappers hoe het eiwit toegang krijgt tot oligodendrocyten. Eerder werk had de immuunsensor Toll-like receptor 2 (TLR2) op celoppervlakken geïdentificeerd als een aanhechtingsplaats voor alpha-synucleïne in neuronen en microgliacellen. Door genexpressiegegevens van MSA-hersenen te analyseren, vond het team dat oligodendrocyten bij patiënten ongewoon hoge niveaus van TLR2 droegen vergeleken met controles, en dat hogere TLR2 gekoppeld was aan lagere niveaus van myeline-gerelateerde genen zoals myeline basic protein. Deze relatie bleek niet in meerdere onafhankelijke Parkinson-datasets, wat suggereert dat de gevoeligheid van oligodendrocyten voor alpha-synucleïne via TLR2 een kenmerkend aspect van MSA is in plaats van een algemene eigenschap van alle synucleïneziekten.
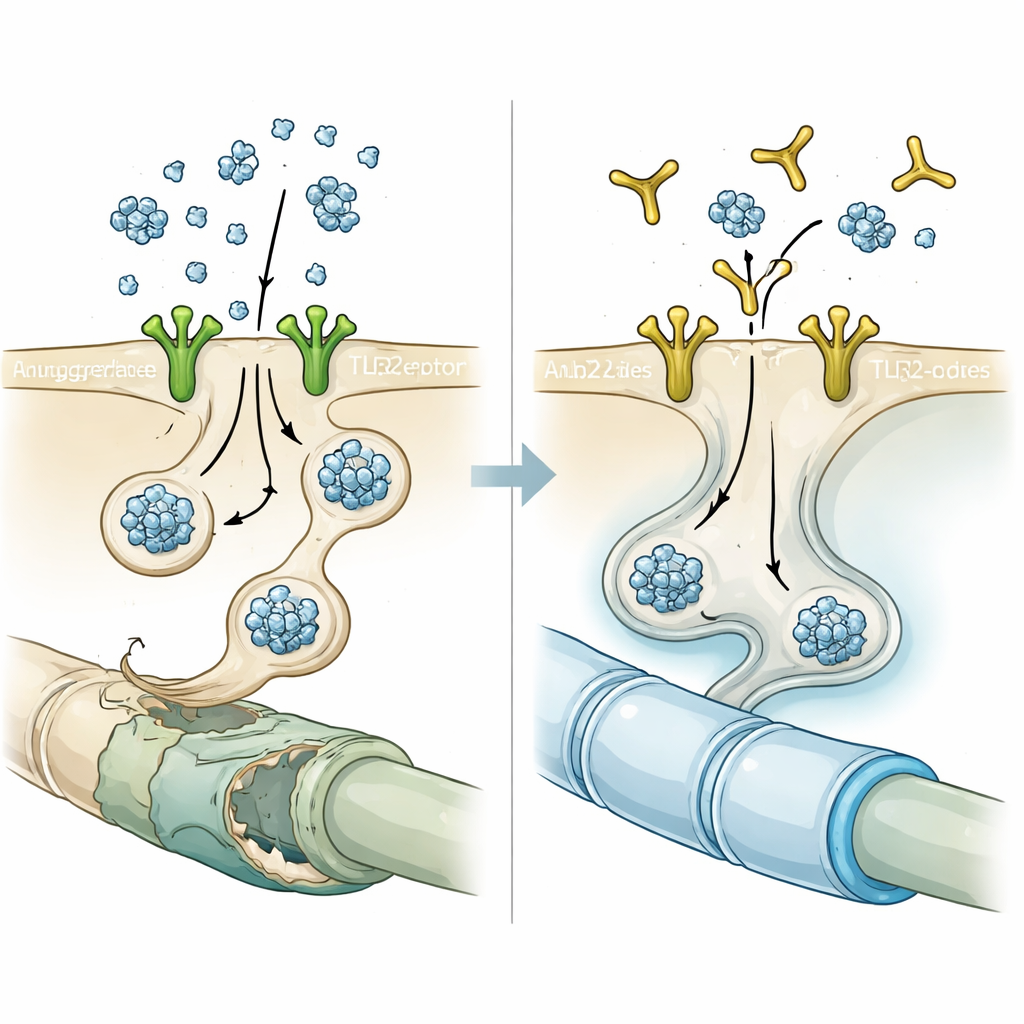
De poort blokkeren met een antilichaam
Gewapend met deze aanwijzing testten de onderzoekers NM-101, een antilichaam dat is ontworpen om aan TLR2 te binden en activatie te blokkeren. In celkweken verminderde een korte voorbehandeling van oligodendrocyten met NM-101 voordat neuron-afgeleid alpha-synucleïne werd toegevoegd sterk het aantal en de intensiteit van inclusie-achtige klonters. Bij muizen die ofwel te veel neuronale alpha-synucleïne produceerden of injecties van vooraf gevormde alpha-synucleïne fibrillen kregen, verlaagde wekelijkse NM-101-toediening geaggregeerd eiwit in het witte stof, kalmeerde ontstekingsreacties van microglia en astrocyten en verminderde de activatie van het ontstekingsenzym caspase-1 binnen oligodendrocyten. Behandelde dieren leefden langer en presteerden beter op motorische tests, wat erop wijst dat de beschermende effecten van het antilichaam functioneel betekenisvol waren en niet slechts microscopische curiositeiten.
Beschadigde isolatie herstellen
Aangezien oligodendrocyten de makers van myeline in de hersenen zijn, onderzocht het team of de overdracht van alpha-synucleïne myeline schaadde en of blokkering van TLR2 kon helpen. Single-cell RNA-sequencing van menselijk-afgeleide oligodendrocyten blootgesteld aan neuron-geconditioneerde alpha-synucleïne toonde brede verschuivingen weg van een rijpe, myeline-producerende staat en richting een meer onrijp, progenitor-achtig profiel, met veel belangrijke myelinegenen omlaag gereguleerd. Parallelle genexpressiestudies van laser-geïsoleerde oligodendrocyten uit MSA-patiënten en uit het muismodel toonden een gedeeld signatuur: verminderde expressie van genen die betrokken zijn bij het vormen en onderhouden van myeline. Onder de elektronenmicroscoop vertoonde het witte stof van alpha-synucleïne muizen dunnere, gedesorganiseerde myelinescheden. NM-101-behandeling keerde veel van deze veranderingen om, verdikte myeline, herstelde niveaus van myeline-eiwitten en normaliseerde de expressie van genen die nodig zijn voor oligodendrocytenrijping.
Wat dit betekent voor toekomstige behandelingen
De studie ondersteunt een helder verhaal: bij MSA kan door neuronen geproduceerd alpha-synucleïne via TLR2 op het oppervlak van oligodendrocyten binnendringen, zich daar ophopen, ontsteking veroorzaken, het ontwikkelingsprogramma van de cellen ontsporen en de myelinebekleding van hersenbedrading aantasten. Door TLR2 met een gericht antilichaam te blokkeren, konden de onderzoekers deze keten van gebeurtenissen onderbreken in muizen en menselijke celmodellen, waardoor toxische inclusies verminderden, ontsteking afnam, myeline werd hersteld en overleving en beweging verbeterden. Hoewel NM-101 zelf nog grondig bij mensen getest moet worden, vestigt dit werk TLR2-afhankelijke eiwitoverdracht als een centrale drijfveer van MSA-achtige pathologie en benadrukt anti-TLR2-immunotherapie als een veelbelovende strategie om deze verwoestende ziekte te vertragen of te voorkomen.
Bronvermelding: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Trefwoorden: multiple system atrophy, alpha-synucleïne, oligodendrocyten, myelineschade, immunotherapie