Clear Sky Science · nl
Olig2 werkt als een induceerbare barrière voor in vivo conversie van astrocyt naar neuron
Gliacellen in de hersenen omzetten in neuronen
De volwassen hersenen hebben slechts een beperkte capaciteit om verloren neuronen te vervangen, wat een grote belemmering vormt bij aandoeningen zoals beroerte, de ziekte van Alzheimer en ruggenmergletsel. Een veelbelovende gedachte is om nabije "ondersteunende cellen" die astrocyten heten rechtstreeks om te zetten in nieuwe neuronen met behulp van gentherapie. Deze studie stelt een cruciale vraag: wat verhindert dat die omzetting efficiënt werkt in het levende brein — en kunnen die remmen worden losgelaten?
Een verborgen rem op cellulaire transformatie
Astrocyten helpen normaal gesproken neuronen voeden, de hersenchemie in stand houden en reageren op letsel. In bepaalde ziektebeelden kunnen ze zich enigszins als stamcellen gedragen, wat de hoop wekt dat ze ter plaatse kunnen worden gereprogrammeerd tot neuronen. Wetenschappers weten al dat een klasse van genen, de proneurale transcriptiefactoren — zoals Ngn2, Ascl1 en NeuroD1 — astrocyten in de richting van een neuronale identiteit kan duwen. Toch blijft deze conversie van astrocyt naar neuron in dieren frustrerend inefficiënt. De auteurs vermoedden dat astrocyten, naast reeds bestaande verdedigingsmechanismen, een nieuwe, induceerbare barrière opwerpen zodra reprogrammering wordt opgestart.
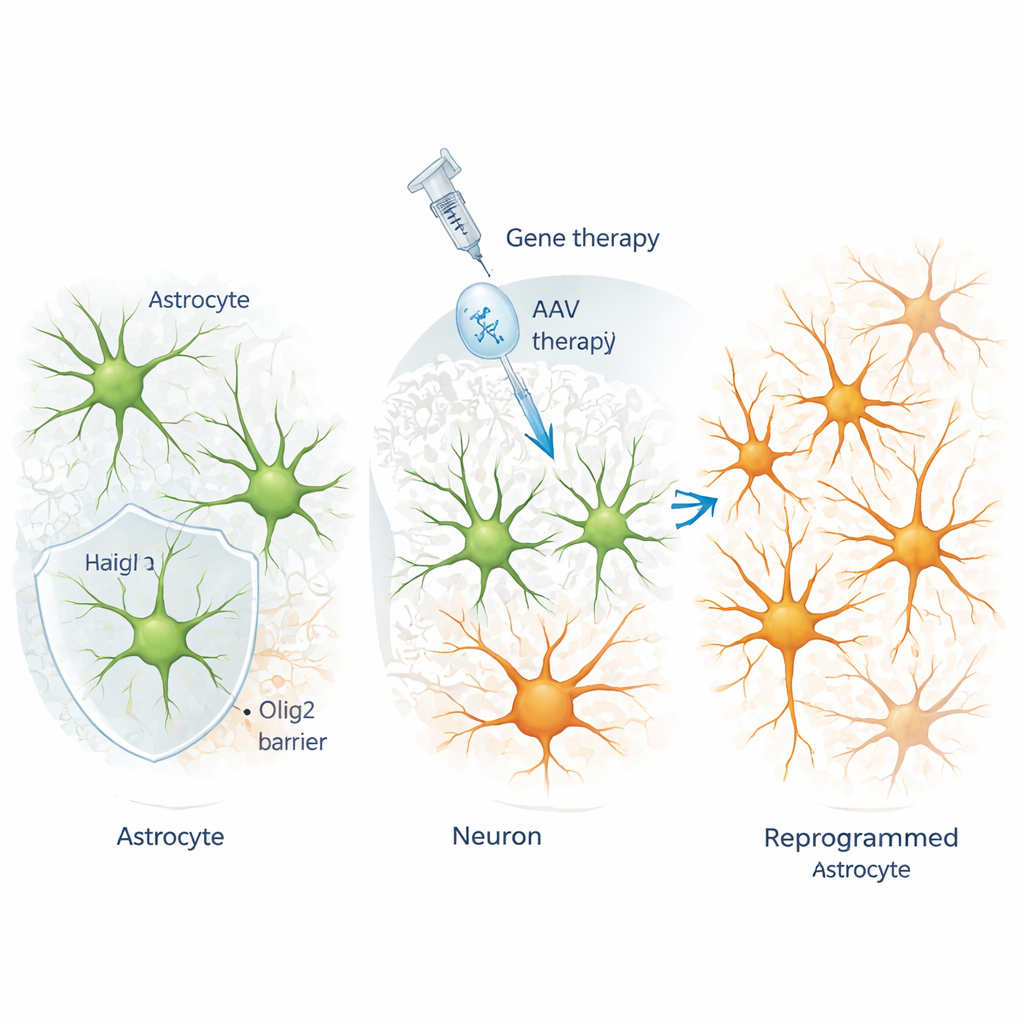
Een eiwit genaamd Olig2 treedt op om verandering te weerstaan
Werkend in de cortex van volwassen muizen leverden de onderzoekers reprogrammeringsfactoren aan astrocyten met behulp van ontworpen virussen die sterk selectief zijn voor deze cellen. Ze ontdekten dat telkens wanneer een basische helix-loop-helix (bHLH) factor zoals Ngn2, Ascl1 of NeuroD1 in astrocyten werd geforceerd, een andere bHLH-eiwit — Olig2 — sterk werd aangezet. Onder normale omstandigheden wordt Olig2 gevonden in cellen van de oligodendrocyt-lijn, niet in rijpe corticale astrocyten. Zorgvuldige traceerexperimenten toonden aan dat de extra Olig2-positieve cellen na behandeling niet werden geproduceerd door proliferatie van oligodendrocytvoorlopers — in plaats daarvan waren het juist de astrocyten die als doel voor conversie waren bedoeld die Olig2 inschakelden als reactie op het reprogrammeringssignaal.
Het wegnemen van de rem verdrievoudigt conversie en levert werkende neuronen op
Om te testen of Olig2 daadwerkelijk een barrière vormt, gebruikte het team korte haarspeld-RNA's om Olig2 specifiek in astrocyten te onderdrukken die ook Ngn2 kregen. Het stilleggen van Olig2 verlaagde de eiwitniveaus in deze cellen vrijwel tot nul en had een opvallend effect: het aandeel gelabelde astrocyten dat neuronen werd, steeg met ongeveer drie keer vergeleken met Ngn2 alleen. In de loop van enkele weken doorliepen veel cellen een tussentijdse fase, waarbij ze typische astrocytmarkers verloren voordat ze volledig neuronale markers kregen. Elektrische opnames uit hersensneden lieten zien dat de omgezette cellen actiepotentialen afvuurden en in ongeveer de helft van de gevallen excitatoire en inhiberende synaptische inputs ontvingen — kenmerken van functionele integratie in lokale netwerken.
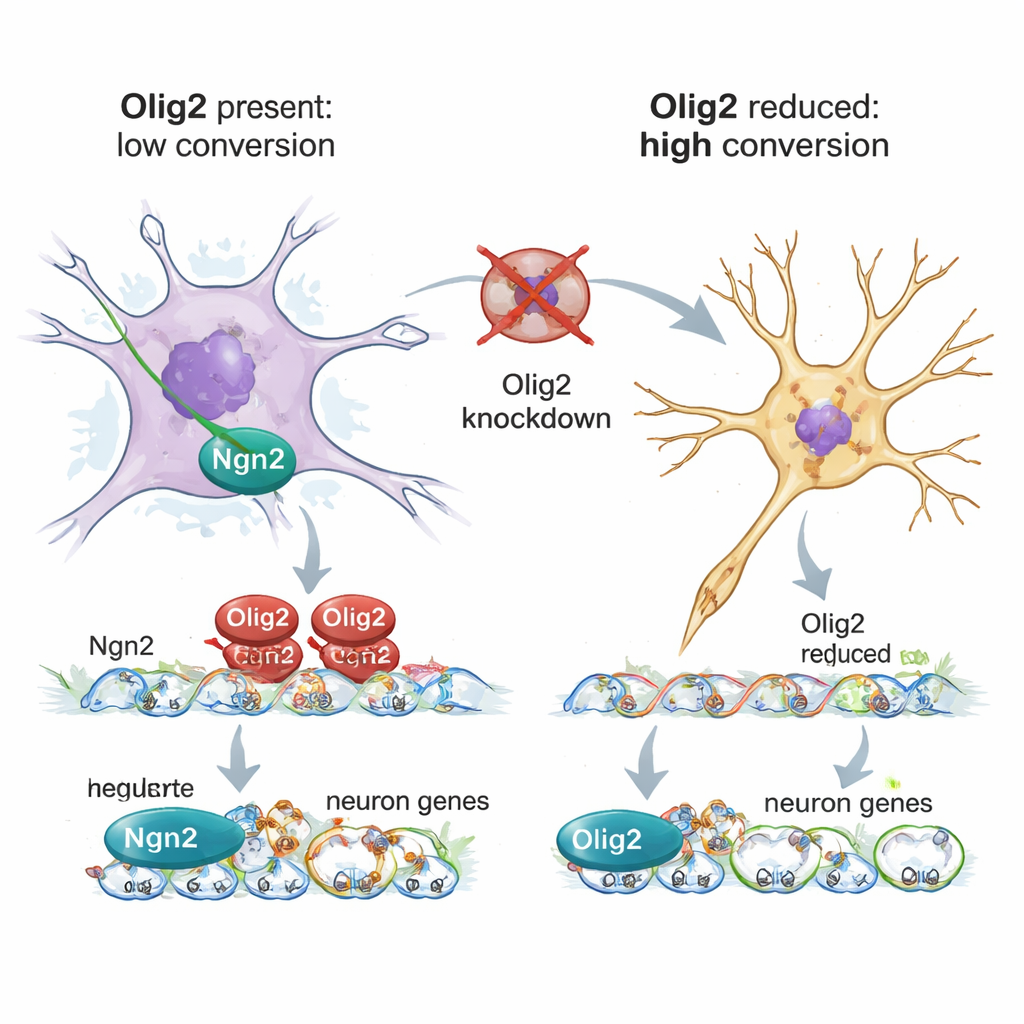
Hoe Olig2 de omschakeling naar een neuronprogramma blokkeert
Met behulp van enkel-cel RNA-sequencing profielen de auteurs duizenden individuele astrocyten die aan Ngn2 waren blootgesteld, met of zonder Olig2-knockdown. Wanneer Olig2 aanwezig was, verschoven astrocyten slechts gedeeltelijk hun genexpressie: sommige metabole en eiwitsynthese-wegen veranderden, maar kernastrocytgenen bleven actief en veel genen die betrokken zijn bij het opbouwen van neuronen bleven gedempt. Toen Olig2 werd verminderd, onderdrukten astrocyten hun rijpe ondersteuningsprogramma veel vollediger en zetten ze genen aan die geassocieerd zijn met neurale stamcellen, neurogenese en axongroei. Een aanvullende methode, CUT&Tag, kaartte waar Olig2 aan het DNA bindt in deze gereprogrammeerde astrocyten. Olig2 belandde op regulatorische regio's van veel pro-neurogene genen — waaronder Ngn2 zelf — wat overeenkomt met een rol als directe repressor die zowel de reprogrammeringsfactor tempert als neuronale genen uitschakelt.
Identiteit van cellen herschakelen door een induceerbare verdediging op te heffen
Alles bij elkaar laat het werk zien dat astrocyten een actieve, induceerbare verdediging opzetten tegen het worden van neuronen: zodra een proneurale factor zoals Ngn2 wordt ingebracht, activeert dat Olig2, dat op zijn beurt Ngn2 terughoudt en belangrijke neuronale genen blokkeert. Het uitschakelen van Olig2 lost niet alle problemen op — de conversie-efficiënties blijven beperkt — maar het verhoogt het aantal functionele nieuwe neuronen aanzienlijk en verschuift astrocytenmetabolisme en genexpressie naar een meer neuron-achtig profiel. Voor de niet-specialist is de conclusie dat succesvolle herstel van de hersenen waarschijnlijk niet alleen vereist dat men het gaspedaal indrukt met pro-neuronale factoren, maar ook dat men recent ontdekte remmen zoals Olig2 loslaat die cellen gebruiken om hun identiteit te beschermen.
Bronvermelding: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
Trefwoorden: conversie van astrocyt naar neuron, celreprogrammering, Olig2, gentherapie, neuroregeneratie