Clear Sky Science · nl
NKG2D-opregulatie maakt tumoren gevoeliger voor gecombineerde anti-PD1- en anti-VEGF-therapie en voorkomt gehoorverlies
Waarom dit onderzoek belangrijk is voor mensen met gehoorverlies
Sommige mensen erven een aandoening die NF2-gerelateerde schwannomatose wordt genoemd, waarbij goedaardige tumoren op de zenuwen van het binnenoor groeien en vaak geleidelijk tot blijvend gehoorverlies leiden. Huidige behandelingen kunnen tumoren verkleinen maar kunnen het gehoor beschadigen of na verloop van tijd hun effectiviteit verliezen. Deze studie onderzoekt een nieuwe combinatie van geneesmiddelen die niet alleen de tumorgroei in laboratoriummodellen vertraagt, maar ook helpt het gehoor te beschermen, wat wijst op zachtere en mogelijk duurzamere opties voor patiënten.
De tumoren achter de stilte begrijpen
Bij NF2-gerelateerde schwannomatose ontstaan tumoren die vestibulaire schwannomen worden genoemd op de evenwichts- en gehoorzenuw binnen de schedel. Naarmate deze tumoren groter worden, kunnen ze de fijne zenuwvezels beschadigen die geluidssignalen naar de hersenen geleiden en in ernstige gevallen op de hersenstam drukken. Chirurgie en bestraling kunnen levens redden en tumoren verwijderen of onder controle houden, maar beide brengen echte risico’s met zich mee: verslechterend gehoor, duizeligheid en verzwakking van de aangezichtszenuw. Een middel genaamd bevacizumab, dat het groeisignaal voor bloedvaten (VEGF) blokkeert, wordt soms gebruikt om deze tumoren te verkleinen en het gehoor te verbeteren, maar slechts ongeveer een derde van de patiënten profiteert en het effect neemt vaak af. Dat heeft de zoektocht aangewakkerd naar behandelingen die zowel veiliger als duurzamer zijn.
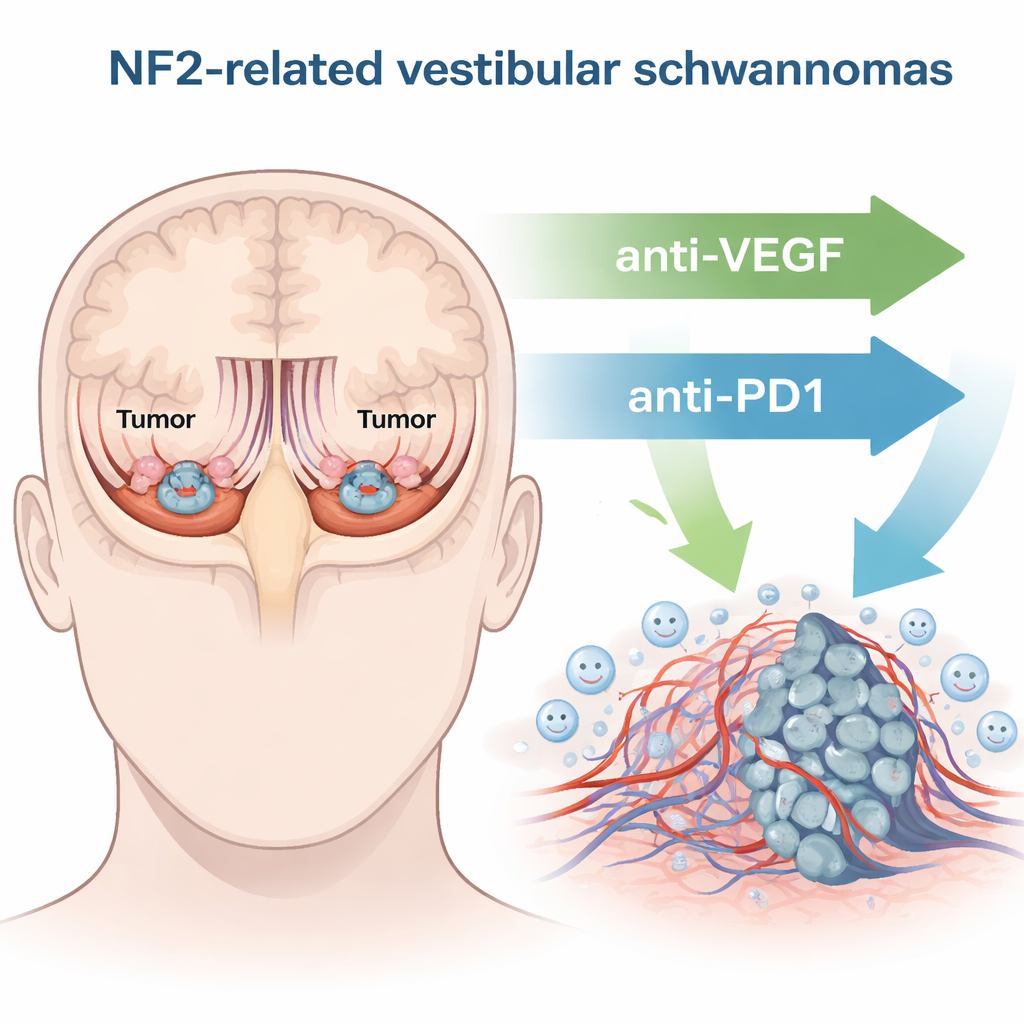
Het immuunsysteem als bondgenoot inschakelen
In het afgelopen decennium is de kankertherapie veranderd door immuuncheckpointremmers — geneesmiddelen die de “remmen” op immuuncellen loslaten zodat ze tumoren beter kunnen aanvallen. Een van die remmen, PD-1, zit op het oppervlak van immuuncellen en kan ze uitschakelen wanneer die wordt geactiveerd. De auteurs vroegen of het blokkeren van PD-1 (met een anti-PD1-antistof) het immuunsysteem zou kunnen helpen vestibulaire schwannomen onder controle te houden, en of combinatie met VEGF-blokkade nog beter zou werken. Met muismodellen die nauw aansluiten bij menselijke binnenoor- en perifere zenuwtumoren, behandelden ze dieren met alleen anti-VEGF, alleen anti-PD1, of de combinatie, en volgden daarna tumorgroei, overleving en gehoor.
Tumorbloedvaten beter laten functioneren, niet laten verdwijnen
Het team ontdekte dat anti-VEGF meer deed dan tumoren simpelweg uithongeren. Het remodelleerde hun abnormale, lekkende bloedvaten tot stabielere, beter functionerende kanalen. Onder de microscoop hadden behandelde tumoren meer vaten bedekt door ondersteunende cellen en een hoger aandeel vaten dat daadwerkelijk bloed vervoerde. Deze “normalisatie” verbeterde de levering van de anti-PD1-antistof naar de tumor en liet meer kankerbestrijdende immuuncellen — vooral CD8-T-cellen en natural killer (NK)-cellen — binnenkomen. Bij muizen die de combinatietherapie kregen, groeiden tumoren langzamer, waren er minder delende cellen en meer cellen die geprogrammeerd afstierven, en leefden de dieren langer dan bij een van beide middelen afzonderlijk.
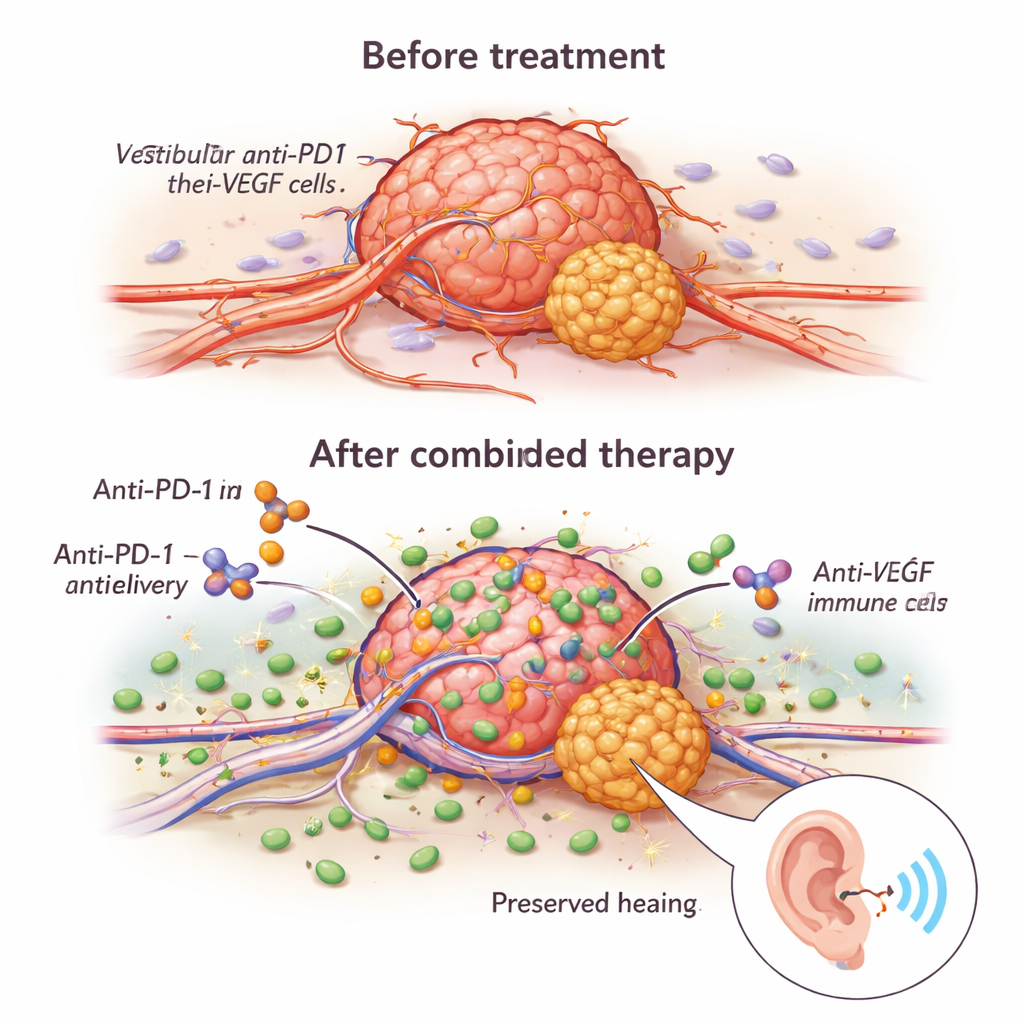
De dodelijkheid van immuuncellen opvoeren
Het voordeel van de combinatie ging verder dan alleen het binnenkrijgen van meer immuuncellen in de tumor; die cellen waren ook agressiever zodra ze arriveerden. Anti-VEGF verhoogde de aanwezigheid van moleculen zoals granzyme B en perforine, die fungeren als de moleculaire “kogels” van het immuunsysteem om gaten in tumorcellen te slaan. Een cruciale schakel in dit proces was een receptor genaamd NKG2D, aanwezig op zowel T-cellen als NK-cellen. Anti-VEGF verhoogde NKG2D en de bijbehorende moleculen op tumorcellen, waardoor immuuncellen effectievere killercellen werden in laboratoriumtests. Toen onderzoekers NKG2D blokkeerden, daalden de antitumor-effecten van de therapieën scherp, wat aantoont dat deze route centraal staat in de synergie tussen de middelen. Belangrijk is dat kleine monsters van mensentumoren die langdurig met bevacizumab waren behandeld, genactiviteitspatronen vertoonden die consistent zijn met meer geactiveerde en minder “uitgeputte” T-cellen en NK-cellen, wat suggereert dat vergelijkbare immuunversterking ook bij patiënten kan optreden.
Gehoor beschermen terwijl tumoren onder controle blijven
Een cruciale vraag was of deze immuun-gebaseerde behandelingen het gehoor zouden schaden of juist helpen. Wanneer gezonde muizen alleen anti-PD1 kregen, bleven hun gehoordrempels normaal, wat aangeeft dat het middel geen kortetermijnschade aan het gehoorsysteem lijkt te veroorzaken. Bij muizen met tumoren verbeterde anti-VEGF alleen het gehoor vergeleken met geen behandeling, wat aansluit bij klinische ervaring. Anti-PD1 alleen en de combinatie van anti-PD1 met anti-VEGF herstelden beide de gehoordrempels tot bijna normale waarden. Toen de onderzoekers een realistisch scenario nabootsten — eerst behandelen met anti-VEGF en vervolgens doorgaan, stoppen, of anti-PD1 toevoegen — vonden ze dat overschakelen naar alleen anti-PD1 de tumorgroei nog steeds kon vertragen, maar dat stoppen met anti-VEGF het gehoorvoordeel wegnam. Het handhaven van anti-VEGF en het toevoegen van anti-PD1 gaf de beste resultaten voor zowel overleving als behoud van gehoor.
Wat dit voor patiënten zou kunnen betekenen
Voor mensen met NF2-gerelateerde schwannomatose suggereert dit werk een toekomst waarin behandeling meer doet dan tumoren slechts onder controle houden — het kan ook het vermogen om te horen behouden. In zorgvuldig ontworpen muismodellen creëerde de combinatie van een VEGF-remmer met een PD-1-remmer een gunstiger omgeving voor immuuncellen, versterkte hun tumor-dodende kracht via NKG2D, en beschermde het gehoor beter dan elk middel afzonderlijk. Hoewel klinische onderzoeken nog nodig zijn om veiligheid en baten bij mensen te bevestigen, biedt de studie een duidelijk stappenplan om deze geneesmiddelcombinatie te testen als een nieuwe, mogelijk duurzamere strategie voor het behandelen van vestibulaire schwannomen en het voorkomen van gehoorverlies.
Bronvermelding: Lu, S., Yin, Z., Wu, L. et al. NKG2D upregulation sensitizes tumors to combined anti-PD1 and anti-VEGF therapy and prevents hearing loss. Nat Commun 17, 1148 (2026). https://doi.org/10.1038/s41467-026-68865-8
Trefwoorden: vestibulair schwannoom, NF2, immunotherapie, bevacizumab, behoud van gehoor