Clear Sky Science · nl
Antiparallel stapeling van Csu-pili stuurt 3D-biofilmassemblage van Acinetobacter baumannii
Hoe ziekenhuiskiemen beschutte steden bouwen
Sommige van de taaiste ziekenhuiskiemen overleven antibiotica door zich te verschuilen in slijmerige, driedimensionale gemeenschappen die biofilms worden genoemd. Deze studie stelt een eenvoudige maar cruciale vraag: hoe weven individuele bacteriën zich tot zulke sterke, gelaagde structuren? Door in te zoomen met geavanceerde elektronenmicroscopie onthulden de onderzoekers een microscopische “klittenband” van haarachtige filamenten waarmee de gevaarlijke ziekteverwekker Acinetobacter baumannii zichzelf in beschermende 3D-klonten vlecht. Inzicht in dit verborgen geraamte kan nieuwe manieren openen om biofilms uiteen te trekken en bestaande medicijnen beter te laten werken.
Piepkleine haartjes die bacteriën bij elkaar houden
A. baumannii, een belangrijke oorzaak van moeilijk behandelbare ziekenhuisinfecties, draagt dunne oppervlaktehaartjes die Csu-pili worden genoemd. Eerder werk liet zien dat deze pili essentieel zijn voor het vormen van robuuste, koepelachtige biofilms, maar niemand wist hoe ze cellen daadwerkelijk in een 3D-structuur verweven. Met verschillende vormen van elektronenmicroscopie bevestigden de auteurs eerst dat in vloeibare kweek de pili meestal afzonderlijk van elke bacterie uitsteken, als stekels aan een klit. In dicht op een oppervlak gegroeide kolonies verandert het beeld echter dramatisch: veel pili pakken zich strak bijeen en vormen brede, vlakke banden die tussen aangrenzende cellen doorlopen en een fragiel ogend maar uitgebreid driewijd netwerk creëren. 
Vlakke ladders opgebouwd uit gepaarde filamenten
Om te achterhalen hoe deze banden zich vormen, zuiverde het team Csu-pili en observeerde wat ze op zichzelf deden. Gedurende dagen tot weken begonnen enkele filamenten te paren en toen samen te smelten tot multi-filament “superstacks”, die uiteindelijk een gelachtig netwerk vormden dat sterk leek op de structuren in echte biofilms. Hoogresolutie cryo-elektronenmicroscopie onthulde het onderliggende ontwerp. Elke pilus is geen glad buisje maar een zigzaggende staaf. Wanneer twee staven naast elkaar liggen in tegengestelde richting, raken ze elkaar op herhalende hoekpunten en vormen ze stabiele laterale verbindingen. Veel van zulke antiparallelle paren kunnen dan op een rij gelegd worden tot een zeer dunne, velachtige stapel—eigenlijk een microscopische ladder of lint dat slechts één filament dik is maar veel filamenten breed.
Een ingebouwd bouwplan voor 3D-groei
De gedetailleerde structuren tonen dat dit stapelvermogen in de geometrie van de pili zelf ingebakken is. Het zigzagpatroon herhaalt zich over zeer korte afstanden en creëert vele potentiële contactpunten langs elk filament. Daardoor, zodra twee pili elkaar in de juiste oriëntatie treffen, kan een keten van verbindingen zich vormen als een rits en de plaat snel verlengen. Belangrijk is dat de richting waarin de staven gericht zijn ervoor zorgt dat contacten meestal ontstaan tussen pili van verschillende cellen, niet van dezelfde, wat cel‑celverbindingen van nature bevordert. De stapels blijven flexibel en rekbaar, zodat de groeiende biofilm fysieke stress kan absorberen zonder uit elkaar te vallen. De onderzoekers zagen dat tijdens celdeling nieuwe dochtercellen vaak hun pili gezichts‑tegen‑gezicht krijgen gepositioneerd, wat stapelvorming precies daar stimuleert waar nodig om cellen tot een 3D-cluster te binden. 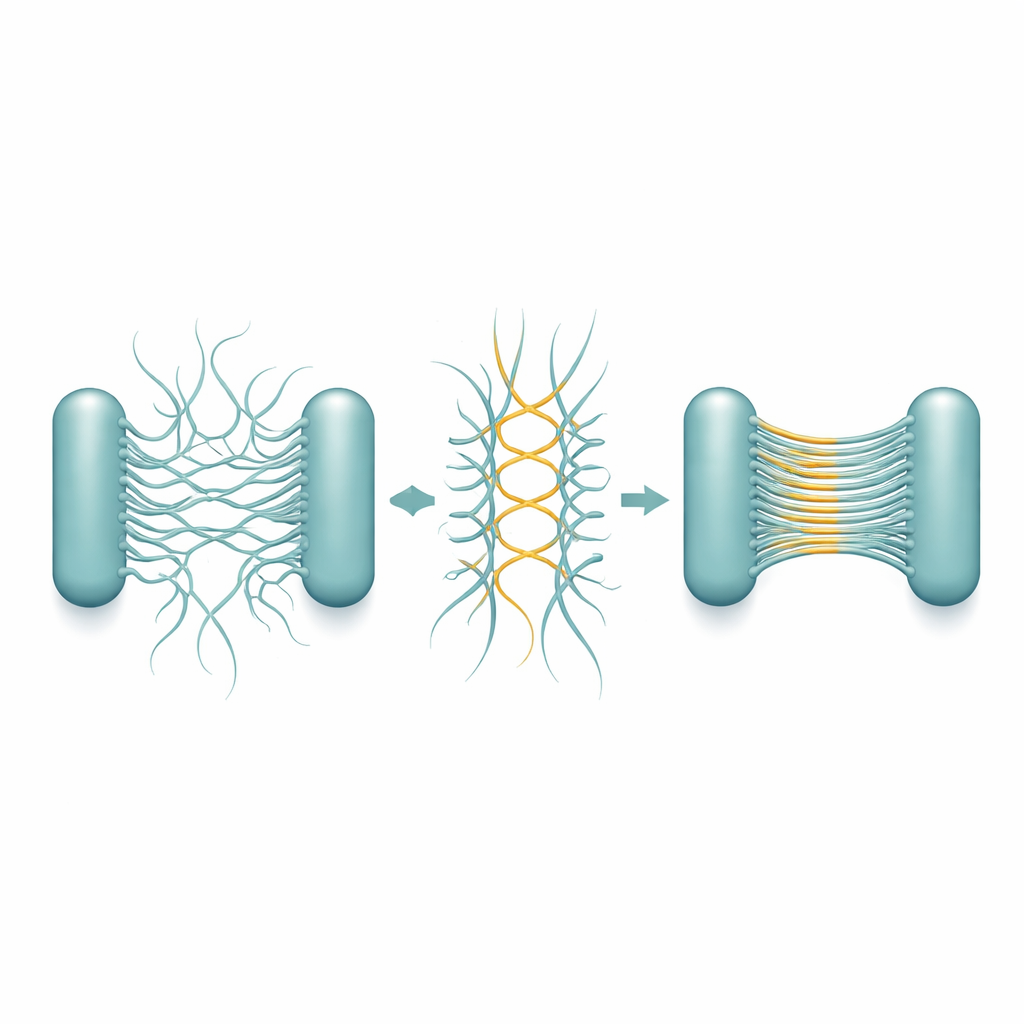
Lijm, vulling en vroeg geraamte
De studie onderzocht ook hoe andere componenten van de biofilm bijdragen. Een suikerachtig polymeer genaamd PNAG en los DNA van gebroken cellen hopen zich op in rijpe biofilms. Microscopie toonde deze stoffen die de smalle openingen tussen bacteriën vullen en zich om de pilusstapels wikkelen, veel zoals beton dat rond stalen wapening wordt gegoten. Toch vormden bacteriën nog steeds georganiseerde vlotten die alleen door Csu-pilusstapels bij elkaar werden gehouden toen het team PNAG en DNA verwijderde. Dit toont aan dat de pili het primaire geraamte bouwen, terwijl het omringende materiaal later het geheel cement en stabiliseert.
Nieuwe zwakke plekken in bacteriële forten
In eenvoudige bewoordingen legt dit werk uit hoe A. baumannii zijn oppervlaktehaartjes gebruikt om zich in sterke, meerlagige klonten te vlechten waar geneesmiddelen en immuuncellen moeite mee hebben door te dringen. De pili werken eerst als haken om zich aan oppervlakken vast te grijpen en vervolgens als flexibele banden die zich opstapelen tot platte vellen, waardoor naburige cellen in alle richtingen met elkaar verbonden worden. Suikerpolymeren en DNA vullen daarna de openingen op en veranderen dit bandennetwerk in een solide vesting. Door precies aan te wijzen hoe pili aan elkaar kleven, benadrukt de studie een nieuw doelwit: medicijnen of moleculen die pilus‑piluscontacten blokkeren kunnen het biofilmgeraamte van binnenuit verzwakken, waardoor hardnekkige bacteriële infecties gemakkelijker op te ruimen zijn.
Bronvermelding: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Trefwoorden: biofilms, Acinetobacter baumannii, pili, antibioticaresistentie, cryo-elektronenmicroscopie