Clear Sky Science · nl
Verbeterde methaanchloring via RuO2-gasconvectie-elektrode met in situ gegenereerde dynamische driefasengrenzen
Een alledaags gas omzetten in nuttige producten
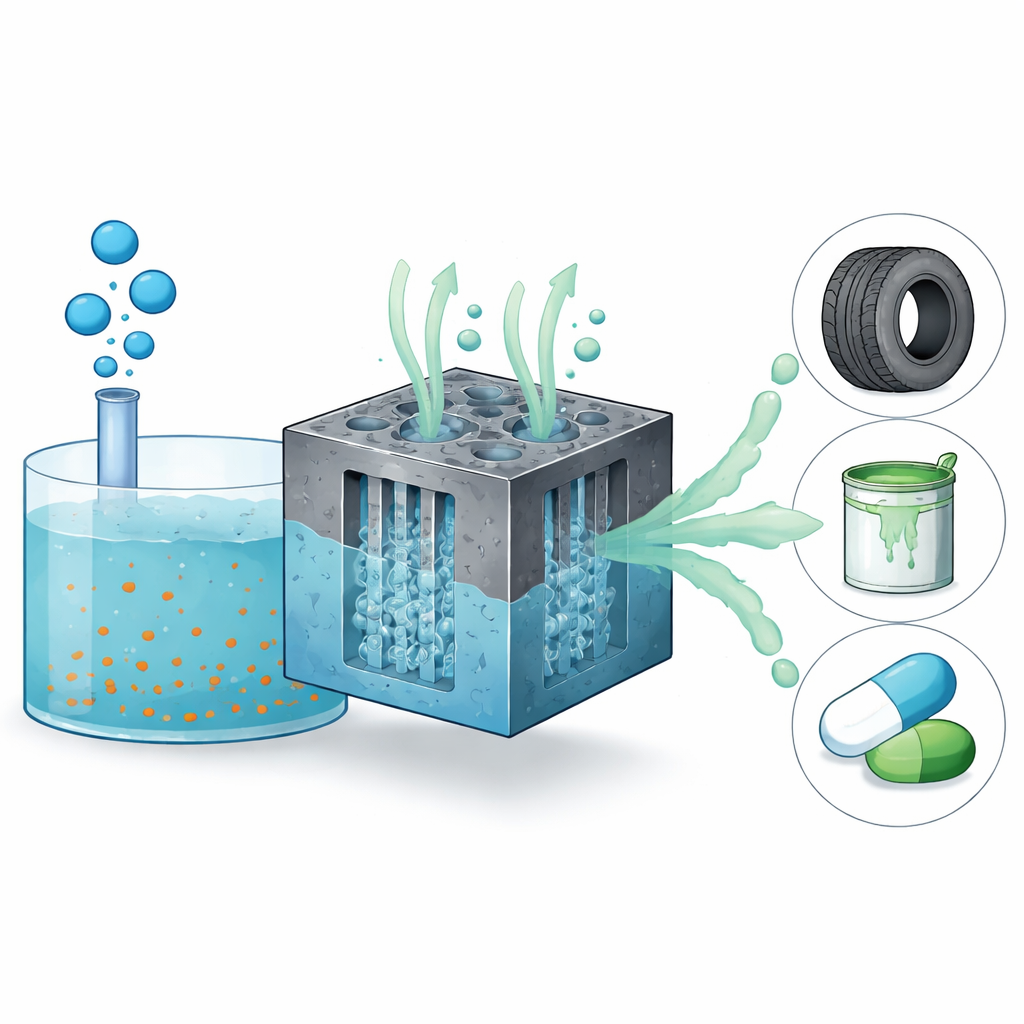
Methaan wordt vaak besproken als een problematisch broeikasgas, maar het is ook een rijke grondstof die kan worden omgezet in alledaagse producten zoals rubber, verf en geneesmiddelen. Een belangrijke stap in die keten is tegenwoordig het maken van chlormethaan, een basisingrediënt voor veel industriële chemicaliën. Het probleem is dat de gangbare productieroute heet, energie-intensief is en afhankelijk van relatief dure grondstoffen. Deze studie onderzoekt een koelere, schonere manier om methaan en zout water met elektriciteit en een speciaal ontworpen elektrode om te zetten in chlormethaan, wat de industrie mogelijk kan helpen zowel de uitstoot als het energieverbruik te verminderen.
Waarom de productie van chlormethaan heroverwogen moet worden
Chlormethaan is een werkpaardmolecuul in de chemische productie, vooral voor de vervaardiging van organosiliciumverbindingen die worden gebruikt in kit, coatings en andere materialen, maar ook voor producten in de rubber-, verf- en farmaceutische industrie. De vraag groeit tot miljoenen tonnen per jaar, met name in China. Vandaag de dag wordt het voornamelijk geproduceerd door methanol te laten reageren met waterstofchloride bij hoge temperaturen en drukken. Dat proces verbruikt veel energie, is afhankelijk van methanol waarvan de prijs sterk kan schommelen, en omvat bijtende chemicaliën die apparatuur aantasten. Een duurzamere route zou gebruikmaken van overvloedig aanwezig methaan direct, plus mildere chloorbronnen zoals zout afvalwater, en bij benadering kamertemperatuur kunnen werken.
De uitdaging van het temmen van een inert gas
Het direct gebruiken van methaan is niet eenvoudig. De sterk gebonden waterstofatomen maken het tot een van de moeilijkst te activeren moleculen, wat normaal gesproken temperaturen van enkele honderden graden Celsius vereist. In vloeistofgebaseerde systemen is er een extra obstakel: methaan lost nauwelijks op in water, dus bereikt slechts een kleine hoeveelheid op elk moment het katalysatoroppervlak. Eerdere lichtgestuurde en elektrisch aangedreven benaderingen konden wel chlormethaan maken, maar de productiesnelheden waren bescheiden en de katalysatoren degradeerden vaak. De centrale vraag die de auteurs aanpakken is hoe je zowel methaan efficiënt kunt activeren als een constante aanvoer ervan in contact kunt houden met reactieve chloorspecies bij omgevingscondities.
Een nieuwe elektrode die gas en vloeistof op verzoek mengt
De onderzoekers combineerden twee vorderingen: een katalysator die uitblinkt in het vormen van reactief chloor op zijn oppervlak, en een elektrode-ontwerp dat gas en vloeistof dwingt om te vermengen waar die katalysator zich bevindt. Ze gebruikten rutheniumoxide, een bekend industrieel materiaal voor chloorproducerende reacties, om oppervlaksgebonden chloorspecies te creëren die waterstof van methaan kunnen afsplitsen en chlormethaan kunnen vormen. In plaats van een standaard gasdiffusie-elektrode, waarbij methaan eenvoudig door een dunne laag sijpelt en langzaam oplost, bouwden ze een driedimensionale gasconvectie-elektrode. In dit ontwerp stromen methaangas en zoutvloeistof in verschillende richtingen door een poreus koolstofschuim dat is bedekt met katalysator en een dun hydrofiel laagje. Drukverschillen zorgen ervoor dat gas en vloeistof herhaaldelijk in de poriën binnendringen, waardoor continu nieuwe contactzones tussen gas, vloeistof en vaste stof ontstaan.

Hoe het nieuwe ontwerp de productie verhoogt
Computervloeisimulaties en massatransportmodellering tonen aan dat deze gasconvectie-elektrode dynamische, volume-vullende driefasengrenzen creëert in plaats van slechts een dunne reactielaag. Kolkende stromingen en belletjes vernieuwen voortdurend het gas–vloeistofoppervlak, waardoor de methaanconcentraties nabij de katalysator dicht bij hun fysische limiet blijven in plaats van met de afstand af te nemen. Elektrochemische tests bevestigen het voordeel: vergeleken met een conventionele gasdiffusie-elektrode met dezelfde katalysator verhoogt het nieuwe systeem de chlormethaanproductie per elektrode-oppervlak met ongeveer negentien keer en behoudt het een hoge selectiviteit voor het gewenste product. Het onderdrukt ook een concurrerende nevenreactie die simpelweg chloorgas vormt, waardoor de efficiëntie waarmee elektrische stroom in nuttige chemische bindingen wordt omgezet verbetert. De opstelling draait stabiel gedurende ten minste vijftien uur met weinig katalysatorverlies, en het opschalen van de katalysatorbelasting verhoogt de opbrengst verder.
Wat dit voor de industrie en het milieu kan betekenen
Voor niet‑specialisten is de belangrijkste conclusie dat het team een soort "mini‑chemische fabriek" heeft gebouwd waarin gas en vloeistof door een poreus blok worden gestuurd zodat ze veel effectiever vergaderen en reageren dan voorheen. Door deze slimme stromingscontrole te combineren met een robuuste katalysator, tonen ze aan dat chlormethaan geproduceerd kan worden uit methaan en zoute oplossingen bij kamertemperatuur met indrukwekkende snelheden en efficiëntie. Hoewel er meer engineeringwerk nodig is voordat deze aanpak volledige industriële schaal bereikt, wijst het op een veelbelovende manier om methaanemissies en hypersaline afvalwaterstromen om te zetten in een waardevolle chemische grondstof, mogelijk met lagere energiebehoefte, minder apparatuurcorrosie en een kleinere milieu-impact in één stap.
Bronvermelding: Fu, Z., Zhou, Y., Cao, Z. et al. Enhanced methane chlorination via RuO2-gas convection electrode with in-situ generated dynamical three-phase boundaries. Nat Commun 17, 2221 (2026). https://doi.org/10.1038/s41467-026-68845-y
Trefwoorden: methaanconversie, chlormethaan, elektrocatalyse, gasconvectie-elektrode, hergebruik van zout afvalwater