Clear Sky Science · nl
Vernietiging van de negatieve elektrode door tweefasige zinkaanslag en het herstel ervan in zinkbatterijen
Waarom zinkbatterijen ertoe doen in het dagelijks leven
Het veilig en goedkoop opslaan van elektriciteit is essentieel voor alles, van het ondersteunen van zonnepanelen bij een woning tot het stabiliseren van het elektriciteitsnet. Zink‑metalen batterijen zijn aantrekkelijke kandidaten: zink is overvloedig, niet‑toxisch en werkt in waterige elektrolyten die veel veiliger zijn dan de ontvlambare vloeistoffen in veel lithiumbatterijen. Toch verliezen deze veelbelovende batterijen nog te snel capaciteit en volgen er kortsluitingen. Dit artikel onthult een verborgen tweestaps‑groeiproces op de zinkelektrode dat deze schade veroorzaakt, en presenteert een chemische ‘zelfherstellende’ strategie die de batterijen veel langer laat werken.
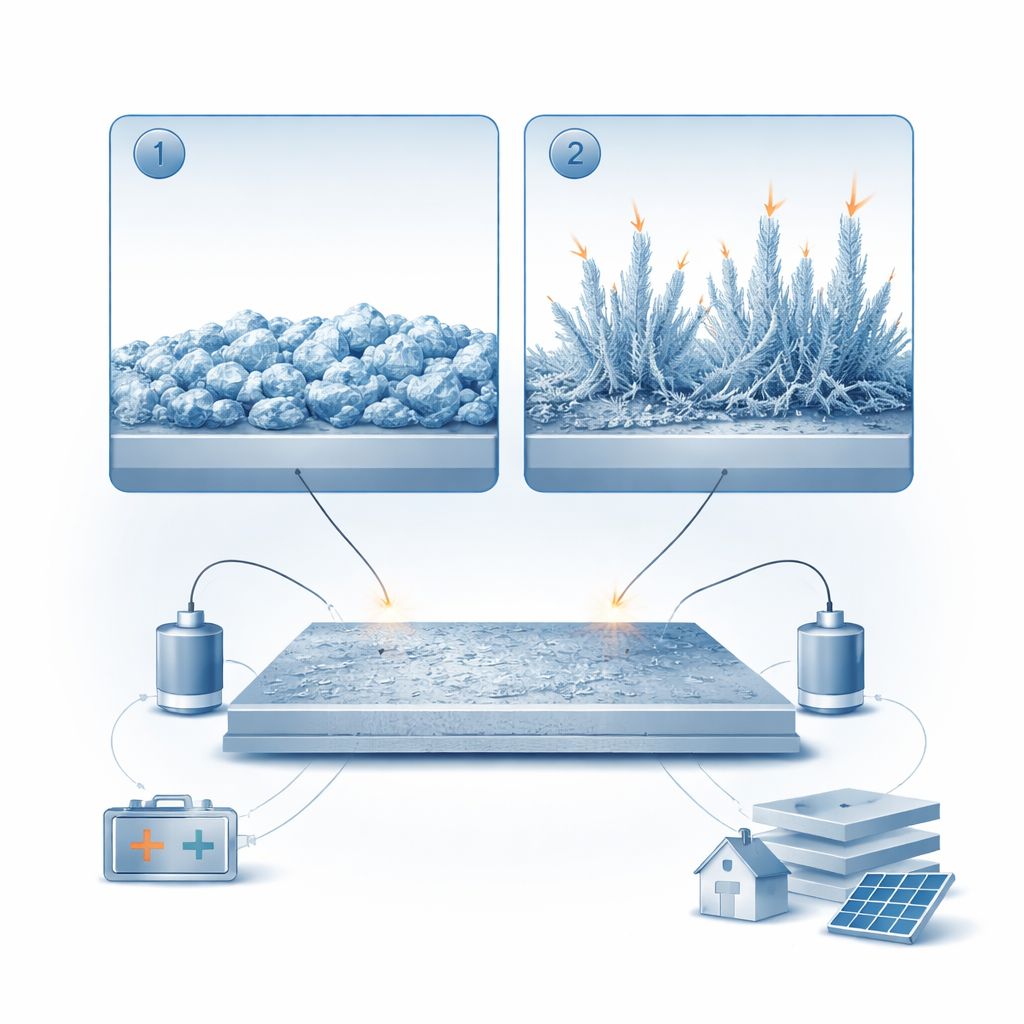
Van glad metaal naar zink “mos”
De negatieve elektrode in deze batterijen bestaat uit zinkmetaal, dat tijdens het laden en ontladen herhaaldelijk geplaatsts (zink toevoegt) en gestript wordt (zink verwijdert). Met behulp van een transparante cel met microscoop keken de onderzoekers hoe zink zich in de loop van de tijd op een metalen oppervlak ophoopt. Ze ontdekten dat zink niet op één manier groeit, maar in twee duidelijke fasen. Eerst vormt het relatief dichte, klonterige kristallen die een glanzende, compacte laag maken. Daarna, naarmate het aanslagproces doorgaat, ontspruiten dunne, filamentachtige structuren vanaf scherpe randen en punten. Deze tweede, ‘mossige’ zinkfase vult de ruimte tussen de elektroden en sluit ze uiteindelijk met elkaar aan, wat interne kortsluitingen in de hand kan werken.
Hoe mossig zink verandert in dood zink
Het team combineerde directe beeldvorming, elektronenmicroscopie en computersimulaties om te begrijpen waarom deze mossige laag verschijnt. De scherpe uitsteeksels op het klonterige zink concentreren het elektrische veld—een effect vergelijkbaar met wat bliksemafleiders doen bij elektrische ontlading. Die concentratie trekt meer zinkionen naar de punten, wat snelle, snorhaarachtige groei voedt. Tijdens het omgekeerde proces, wanneer zink wordt gestript, lossen de mossige filamenten het eerst op en kunnen ze het elektrische contact met het onderliggende metaal verliezen. Wat overblijft is ‘dood’ zink: kleine, elektrisch geïsoleerde stukjes die niet langer deelnemen aan de batterijreactie maar nog steeds waardevol actief materiaal bevatten, wat leidt tot capaciteitsverlies en ruwe, onstabiele oppervlakken.
Een slimmer elektrolyt ontwerpen
Geleerd dat mossige groei voortkomt uit lokale ionenopbouw bij uitstekende plekken, ontwierpen de onderzoekers een elektrolytadditief dat zowel de vorming van mossig zink als het verspilde dode zink tegengaat. Ze gebruikten een zout genaamd acetylcholinejodide, dat positieve organische kationen en jodideanonen in hetzelfde molecuul levert. Volgens gevoelige massameting en infraroodspectroscopie adsorberen de kationen sterk en selectief op het zinkoppervlak en vormen ze een dun positief geladen laag die de zink‑ionflux egaliseert. Dit bevordert gladde, vlakke zinkaanslag in plaats van filamentgroei, waardoor het oppervlak compact blijft en beter bestand is tegen corrosie en waterstofgasvorming.
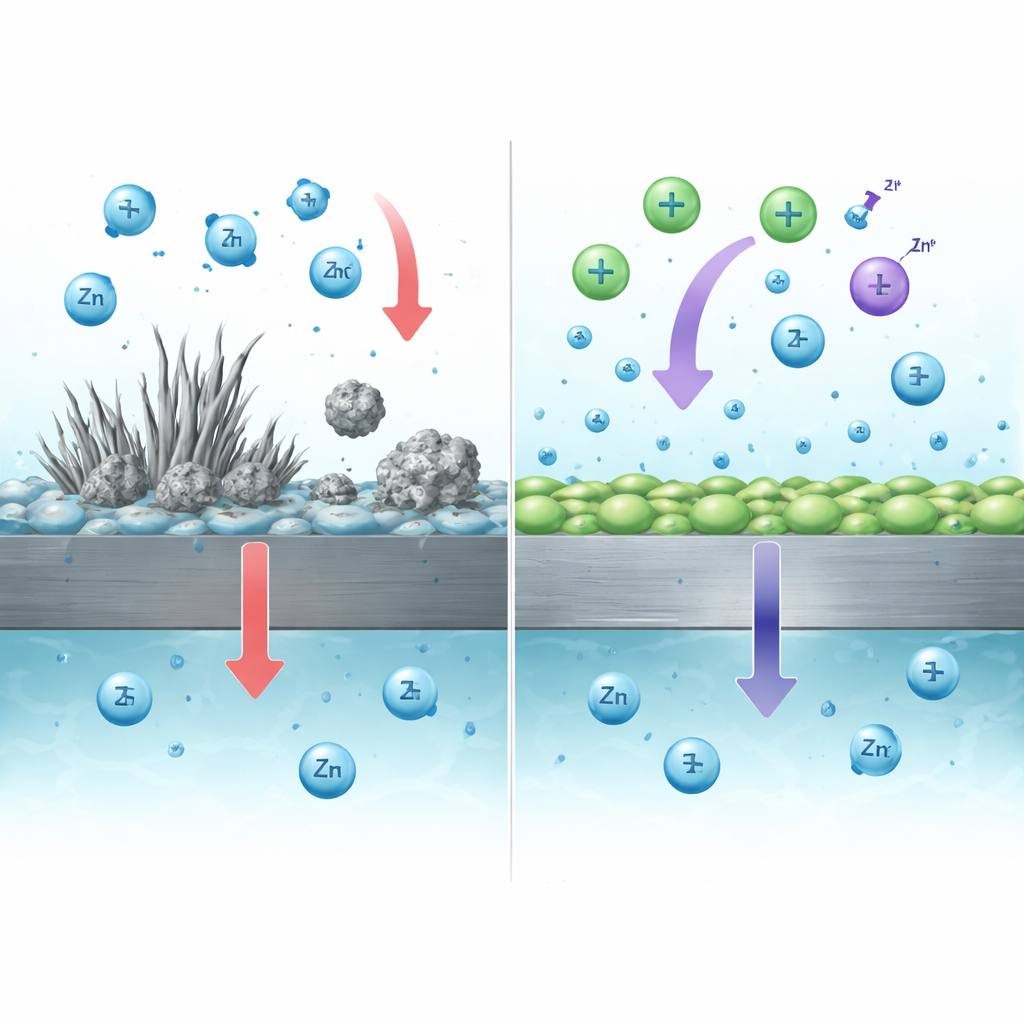
Verloren zink herstellen om de levensduur te verlengen
Het jodidegedeelte van het additief speelt een andere maar aanvullende rol. Tijdens het opladen wordt jodide gedeeltelijk omgezet in een milde oxiderende soort (I3−) die kan reageren met dode zinkdeeltjes en met isolerende zinkhoudende bijproducten die op het oppervlak ontstaan. Deze reacties zetten elektrisch geïsoleerd zink om in opgeloste zinkionen, die vervolgens in volgende cycli weer op de elektrode aangroeien. Experimenten toonden aan dat dood zink dat in een jodiumhoudende oplossing werd ondergedompeld bijna theoretisch volledig oploste, en volledige cellen met het duale‑ionadditief meer lading herwonnen dan mogelijk zou zijn uit vers geplaatsts zink alleen—duidelijke aanwijzing dat eerder verloren zink in de batterij werd ‘gerecycled’.
Wat dit betekent voor echte batterijen
Door veld‑egaliserende kationen te combineren met een zink‑recyclerend anion, stelde de nieuwe elektrolyt zinkelektroden in staat een gemiddelde Coulomb‑efficiëntie van ongeveer 99,7% te bereiken en een stabiele werking van meer dan 1400 uur bij hoge stroom en capaciteit—condities relevant voor netopslag op schaal. Symmetrische zinkcellen en praktische zink‑jodium pouch‑cellen behielden lage spanningsverliezen en behielden meer dan 96% van hun capaciteit na honderden tot tienduizenden cycli, afhankelijk van de test. Voor de niet‑specialist is de kernboodschap dat de onderzoekers precies hebben vastgesteld hoe zinkelektroden degraderen—via een tweefasige mossige groei die dood metaal produceert—en hebben aangetoond welk chemisch recept zowel deze schadelijke structuur voorkomt als verloren materiaal herstelt. Deze dubbele aanpak brengt veilige, waterige zinkbatterijen veel dichter bij langdurig, grootschalig gebruik in woningen en netwerken.
Bronvermelding: Gan, H., Liu, D., Zhang, Y. et al. Negative electrode degradation induced by two-stage zinc plating and its recovery in zinc batteries. Nat Commun 17, 2067 (2026). https://doi.org/10.1038/s41467-026-68844-z
Trefwoorden: zinkmetalen batterijen, elektrode‑degradatie, mossig zink, elektrolytadditieven, netopslag van energie