Clear Sky Science · nl
cGAS-IFN-I-responsen door extractie van nucleair DNA uit stervende cellen via nucleocytose
Hoe ons immuunsysteem DNA van doden leest
Wanneer onze cellen afsterven tijdens infecties, kanker of door gewone slijtage, moeten hun resten worden opgeruimd zonder te veel ontsteking te veroorzaken. Dit artikel onthult een verrassende manier waarop immuuncellen zich daadwerkelijk een weg kunnen banen naar de kernen van stervende cellen, hun DNA naar buiten trekken en dat gebruiken als een alarmsignaal. Inzicht in dit verborgen opruim‑en‑waarschuwingssysteem kan veranderen hoe we denken over antivirale middelen, auto‑immuniteit, kankertherapie en bijwerkingen van geneesmiddelen.
Een verborgen DNA‑alarm binnen immuuncellen
Onze cellen bevatten een sensor genaamd cGAS die DNA detecteert dat op de verkeerde plaats voorkomt—drijvend in het celvocht in plaats van veilig verpakt in de kern of mitochondriën. Wanneer cGAS dergelijk DNA aantreft, zet het een krachtig alarmprogramma in gang dat type I interferonen produceert, belangrijke antivirale en immuunregulerende eiwitten. Wetenschappers wisten dat virussen hun genetisch materiaal in cellen kunnen brengen om deze route te activeren, en dat fragmenten van ons eigen DNA soms lekken en auto‑immuunziekten kunnen veroorzaken. Maar er bleef een fundamenteel raadsel: hoe bereikt grote hoeveelheden van ons eigen DNA, vooral uit dode cellen, ooit cGAS zonder simpelweg te worden afgebroken in cellulair ‘maagzuur’—de lysosomen?
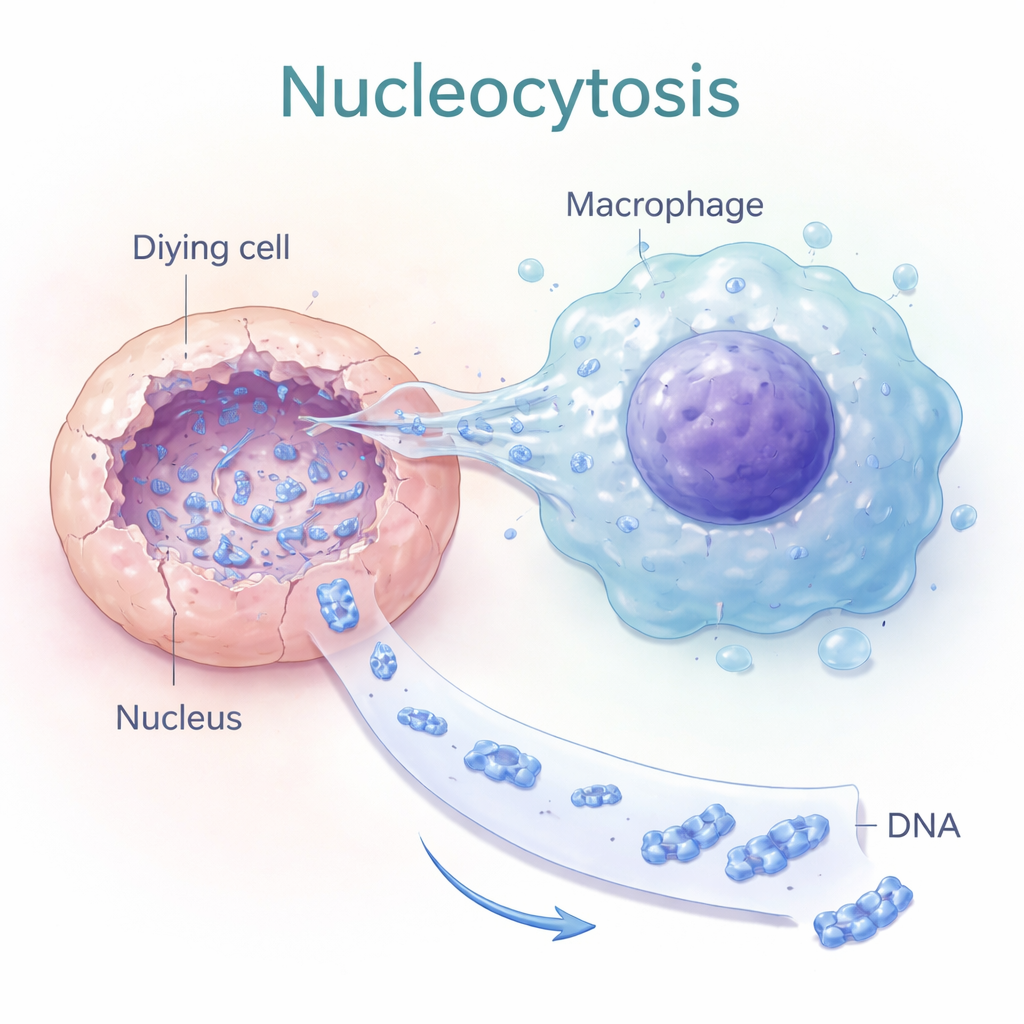
Nucleocytose: tunnelen in de kernen van dode cellen
De auteurs ontdekten een proces dat ze “nucleocytose” noemen, waarbij bepaalde macrofagen—immuuncellen die normaal gesproken puin insluiten—iets veel gerichter doen. In plaats van een volledige dode cel te verslinden, strekken ze dunne, vingerachtige uitsteeksels direct in de kern van de stervende cel. Live‑celbeeldvorming toonde dat de DNA‑intensiteit in de kern van de dode cel afnam terwijl die in de aangrenzende macrofaag toenam, wat wijst op actieve extractie van nucleair DNA. Dit transport was afhankelijk van het cellulaire geraamte (actine) en van signaalmoleculen die de celvorm regelen, wat suggereert dat nucleocytose een doelbewuste mechanische handeling is, niet een passief lek.
Wanneer antivirale geneesmiddelen het DNA‑alarm inschakelen
Tijdens de COVID‑19‑pandemie werden middelen zoals hydroxychloroquine veel getest als antivirale middelen, maar hun precieze effecten in het lichaam bleven onduidelijk. De onderzoekers vonden dat hydroxychloroquine en meerdere verwante “cationische amfifiele” middelen de cGAS–STING–interferonroute sterk kunnen activeren—maar slechts in een subset van macrofagen. Deze middelen verstoren lysosomen door hun pH te verhogen en door een enzym genaamd PPT1 te blokkeren, dat helpt bij het afbreken van vetachtige labels op eiwitten. Het gecombineerde effect duwt sommige cellen in een bijzondere vorm van celdood waarbij een eiwit genaamd calreticuline zich ophoopt in de kern. Macrofagen richten dan bij voorkeur protrusies naar deze calreticuline‑rijke kernen, extraheren DNA via nucleocytose en veroorzaken intense interferonproductie in slechts een paar cellen—genoeg om een sterk lokaal antiviraal signaal te creëren zonder het hele lichaam te overspoelen.
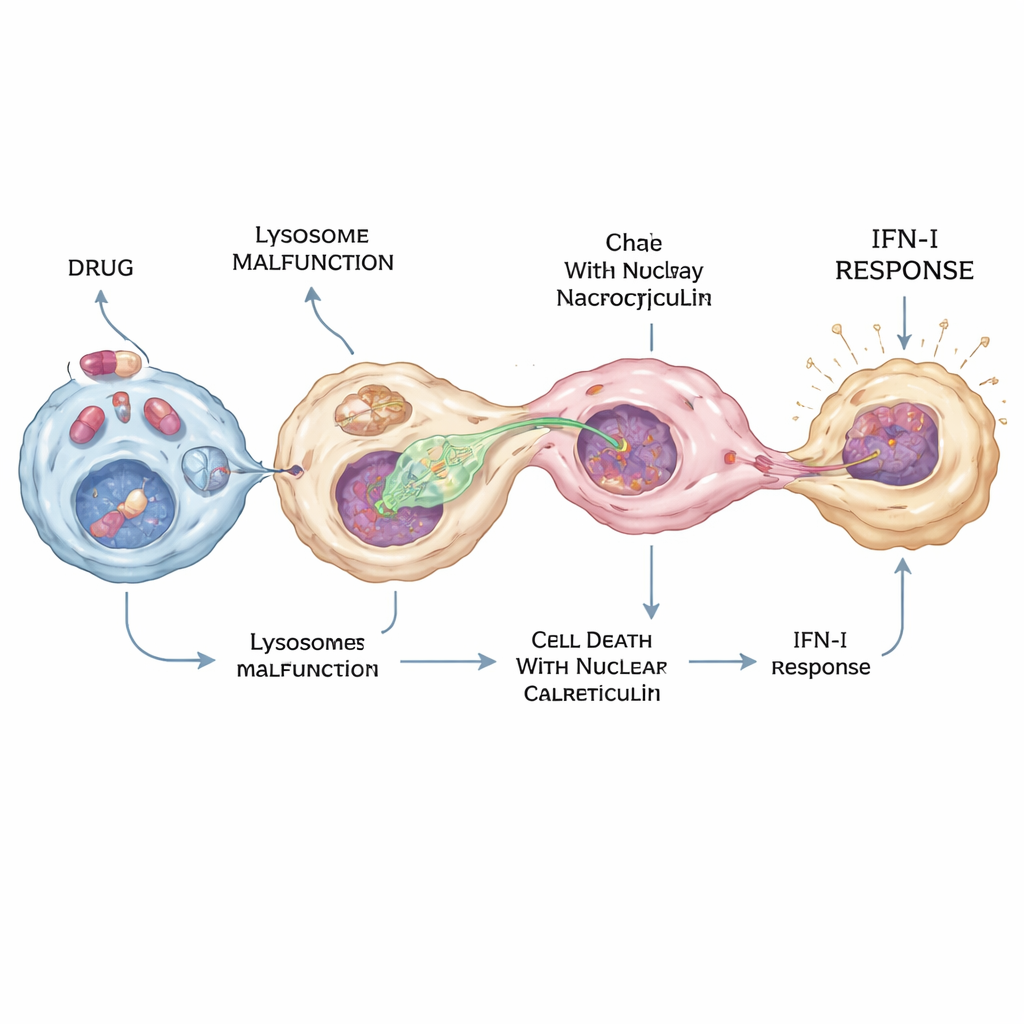
Van lokale verdediging naar ziekte en bijwerkingen
Door zowel cellulaire kweekmodellen als longen van muizen te bestuderen, toonden de onderzoekers aan dat medicijnbehandelde macrofagen een STING‑afhankelijke interferonrespons kunnen ontketenen die grotendeels lokaal blijft—bijvoorbeeld in de long—en niet systemisch wordt. Dit helpt verklaren waarom middelen zoals hydroxychloroquine antivirale of anti‑tumorvoordelen in sommige weefsels kunnen laten zien, maar ook waarom ze bij langdurig gebruik orgaanspecifieke bijwerkingen kunnen veroorzaken, zoals oog‑ of harttoxiteit. Hetzelfde nucleocytoseproces zou plausibel kunnen bijdragen aan auto‑immuun‑ of ontstekingsziekten wanneer dode cellen en lysosomale stress samenvallen, omdat het een directe route biedt voor eigen DNA om het cGAS‑alarm te activeren.
Waarom dit belangrijk is voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat immuuncellen niet alleen passief dode cellen opeten; ze kunnen actief hun kernen ontginnen op zoek naar DNA en dat gebruiken als signaal om hulp te roepen. Deze nucleocytoseroute verklaart hoe ons eigen DNA krachtige antivirale verdedigingsmechanismen op een gefocuste, lokale manier kan activeren, terwijl het ook benadrukt hoe middelen die lysosomen of PPT1 verstoren deze schakel onbedoeld kunnen omzetten. Door te leren nucleocytose opwaarts of neerwaarts te sturen—hetzij door slimmere antivirale en kankertherapieën te ontwerpen, hetzij door ongewenste zelf‑DNA‑signalen bij auto‑immuunziekten te vermijden—hopen onderzoekers dit nieuw ontdekte mechanisme te benutten voor veiligere en preciezere behandelingen.
Bronvermelding: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Trefwoorden: nucleocytose, cGAS-STING, hydroxychloroquine, type I interferon, macrofagen