Clear Sky Science · nl
Priming versus propagating: verschillende immuuneffecten van alfa- versus bèta-deeltjesuitstralende radiofarmaca wanneer gecombineerd met remming van immuuncheckpoints bij muizen
Straling omvormen tot een immuunbondgenoot
Oncologen proberen steeds vaker het immuunsysteem in te schakelen om tumoren te bestrijden, maar veel kankers negeren of weerstaan deze middelen nog steeds. Deze studie stelt een actuele vraag: kunnen verschillende typen gerichte straling niet alleen tumoren direct verkleinen, maar ook het immuunsysteem trainen om beter te reageren — en verandert de keuze van het radioactieve middel de manier waarop dat ‘coachen’ werkt?
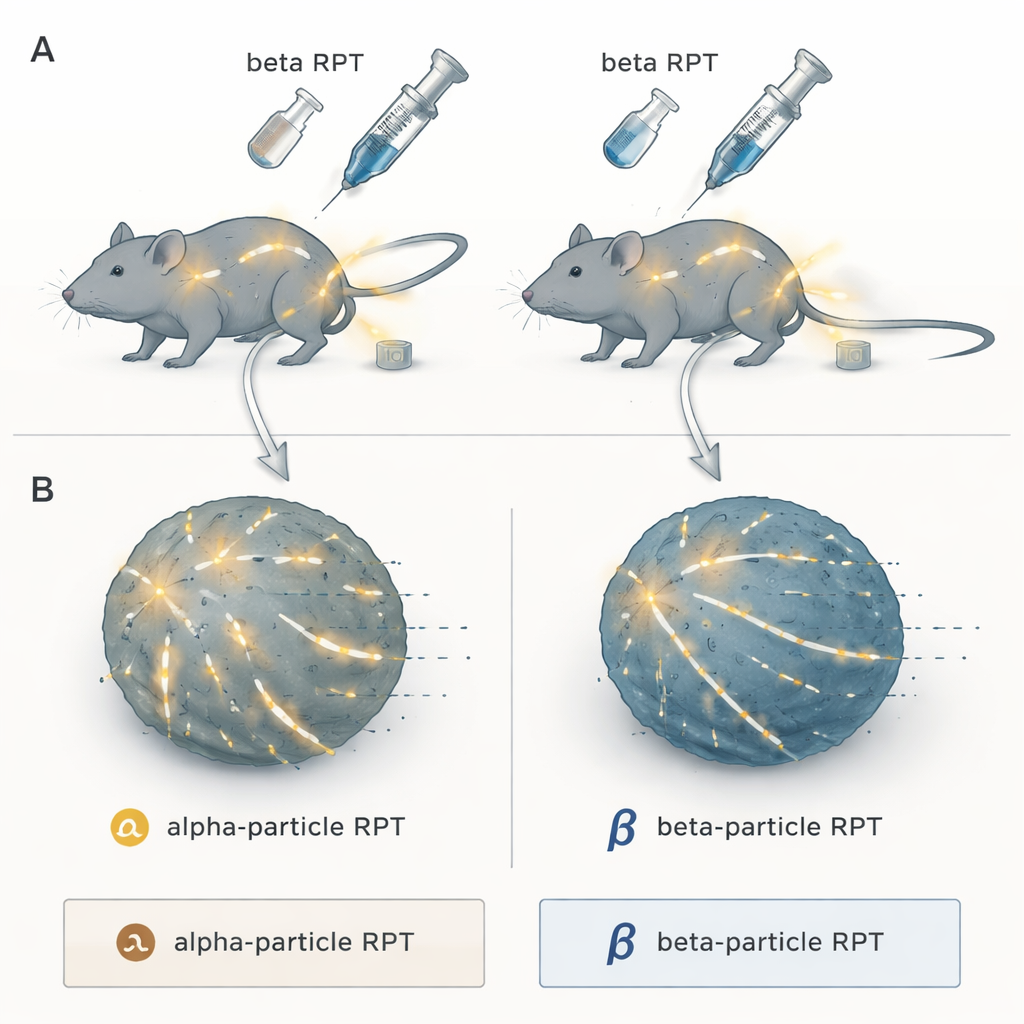
Twee varianten van precisiestraling
De onderzoekers richtten zich op radiofarmaceutische therapie, een ‘zoek‑en‑vernietig’ benadering waarbij een radioactieve lading wordt gekoppeld aan een molecuul dat van nature naar tumoren trekt. Na injectie circuleert het door het lichaam en levert straling af aan kankervlekken waar ze zich ook verbergen, iets wat gewone externe bundelstraling bij wijdverspreide ziekte moeilijker kan bereiken. Het team vergeleek twee hoofdgroepen: alfa‑deeltjesuitzenders, die extreem geconcentreerde energie in zeer korte afstanden afgeven, en bèta‑deeltjesuitzenders, die minder dichte straling uitzenden die verder door weefsel reist. Allebei waren gekoppeld aan hetzelfde tumorzoekende verbinding NM600, zodat alleen het type straling — niet de targeting — verschilde.
Straling gecombineerd met remmers van immuuncheckpoints
Op zichzelf kunnen checkpointremmers zoals anti‑PD‑L1 en anti‑CTLA4 de rem op immuuncellen opheffen, maar ze werken het best wanneer de tumor al zichtbaar is voor het immuunsysteem. In muismodellen van melanoom, prostaatkanker en colorectale kanker gaven de wetenschappers een zorgvuldig gekozen lage stralingsdosis van ofwel alfa‑ ofwel bèta‑gebonden NM600, met of zonder een combinatie van checkpointremmers. Ze varieerden ook het tijdstip waarop de immuunmiddelen werden gegeven — vooraf, kort daarna of flink later — om te zien hoe timing uitpakte voor uitkomsten zoals tumorgroei, overleving en langetermijn immuungeheugen.
Wanneer bèta‑straling uitblinkt: versterken van een bestaande respons
In een ‘immuun‑hete’ colorectale kankermodel dat al reageert op immunotherapie, kwamen de beste resultaten van bèta‑uitzendend NM600, vooral wanneer de immuunmiddelen vroeg of op een tussentijds tijdstip werden gestart. Tumoren krompen meer, muizen leefden langer en genezen dieren verwierpen vaak dezelfde kanker wanneer die maanden later opnieuw werd ingebracht. Gedetailleerde immuunprofilering toonde dat bèta‑gebaseerde behandeling plus checkpointblokkade niet zozeer een nieuwe respons creëerde als wel een bestaande versterkte: reeds aanwezige tumorspecifieke cytotoxische T‑cellen breidden zich uit, raakten actiever en produceerden meer aanvalssignalen. Kortom: bèta‑uitzenders blinken uit in het propagateren van een lopende immuunrespons.
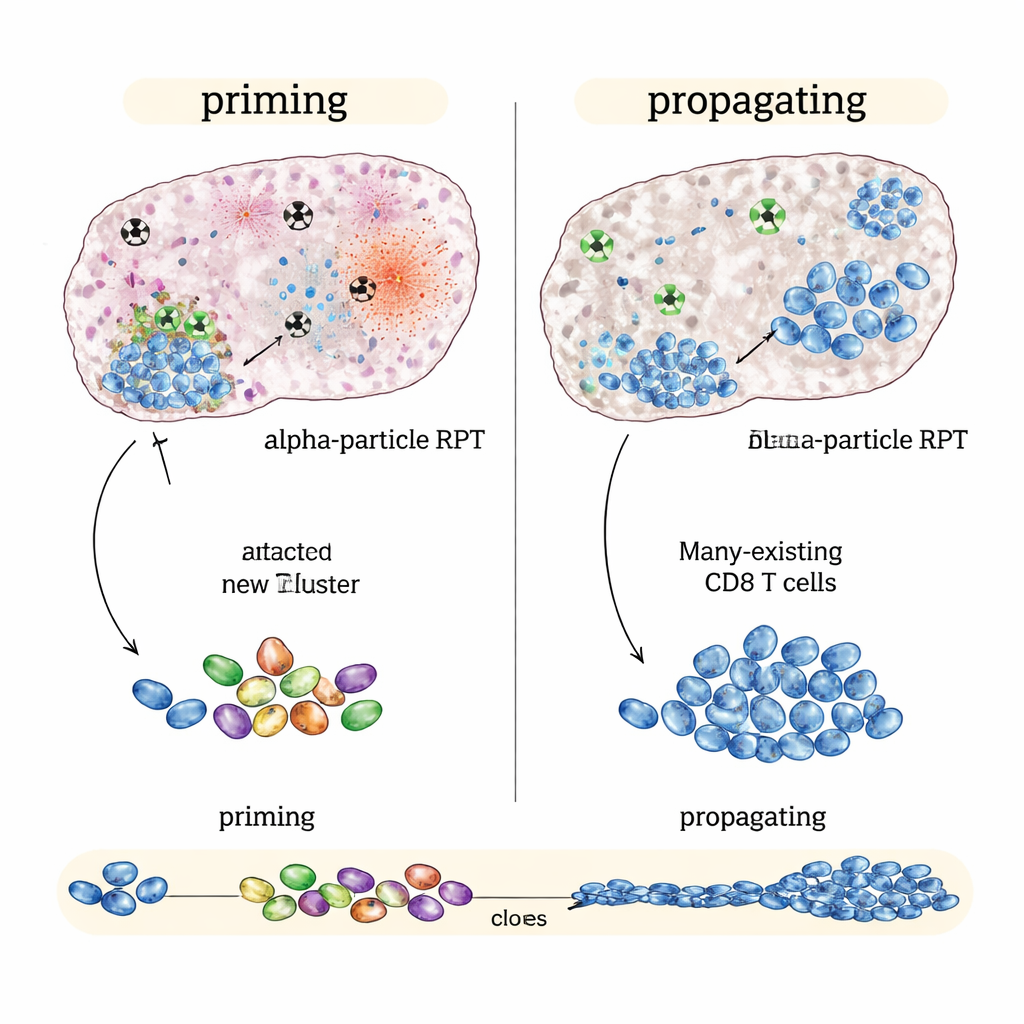
Wanneer alfa‑straling uitblinkt: het ontketenen van een nieuwe immuunaanval
Daarentegen presteerde in ‘immuun‑koude’ tumoren, zoals een melanoom‑ en een prostaatkankermodel die nauwelijks op checkpointmiddelen alleen reageren, de alfa‑uitzender beter dan bèta‑uitzenders bij dezelfde gemiddelde tumordosis. Alfa‑gebaseerde therapie plus immuunmiddelen vertraagde de tumorgroei sterker en verlengde de overleving meer. Enkel‑cel genetische analyses suggereerden waarom: alfa‑straling veroorzaakte intense, gelokaliseerde schade die sterke alarmsignalen binnen de tumor leek op te wekken terwijl aangrenzende immuunstructuren grotendeels werden gespaard. Dit patroon ging samen met bredere, meer diverse T‑celresponsen en aanwijzingen dat nieuwe tumorsignalende cytotoxische T‑cellen werden gevormd en gekoppeld aan langlevend geheugen — bewijs van immuunpriming in plaats van louter amplificatie.
Waarom type en timing van straling ertoe doen
Over de verschillende modellen heen presteerde vroege of tussentijdse toediening van checkpointremmers — ruwweg samenvallend met het piekmoment van stralingsgeïnduceerde gevarensignalen — consequent beter dan uitgestelde behandeling. Het werk suggereert een praktische vuistregel: bij kankers die al zichtbaar zijn voor het immuunsysteem kunnen laaggedoseerde bèta‑gebaseerde radiofarmaca ideale partners zijn voor checkpointremmers omdat ze bestaande immuniteit propagëren en versterken. Bij meer immuunresistente kankers kunnen hoogimpact alpha‑uitzenders beter geschikt zijn om nieuwe T‑celresponsen te primen en een ‘koude’ tumor ‘heet’ te maken. Voor patiënten betekent dit dat niet alle radioactieve middelen onderling uitwisselbaar zijn; het afstemmen van isotoop en schema op de immuunpersoonlijkheid van de tumor kan combinatie radio‑immunotherapie zowel effectiever als duurzamer maken.
Bronvermelding: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Trefwoorden: radiofarmaceutische therapie, alfa vs bèta straling, remmers van immuuncheckpoints, kankerimmunotherapie, tumormicro‑omgeving