Clear Sky Science · nl
Veiligheid en biologische activiteit van een bispecifieke T‑celreceptor gericht op HIV Gag bij mannen met HIV: een eerst‑in‑mensonderzoek
Waarom deze nieuwe HIV‑studie ertoe doet
Mensen met HIV kunnen tegenwoordig dankzij moderne medicijncombinaties bijna normale levensverwachtingen hebben. Maar deze middelen, antiretrovirale therapie (ART) genoemd, verwijderen het virus niet; ze houden het alleen onder controle. Verborgen reservoirs van HIV blijven in het lichaam aanwezig en kunnen de infectie opnieuw opstarten als de behandeling wordt gestopt. Deze studie onderzoekt een nieuw soort precieze immuuntherapie — opgebouwd rond een in het laboratorium gemaakte T‑celreceptor — die tot doel heeft het immuunsysteem te trainen om die schuilplaatsen veilig op te sporen bij mensen die al goed onder controle zijn met ART.
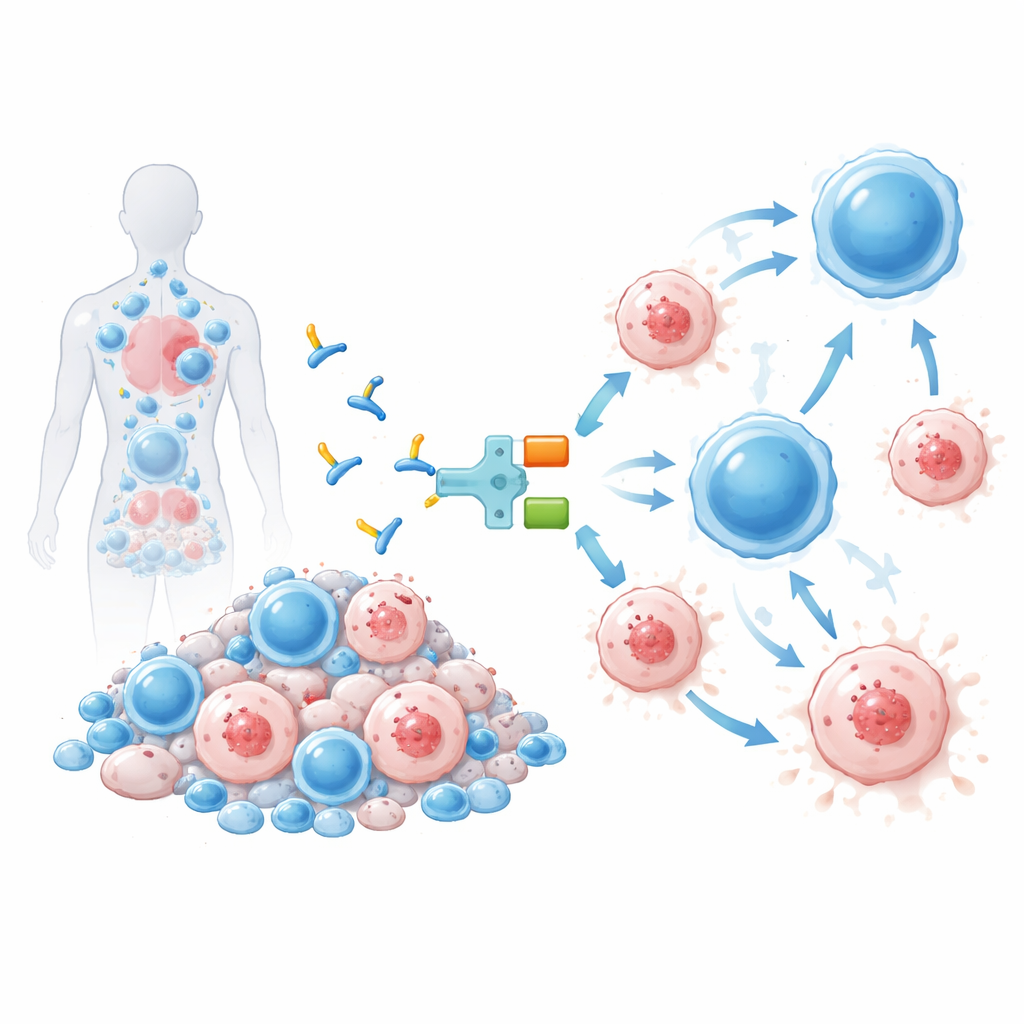
Het verborgen virus dat niet verdwijnt
Zelfs wanneer bloedtests “ondetecteerbaar” virus aangeven, blijft HIV aanwezig als genetisch materiaal in langlevende cellen, voornamelijk een type witte bloedcel dat CD4‑T‑cel wordt genoemd. Deze reservoircellen dragen stil maar intact virus dat weer actief kan worden, waardoor mensen levenslang dagelijks pillen moeten slikken. Het volledig uitroeien van elke geïnfecteerde cel is buitengewoon moeilijk en is alleen in een klein aantal mensen bereikt die risicovolle beenmergtransplantaties voor kanker ondergingen. Veel onderzoekers streven daarom naar een “functionele genezing”: het reservoir zo verkleinen dat het eigen immuunsysteem HIV onder controle kan houden zonder voortdurende medicatie.
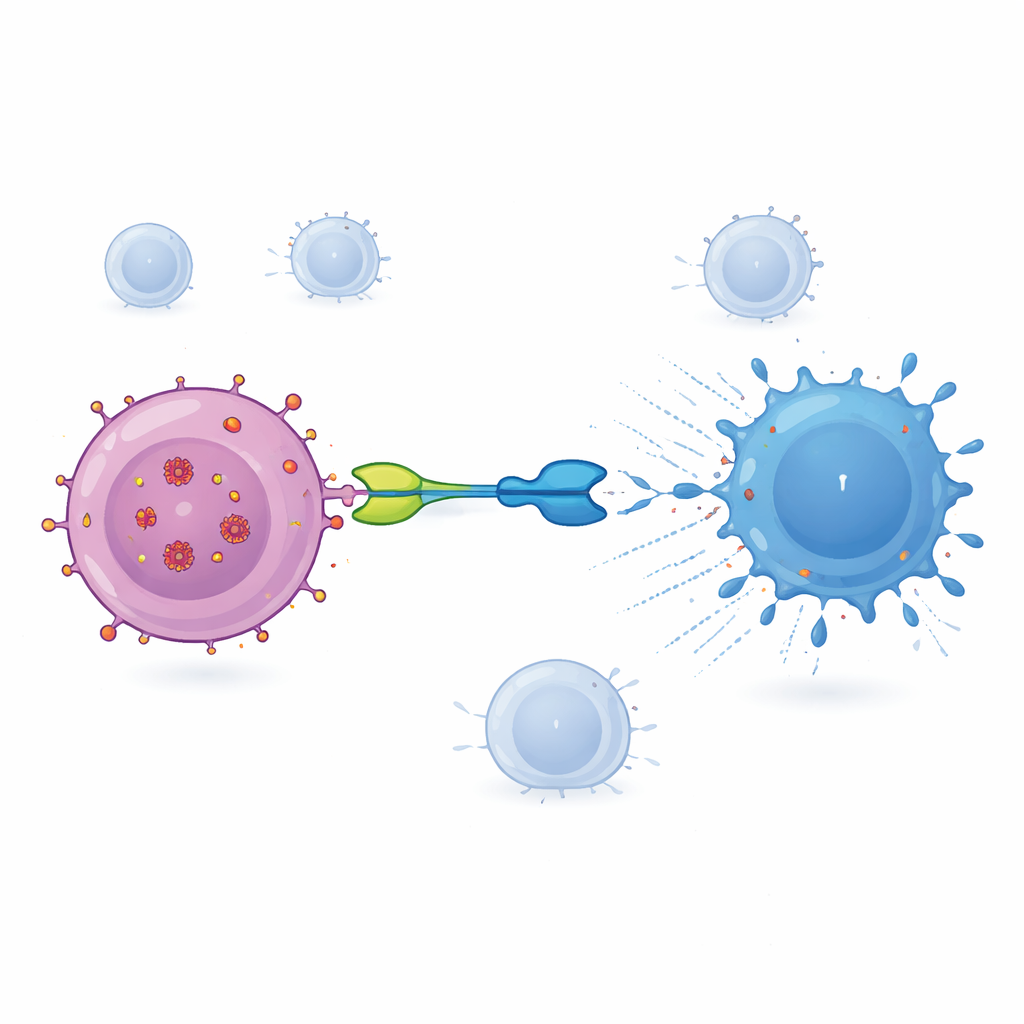
Een ontworpen molecuul om T‑cellen te herleiden
De hier geteste therapie, IMC‑M113V genoemd, is een klein eiwit dat fungeert als een moleculaire adapter tussen geïnfecteerde cellen en het immuunsysteem. Het ene uiteinde van IMC‑M113V is een geconstrueerde T‑celreceptor die een klein HIV‑fragment van het Gag‑eiwit herkent dat op het oppervlak van geïnfecteerde cellen wordt gepresenteerd in de context van een veelvoorkomende immuunmarker (HLA‑A*02:01). Het andere uiteinde hecht zich aan CD3, een structuur die aanwezig is op alle T‑cellen. Wanneer IMC‑M113V beide zijden tegelijk bindt, brengt het gewone T‑cellen dicht bij een HIV‑geïnfecteerde cel en activeert hen om deze te doden. In laboratoriumtesten was dit molecuul extreem gevoelig: het detecteerde slechts enkele kopieën van het virale fragment op het celoppervlak en elimineerde effectief cellen die met verschillende veelvoorkomende HIV‑varianten waren geïnfecteerd, terwijl het geen noemenswaardige activatie toonde tegen een reeks gezonde menselijke cellen.
Eerste test bij mensen met HIV
Om te bepalen of deze benadering veilig is bij mensen, voerden de onderzoekers een vroegfaseonderzoek uit bij twaalf volwassen mannen met HIV in het Verenigd Koninkrijk, België en Spanje. Alle deelnemers hadden goed gecontroleerde infectie met ART, hoge CD4‑waarden en droegen het vereiste HLA‑type. Elke persoon kreeg één intraveneuze dosis IMC‑M113V op een van drie lage doseringsniveaus en werd vervolgens een maand nauwgezet gevolgd. De belangrijkste focus in deze fase was veiligheid: het zoeken naar bijwerkingen zoals koorts, ernstige ontsteking of neurologische problemen, die kunnen optreden bij andere krachtige T‑cel‑activerende geneesmiddelen die in de kankerbehandeling worden gebruikt.
Wat de onderzoekers in de kliniek zagen
Over alle doses genomen werd IMC‑M113V over het algemeen goed verdragen. Helft van de deelnemers meldde enige bijwerkingen, meestal milde klachten zoals vermoeidheid of huidirritatie, en niemand ontwikkelde ernstige problemen zoals cytokine‑afgiftesyndroom of neurotoxiciteit. Bloedtests lieten zien dat de niveaus van het middel binnen ongeveer een dag stegen en daalden, met een halfwaardetijd van ongeveer 15–22 uur. Bij de hoogste dosis (15 microgram) vertoonden meerdere deelnemers tijdelijke stijgingen in ontstekingsmoleculen, vooral interleukine‑6, en tekenen dat hun T‑cellen geactiveerder waren en beter in staat om cel‑dodende eiwitten te produceren. Deze immuunveranderingen waren het sterkst bij vrijwilligers wiens virussen Gag‑varianten droegen waaraan IMC‑M113V bijzonder sterk kan binden, wat suggereert dat het middel zijn beoogde doelwitten in het lichaam aanschakelde. Na een enkele dosis was er echter geen meetbare vermindering van de omvang van het HIV‑reservoir in bloed, beoordeeld aan de hand van viraal RNA en intact viraal DNA in CD4‑cellen.
Wat dit betekent voor toekomstige HIV‑behandeling
Voor de niet‑specialistische lezer is de belangrijkste boodschap dat deze studie een belangrijke eerste proof‑of‑concept levert: een zeer gericht immuun "brug"‑molecuul kan veilig worden toegediend aan mensen met goed gecontroleerd HIV en kan hun T‑cellen activeren om cellen met het virus te herkennen. Het genas HIV niet en maakte het voor mensen niet mogelijk te stoppen met ART, maar dat was ook niet het doel van deze eerst‑in‑mensstudie. De bevindingen ondersteunen het testen van hogere en herhaalde doses, mogelijk in combinatie met middelen die meer geïnfecteerde cellen ertoe aanzetten zich te onthullen, en het uitbreiden van de benadering naar andere immuuntypes buiten HLA‑A*02:01. Als toekomstige onderzoeken bevestigen dat deze strategie betrouwbaar virale reservoirs kan verkleinen zonder gevaarlijke bijwerkingen, kan het een belangrijk onderdeel worden van combinatiebehandelingen gericht op langdurige, medicijnvrije controle van HIV.
Bronvermelding: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Trefwoorden: HIV‑genezing, T‑celtherapie, viraal reservoir, bispecifieke receptor, klinische proef