Clear Sky Science · nl
Mechanistische inzichten in PCBP1-gestuurde ontwinding van geselecteerde i-motief-DNA bij de G1/S-checkpoint
DNA-vouwen die als verkeerslichten werken
Binnen onze cellen is de genetische code meer dan een simpele rechte ladder van DNA. Delen ervan kunnen in ongewone vormen vouwen die fungeren als kleine schakelaars en helpen bepalen wanneer cellen hun DNA kopiëren en delen. Deze studie richt zich op één zulk vorm, het zogenaamde i-motief, en op een eiwit genaamd PCBP1 dat deze structuren kan herkennen en ontwinden op het moment dat een cel zich voorbereidt op DNA-replicatie. Begrijpen hoe deze interactie werkt werpt licht op hoe cellen hun genomen stabiel houden en wat er mis kan gaan bij kanker.
Vreemde DNA-knopen in kankerkoppelde regio’s
De meeste mensen leren dat DNA de beroemde dubbele helix vormt, maar bepaalde C-rijke reeksen (voor cytosine) kunnen vouwen tot een viervoudige knoop die bekendstaat als een i-motief. Deze structuren verschijnen vaak in regelregio’s van genen die celgroei aansturen, zoals cMYC en BCL2. Jarenlang werd er gedebatteerd of i-motieven echt in levende cellen vormen, omdat ze gemakkelijker te detecteren zijn in zure reageerbuiscondities dan bij de bijna-neutrale omstandigheden in het lichaam. Met behulp van gespecialiseerde antilichamen die i-motieven herkennen, heeft recent werk, inclusief de hier beschreven studie, bevestigd dat ze daadwerkelijk in celkernen voorkomen — en vaak clusteren nabij belangrijke groei- en kankergenen.
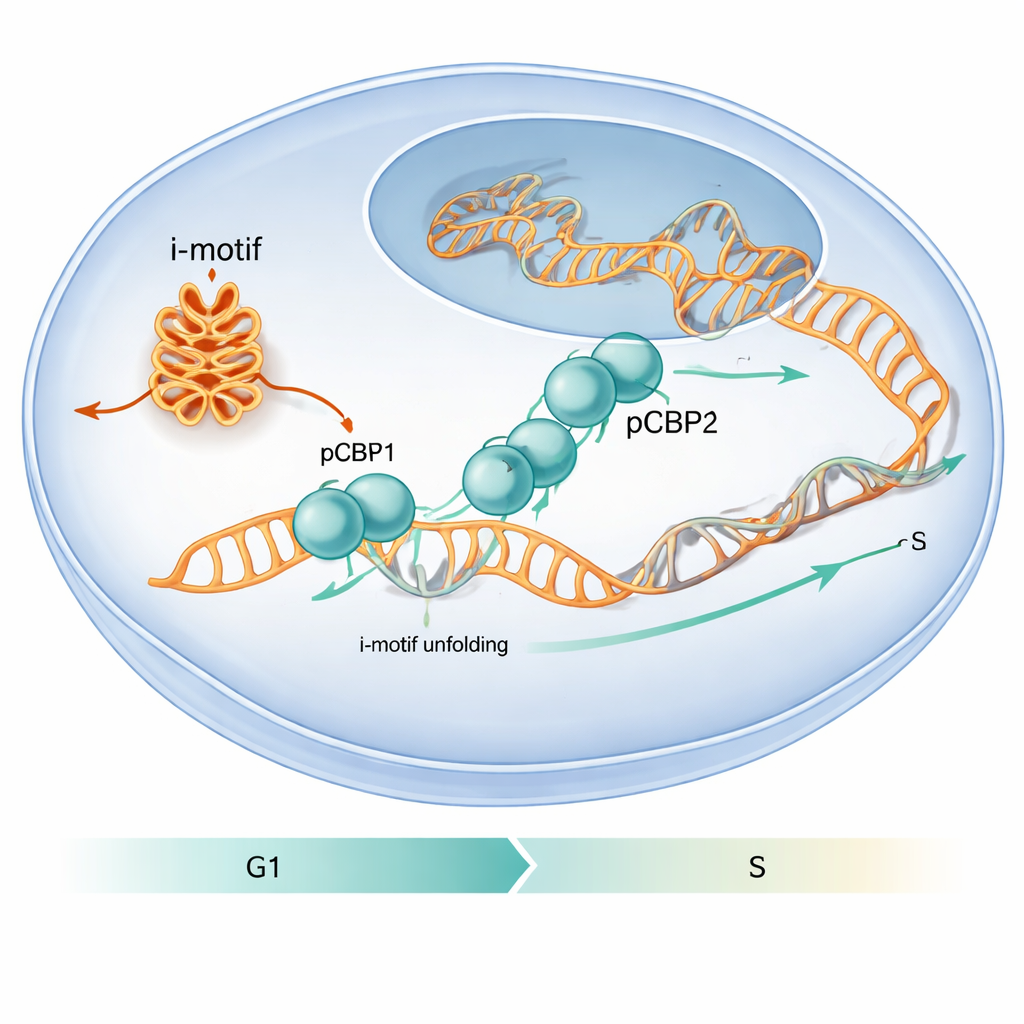
Een eiwit dat speciale DNA-vouwen uitkiest
De auteurs wilden uitzoeken hoe eiwitten in de cel met deze ongewone DNA-vouwen omgaan. Ze richtten zich op PCBP1, een eiwit dat al bekendstaat om het binden van C-rijke DNA- en RNA-streken en om zijn invloed op de celcyclus. Door bestaande genoombrede bindingskaarten te analyseren en gerichte experimenten uit te voeren, vonden ze dat PCBP1 vaak op C-rijke regio’s zit die i-motieven kunnen vormen, vooral rond genstartersites. In celexperimenten met menselijke kankercellijnen toonden regio’s uit de promotoren van cMYC, BCL2 en de insulinegekoppelde ILPR-sequentie zowel sterke i-motiefsignalen als sterke PCBP1-bezetting, wat suggereert dat PCBP1 een toegewijde beschermer van deze structuren is.
Hoe PCBP1 de knoop pakt en ontwindt
In reageerbuisassays vergeleken de onderzoekers hoe goed PCBP1 gebogen i-motieven bindt versus dezelfde DNA-sequentie in een ontvouwen vorm. Ze stelden de zuurgraad zodanig af dat het DNA óf gevouwen bleef óf ontspande, terwijl het eiwit stabiel bleef. PCBP1 toonde altijd een voorkeur voor het gevouwen i-motief en bond het ongeveer twee keer zo sterk als dezelfde sequentie in de ontvouwen toestand, en alleen zwak aan niet-verwante DNA-vormen. Eenmaal gebonden kon PCBP1 actief ontwinding bevorderen, waardoor de i-motiefstreng kon paaren met zijn complementaire partner. Niet alle i-motieven gedroegen zich echter hetzelfde: sommige, zoals de structuur in de cMYC-promotor, ontvouwden snel, terwijl andere, zoals die in BCL2, weerstand boden en slechts langzaam ontvouwden. Extra kenmerken zoals haarspeldlussen in het DNA en de mate waarin de cytosines chemisch geprotoneerd waren (met extra positieve lading) konden de ontwindingsactiviteit van PCBP1 zowel helpen als belemmeren.
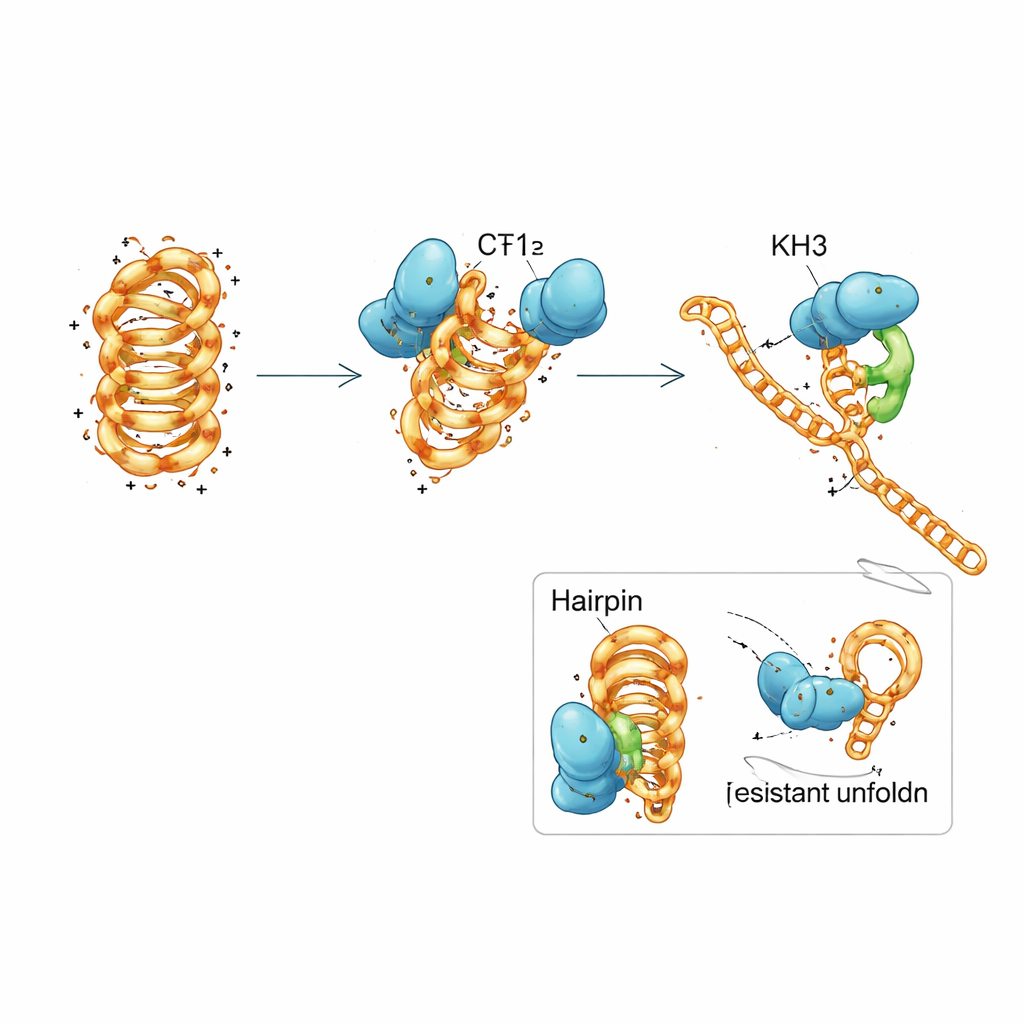
Teamwerk binnen één eiwit
PCBP1 bestaat uit drie herhaalde modules genaamd KH-domains, veelvoorkomende motieven die korte nucleïnezuurstreken grijpen. Het team splitste PCBP1 in stukken en ontdekte dat geen enkele individuele KH-domain het gedrag van het volledige eiwit volledig kon nabootsen. De eerste twee domeinen samen konden zowel gevouwen als ontvouwen DNA vastpakken en het i-motief richting een minder stabiele vorm duwen, maar zij bevorderden volledige ontwinding slechts langzaam. Het derde domein op zichzelf bond nauwelijks. Wanneer alle drie domeinen aanwezig waren en samenwerken, herwon het eiwit zijn sterke voorkeur voor gevouwen i-motieven en zijn efficiënte vermogen om ze te ontwinden. Gedetailleerde biofysische metingen en computermodellering suggereerden een stapsgewijs mechanisme: KH1 en KH2 hechten eerst aan flexibele lusregio’s van het i-motief en verstoren gedeeltelijk geselecteerde basenparen, wat vervolgens KH3 in staat stelt zich te binden en de structuur naar een open, replicatieklare staat te drijven.
De celcyclus op schema houden
Het werk toont ook aan dat deze moleculaire dans van belang is voor celgedrag. Wanneer de onderzoekers PCBP1-niveaus in menselijke cellen verlaagden, verschenen er meer i-motiefstructuren op specifieke genpromotoren, namen markers voor DNA-schade toe en raakten cellen vast op het kritieke G1/S-checkpoint — het moment net voordat DNA-replicatie begint. Onder normale omstandigheden piekt de aanwezigheid van PCBP1 op i-motiefvormende regio’s rond dit checkpoint en neemt vervolgens af zodra de S-fase begint en de i-motieven zijn opgelost. Deze timing suggereert dat PCBP1 fungeert als verzorger: het bindt en ontwindt specifieke i-motieven op precies het juiste moment zodat DNA-replicatie soepel kan verlopen en het genoom intact blijft. Voor de lezer zonder specialistische achtergrond is de boodschap dat ongewone DNA-vouwen kunnen werken als tijdelijke wegversperringen, en dat PCBP1 een van de gespecialiseerde gereedschappen van de cel is om die te verwijderen, wat helpt fouten te voorkomen die anders aan kanker zouden kunnen bijdragen.
Bronvermelding: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Trefwoorden: i-motief DNA, PCBP1-eiwit, celcyclus checkpoint, genoomstabiliteit, DNA secundaire structuur