Clear Sky Science · nl
Lipidnanodeeltjesdatabase gericht op structuur-functiemodellering en datagedreven ontwerp voor levering van nucleïnezuren
Waarom kleine vetbellen ertoe doen voor toekomstige geneesmiddelen
Lipidnanodeeltjes zijn microscopische, op vet gebaseerde belletjes die genetische instructies—zoals mRNA-vaccins—veilig in onze cellen afgeven. Ze speelden een sleutelrol bij COVID-19-vaccins, maar onderzoekers begrijpen nog niet volledig hoe hun gedetailleerde chemische samenstelling bepaalt hoe goed ze werken. Dit artikel beschrijft een nieuwe online bron, de Lipid Nanoparticle Database (LNPDB), gemaakt om verspreide gegevens op één plek te verzamelen zodat wetenschappers systematisch betere en veiligere genafgifte-geneesmiddelen kunnen ontwerpen.
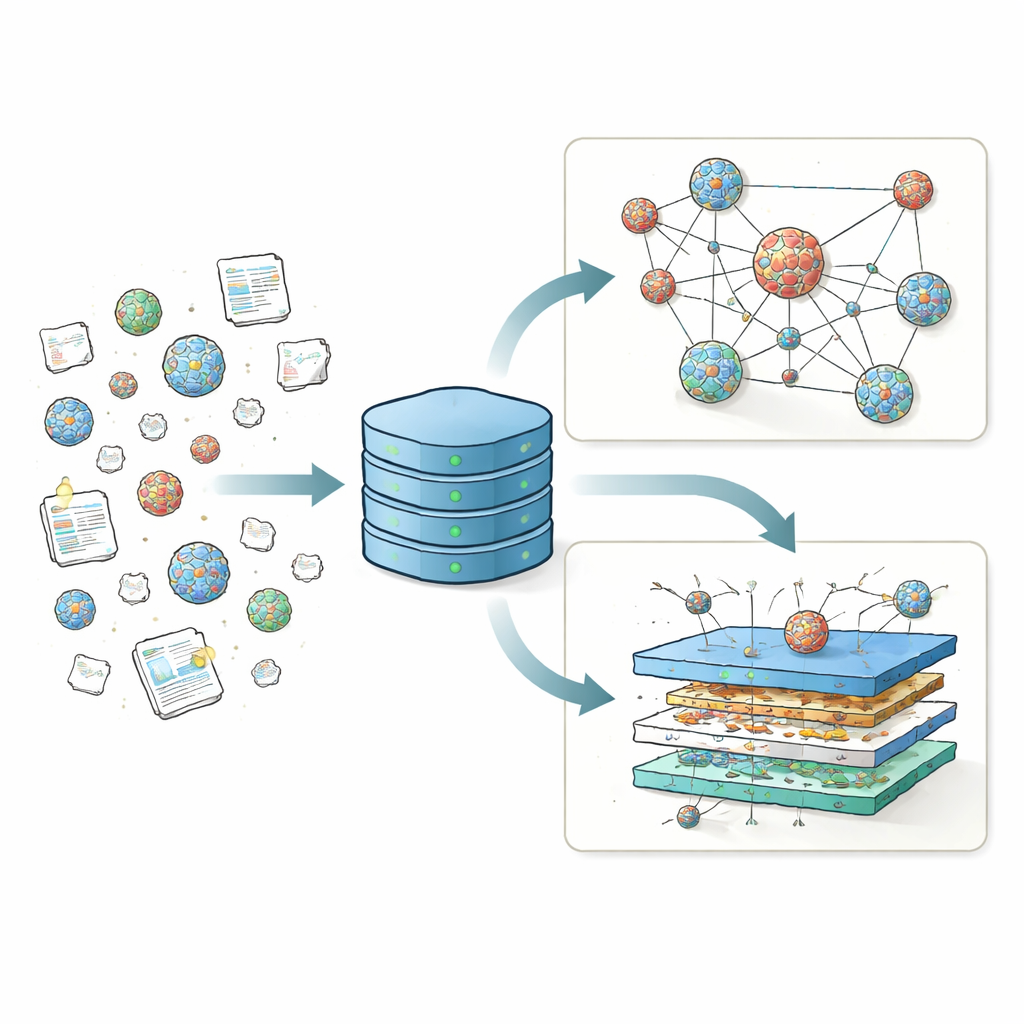
Verspreide resultaten samenbrengen op één plek
Jarenlang hebben verschillende laboratoria duizenden LNP-recepten getest, waarbij ze het belangrijkste geladen lipid, hulp-lipiden, cholesterol en beschermende coating-lipiden varieerden om te zien welke combinaties genetisch materiaal het meest effectief afleveren. Maar deze resultaten werden in veel formaten over tientallen artikelen gerapporteerd, wat het moeilijk maakte studies te vergelijken of grote trends te ontdekken. In tegenstelling tot eiwitonderzoek, dat geborgd is door een centrale Protein Data Bank die tools als AlphaFold voortbracht, had het LNP-veld geen uniforme repository voor structuur- en prestatiegegevens. LNPDB vult deze leemte door gedetailleerde informatie te verzamelen over 19.528 LNP-formuleringen afkomstig uit 42 studies en een commerciële leverancier, en door te standaardiseren hoe de ingrediënten, testcondities en uitkomsten van elk deeltje worden gecodeerd.
Wat er in de nieuwe database staat
Elke LNP-vermelding in LNPDB wordt beschreven langs drie hoofdaspecten: samenstelling, experiment en simulatie. Velden over samenstelling registreren welke lipiden werden gebruikt, hoeveel stikstofatomen het belangrijkste geladen lipid bevat, en de exacte mengverhoudingen tussen de vier kerncomponenten: ioniseerbaar lipid, hulp-lipid, cholesterol en een polyethyleenglycol (PEG)-lipide. Experimentele velden geven vast welk soort genetische lading werd afgeleverd—meestal mRNA dat codeert voor een rapportereiwit—waar het werd gericht (bijvoorbeeld cellen in een kweek, lever, long of spier), hoe de deeltjes werden bereid en hoe succes werd gemeten. Tenslotte bieden simulatievelden kant-en-klare bestanden die het fysieke gedrag van elk lipidmolecuul in voldoende detail beschrijven om atoomniveausimulaties van lipidemembranen uit te voeren. Samen zetten deze gestandaardiseerde beschrijvingen een lappendeken van afzonderlijke schermen om in een coherent landschap dat door de gemeenschap doorzocht, gefilterd en uitgebreid kan worden.
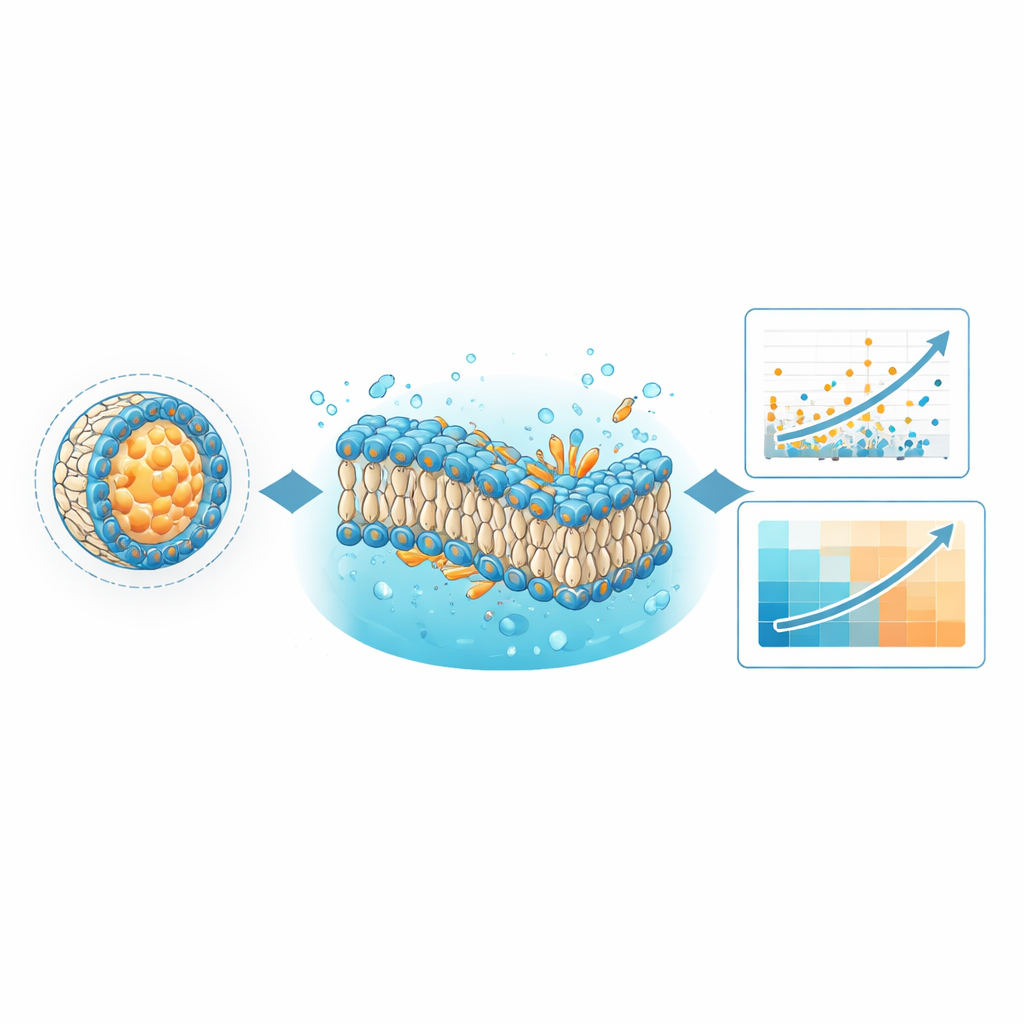
Computers leren betere afleverrecepten te herkennen
Een directe toepassing van LNPDB is het verbeteren van machine-learningmodellen die voorspellen welke formuleringen genetisch materiaal het meest effectief afleveren. De auteurs trainden hun bestaande diep leermodel, LiON, opnieuw met de uitgebreide LNPDB-dataset en verdubbelden daarmee meer dan het aantal voorbeelden dat het model eerder had gezien. LiON leert patronen die de chemische structuren van de ioniseerbare lipiden, de mix van hulpcomponenten en de testcontext koppelen aan de prestaties van elke formulering. Met de rijkere data kwamen LiONs voorspellingen beter overeen met experimentele resultaten voor de meeste testsets en presteerde het beter dan een concurrerend model, AGILE, op meerdere onafhankelijke datasets. Dit suggereert dat een brede, diverse en continu groeiende trainingsset cruciaal is voor het bouwen van algemene ontwerptools voor toekomstige LNP-geneesmiddelen.
Modelmembranen bekijken om verborgen regels te ontdekken
De database is ook opgezet voor een heel ander type berekening: fysica-gebaseerde moleculaire dynamicasimulaties. Met de bij LNPDB meegeleverde simulatiebestanden bouwde het team vereenvoudigde membranen die geselecteerde LNP-formuleringen representeren en observeerde hun gedrag over microseconden aan gesimuleerde tijd. Ze stelden twee vragen: blijven de gemodelleerde dubbellaagmembranen intact en welke algemene vorm nemen de belangrijkste lipiden binnen het membraan aan? De simulaties toonden aan dat formuleringen waarvan de membranen stabiel bleven, experimenteel vaker succesvol waren. Ze kwantificeerden ook een kenmerk genaamd de “critical packing parameter”, dat aangeeft of een lipid meer kegel- of omgekeerde-kegelvormig is in het membraan. In meerdere geteste bibliotheken vertoonden lipiden waarvan de vorm negatieve kromming bevoordeelde—wat wordt gedacht te helpen bij het fuseren met en verstoren van endosomale membranen—sterkere levering, soms beter correlerend met prestatie dan het diep leermodel zelf.
Een nieuw fundament voor slimmer nanogeneeskunde
Voor niet-specialisten is de kernboodschap dat dit werk een gedeelde, groeiende “kaart” opbouwt van hoe de ingrediënten en structuur van kleine vetbellen samenhangen met hun vermogen genetische therapieën af te leveren. Door tienduizenden eerdere experimenten samen te brengen, krachtige voorspellingsmodellen mogelijk te maken en tools te bieden om te simuleren hoe deeltjes zich op moleculair niveau gedragen, legt LNPDB het fundament voor meer rationeel ontwerp in plaats van proefondervindelijke bijstellingen. In de loop der tijd kan deze datagedreven aanpak het maken van effectievere vaccins, genbewerkingstherapieën en andere op nucleïnezuren gebaseerde behandelingen versnellen, terwijl het onderzoekers helpt te begrijpen waarom bepaalde nanopartikelrecepten werken—en andere niet.
Bronvermelding: Collins, E., Ji, J., Kim, SG. et al. Lipid Nanoparticle Database towards structure-function modeling and data-driven design for nucleic acid delivery. Nat Commun 17, 2464 (2026). https://doi.org/10.1038/s41467-026-68818-1
Trefwoorden: lipidnanodeeltjes, mRNA-levering, nanogeneeskunde, machine learning, moleculaire dynamica