Clear Sky Science · nl
Chemisch geleide transcriptomica op enkelcel-niveau onthult sulfotransferase-gemedieerde herinrichting van het skelet in de biosynthese van securinine
Waarom de chemie van een struik ertoe doet
Securinega-alkaloïden zijn krachtige moleculen die voorkomen in een kleine siertstruik, Flueggea suffruticosa, en die lang zijn bestudeerd vanwege mogelijke toepassingen bij kanker en neurologische aandoeningen. Tot nu toe was echter niet echt bekend hoe deze plant zulke ingewikkelde verbindingen opbouwt. Deze studie combineert moderne enkelcel-gene‑lezing met slimme chemische experimenten om, stap voor stap, te onthullen hoe de plant deze moleculen assembleert en hervormt — en ontdekt daarbij een verrassende nieuwe rol voor een veelvoorkomend type enzym. 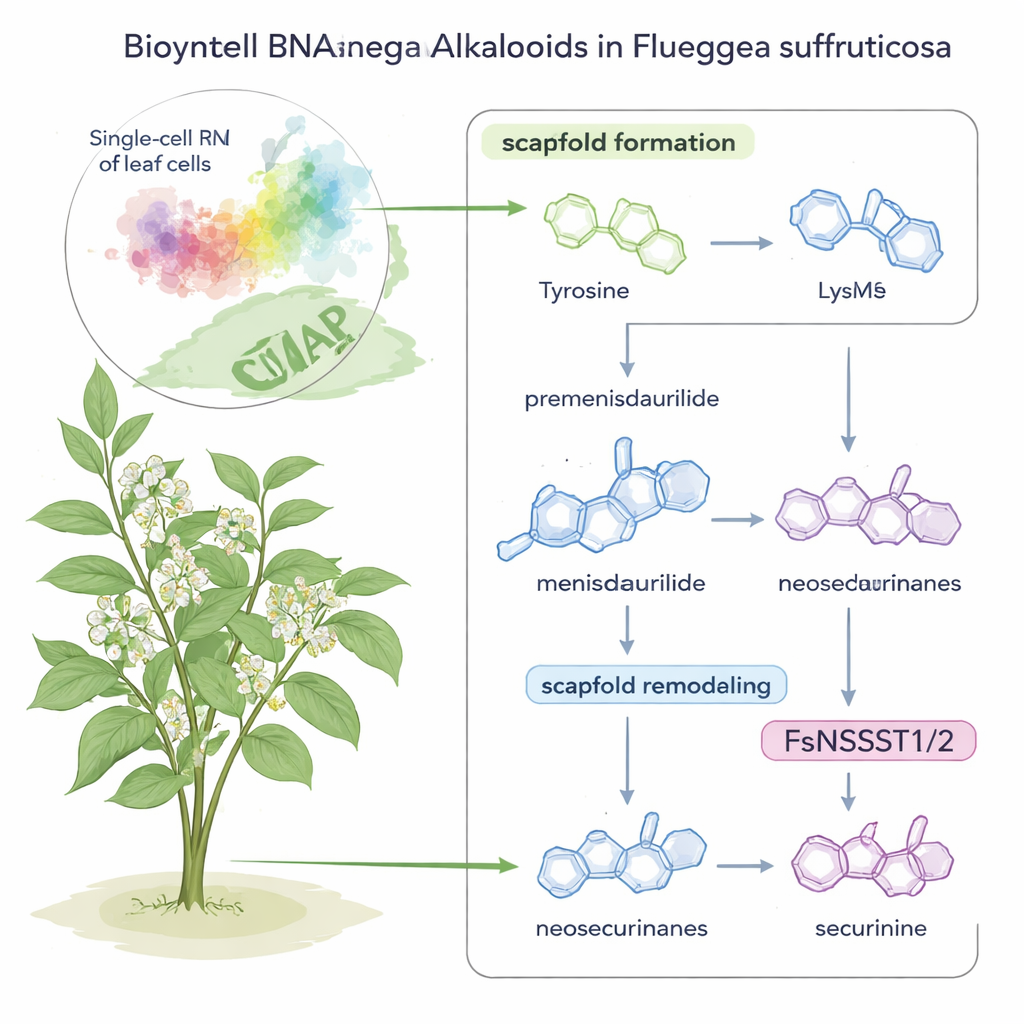
Bouwstenen uit alledaagse aminozuren
Het verhaal begint met twee bekende voedingsstoffen: de aminozuren tyrosine en lysine. In F. suffruticosa wordt tyrosine omgezet in een ongewone ringvormige verbinding genaamd premenisdaurilide, die vervolgens door reductie tot menisdaurilide wordt omgevormd door een nieuw ontdekt enzym dat de auteurs FsMS noemen (voor “menisdaurilide synthase”). Parallel daaraan wordt lysine omgezet in een klein stikstofhoudend ringetje, 1-piperideïne, door een ander enzym, FsPS, dat in eerder werk werd ontdekt. Wanneer menisdaurilide en 1-piperideïne samenkomen onder licht basische, waterachtige omstandigheden, fuseren ze spontaan tot “neosecurinane” alkaloïden — tussenstructuren op weg naar de uiteindelijke medicinale verbindingen.
De chemie in realtime zien plaatsvinden
Om te bewijzen dat deze voorgestelde stappen niet louter theoretisch zijn, synthetiseerde het team versies van de vermoedelijke tussenproducten die waren gelabeld met zware koolstofatomen. Het voeren van deze gelabelde moleculen aan plantaardige extracten stelde de wetenschappers in staat precies te volgen waar de atomen terechtkwamen. Ze zagen dat gelabeld menisdaurilide werd omgezet in gelabelde neosecurinanes, en die op hun beurt in de bekende alkaloïden allosecurinine en securinine, wat bevestigt dat deze tussenstappen daadwerkelijk onderdeel zijn van het natuurlijke pad. Belangrijk is dat sommige van de sleutelreacties die ringen vormen zelfs plaatsvonden in gekookte extracten, wat aantoont dat delen van de route zonder enzymen kunnen verlopen, puur gedreven door de chemie van de moleculen zelf.
Inzoomen op de juiste cellen
Weten welke moleculen waar verschijnen is slechts de helft van de puzzel; de genen die elke stap controleren identificeren vereist te weten welke cellen het werk doen. De onderzoekers sequentieerden RNA van duizenden individuele cellen uit F. suffruticosa-bladeren en groepeerden ze in verschillende celtypes op basis van genactiviteitspatronen. Eén cluster, geassocieerd met de bladnerven, stak eruit: het bracht sterk de bekende padgenen tot expressie en veel enzymen verbonden aan tyrosine-, lysine- en zwavelstofwisseling. Door te onderzoeken welke genen synchroon varieerden met de padenzymen binnen dit cluster, spitste het team zich toe op FsMS en twee sulfotransferases, FsNSST1 en FsNSST2, als belangrijke kandidaten voor de ontbrekende stappen. 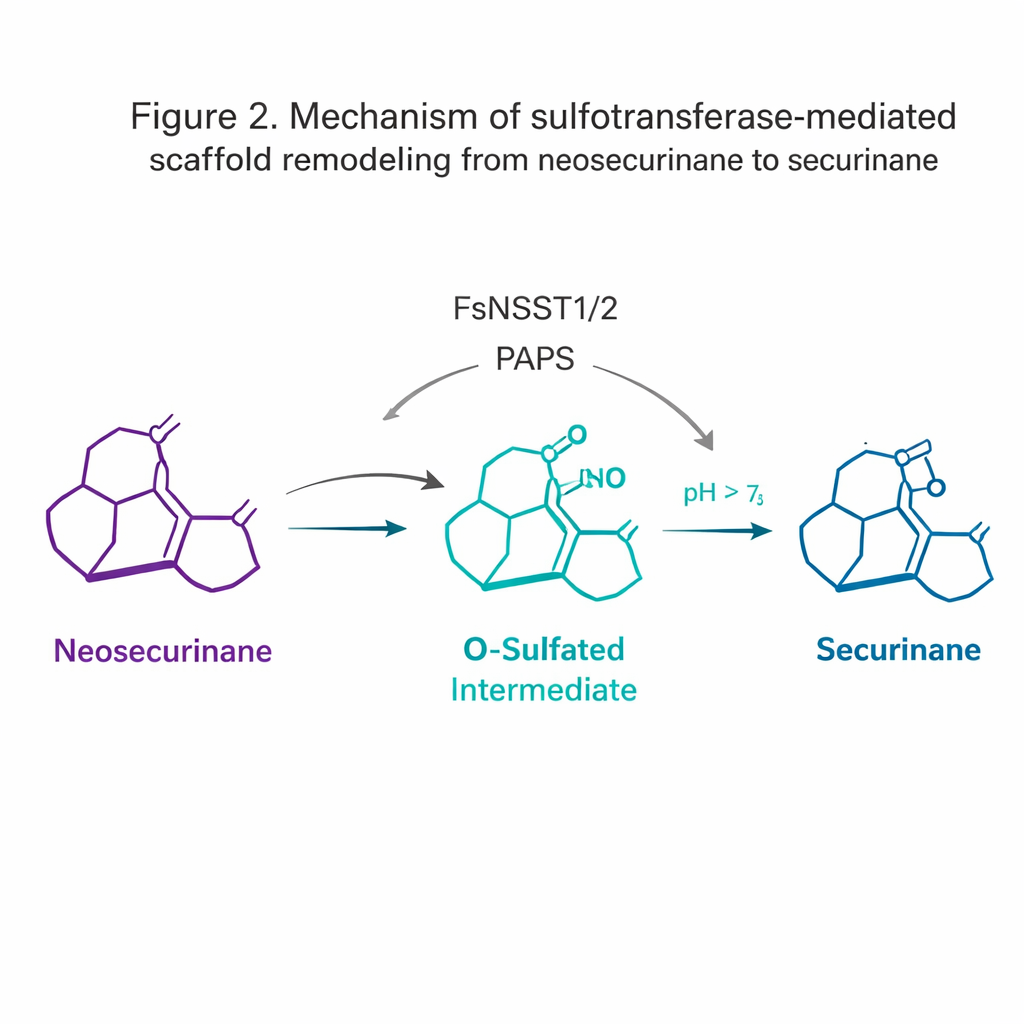
Een enzym dat het moleculaire skelet herinricht
De meest verrassende ontdekking kwam van de sulfotransferases. Sulfotransferases voegen doorgaans een sulfaatgroep toe aan moleculen om hun oplosbaarheid te verbeteren of ze te markeren voor afbraak. Hier functioneren FsNSST1 en FsNSST2 echter als omkeerders: ze hechten sulfaat aan het neosecurinane‑skelet en zetten het tijdelijk om in een hoogenergetisch “O‑gesulfateerd” tussenproduct. Deze geactiveerde vorm ondergaat vervolgens spontaan een 1,2‑amineverschuiving — een kleine herschikking waarbij een stikstofatoom migreert — waarbij het [2.2.2] bicyclische “neosecurinane” raamwerk wordt omgevormd tot het [3.2.1] “securinane” raamwerk. Deze subtiele herinrichtingsstap creëert de kenmerkende tetracyclische kern van de biologisch actieve alkaloïden.
Waarom dit pad van belang is
Voor niet‑specialisten is de kernboodschap dat de plant securinega‑alkaloïden in twee hoofdfasen assembleert: eerst bouwt hij een voorlopig ringsysteem uit alledaagse aminozuren; daarna herformuleert hij dat skelet chemisch tot een complexere vorm met behulp van een sulfaat-"trigger." Door cel‑voor‑cel genprofilering te combineren met isotopen‑gelabelde chemie kaarten de auteurs deze route in detail uit en tonen ze aan dat sulfotransferases — enzymen die in alle levensvormen voorkomen — meer kunnen doen dan moleculen enkel versieren; ze kunnen grootschalige herschikkingen van hun vorm initiëren. Het begrijpen van dit pad verduidelijkt niet alleen hoe een veelbelovende klasse van geneesmiddelachtige moleculen in de natuur ontstaat, maar opent ook de mogelijkheid om gewassen of microben te ontwerpen die nieuwe, door securinega geinspireerde medicijnen produceren.
Bronvermelding: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Trefwoorden: plantaardige alkaloïden, biosynthese, single-cell transcriptomics, sulfotransferase, natuurlijke productchemie