Clear Sky Science · nl
ALKB-1-afhankelijke tRNA-methylering is vereist voor efficiënte eliminatie van vaderlijke mitochondriën
Waarom de mitochondriën van vaders stilletjes verdwijnen
Alle mensen, wormen en de meeste andere dieren erven hun cellulaire energiecentrales—mitochondriën—bijna volledig van hun moeders. De mitochondriën van vaders komen met het sperma in het ei, maar worden snel verwijderd, een biologische schoonmaak die helpt te voorkomen dat beschadigd mitochondriaal DNA wordt doorgegeven. Deze studie in kleine rondwormen onthult een moleculair “stresscheckpoint” dat meehelpt te beslissen of vaderlijke mitochondriën efficiënt worden opgeruimd, en biedt aanwijzingen die mogelijk ooit verband houden met bepaalde vormen van onvruchtbaarheid en mitochondriale ziekten.
De energiecentrales die we van moeder erven
Mitochondriën produceren de energie die cellen in leven houdt en dragen hun eigen kleine cirkelvormige DNA. In de loop van iemands leven kan dit mitochondriale DNA schadelijke mutaties ophopen. Als beide ouders routinematig hun mitochondriën zouden doorgeven, zouden deze defecten zich kunnen mengen en zich over generaties heen kunnen opstapelen. Om dit te vermijden vertrouwen de meeste dieren op maternale overerving: het embryo behoudt de mitochondriën van de moeder en elimineert vrijwel alle mitochondriën van de vader kort na de bevruchting. Hoewel verschillende afvalroutes bekend zijn—zoals cellulaire recyclemechanismen en DNA-knippende enzymen—hebben wetenschappers nog niet volledig begrepen hoe subtiele chemische markeringen op DNA en RNA deze eliminatie van vaderlijke mitochondriën kunnen beïnvloeden.
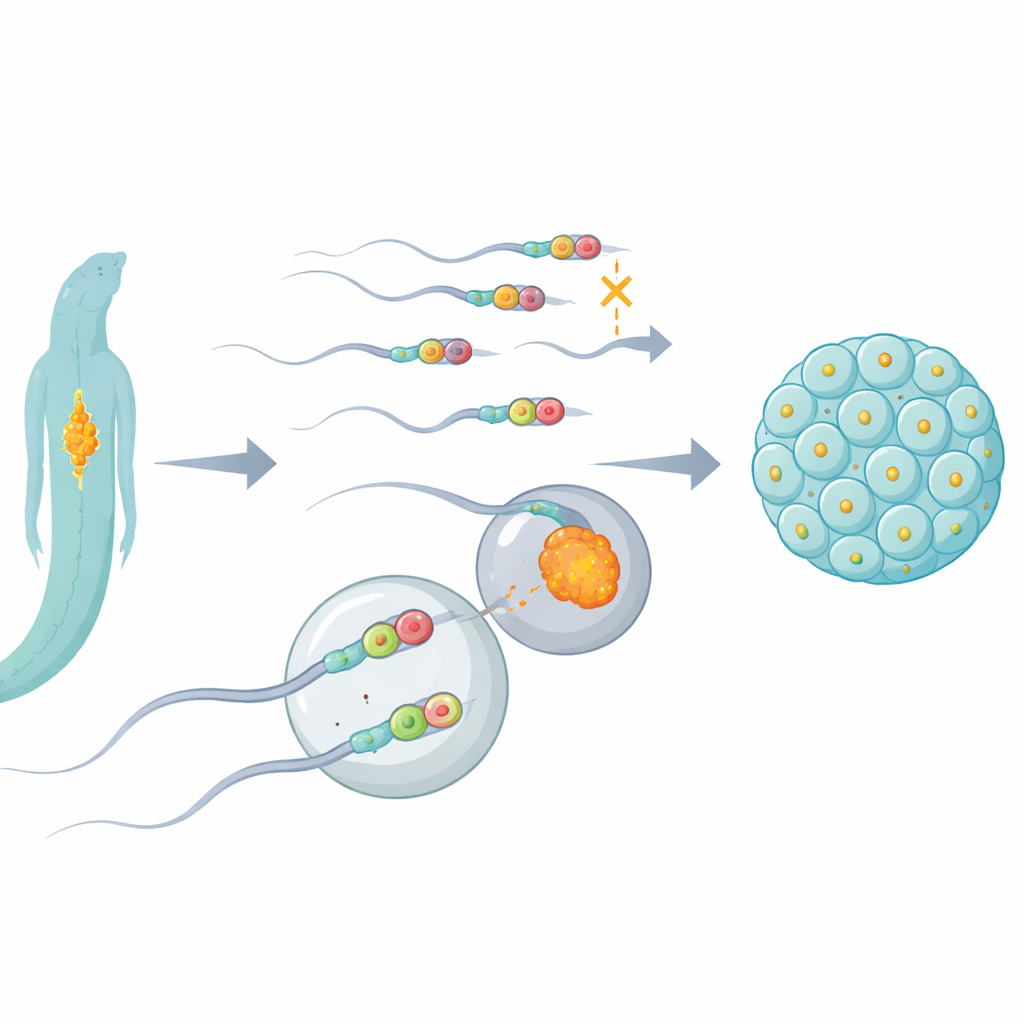
Een moleculaire gum met een belangrijke reproductieve taak
De onderzoekers richtten zich op een eiwit genaamd ALKB-1 in de nematode Caenorhabditis elegans, een werkpaard van de genetica. ALKB-1 is een soort moleculaire gum die methylgroepen—kleine chemische labels—van DNA en RNA kan verwijderen. Door ALKB-1 selectief uit te schakelen of het gehalte ervan te verlagen volgde het team wat er met sperma-mitochondriën en hun DNA gebeurde na de bevruchting. Ze ontdekten dat wanneer de chemische “gum”-activiteit van ALKB-1 verloren ging, vaderlijke mitochondriën en hun DNA abnormaal lang aanwezig bleven in zich ontwikkelende embryo’s, in plaats van snel te worden verwijderd. Deze vertraging trad voornamelijk op wanneer ALKB-1 ontbrak in sperma, en ging gepaard met sperma dat ongewoon veel mitochondriën en mitochondriaal DNA bevatte.
Hoe knoeien met tRNA-chemie mitochondriën verstoort
Dieper graafwerk richtte zich op welke chemische markeringen voor ALKB-1 echt van belang zijn. Testen op DNA suggereerden dat veranderingen in DNA-methylering alleen het probleem van het uitblijven van opruiming niet konden verklaren. In plaats daarvan verschoof de aandacht naar tRNA’s, kleine adaptermoleculen die helpen genetische boodschappen in eiwitten om te zetten. In normale wormen verwijdert ALKB-1 een specifieke markering—genoemd m1A—van een subset tRNA’s. Zonder ALKB-1 stapelden deze markeringen zich op. Deze subtiele verschuiving in tRNA-chemie wijzigde in brede zin hoe efficiënt veel eiwitten werden gemaakt: de eiwitsynthese in het celvocht nam toe, terwijl de eiwitsynthese binnen mitochondriën stokte. Het resultaat was een mismatch tussen eiwitten bestemd voor mitochondriën en wat de organellen konden verwerken, leidend tot klonten slecht beheerde eiwitten en tekenen van mitochondriale stress.
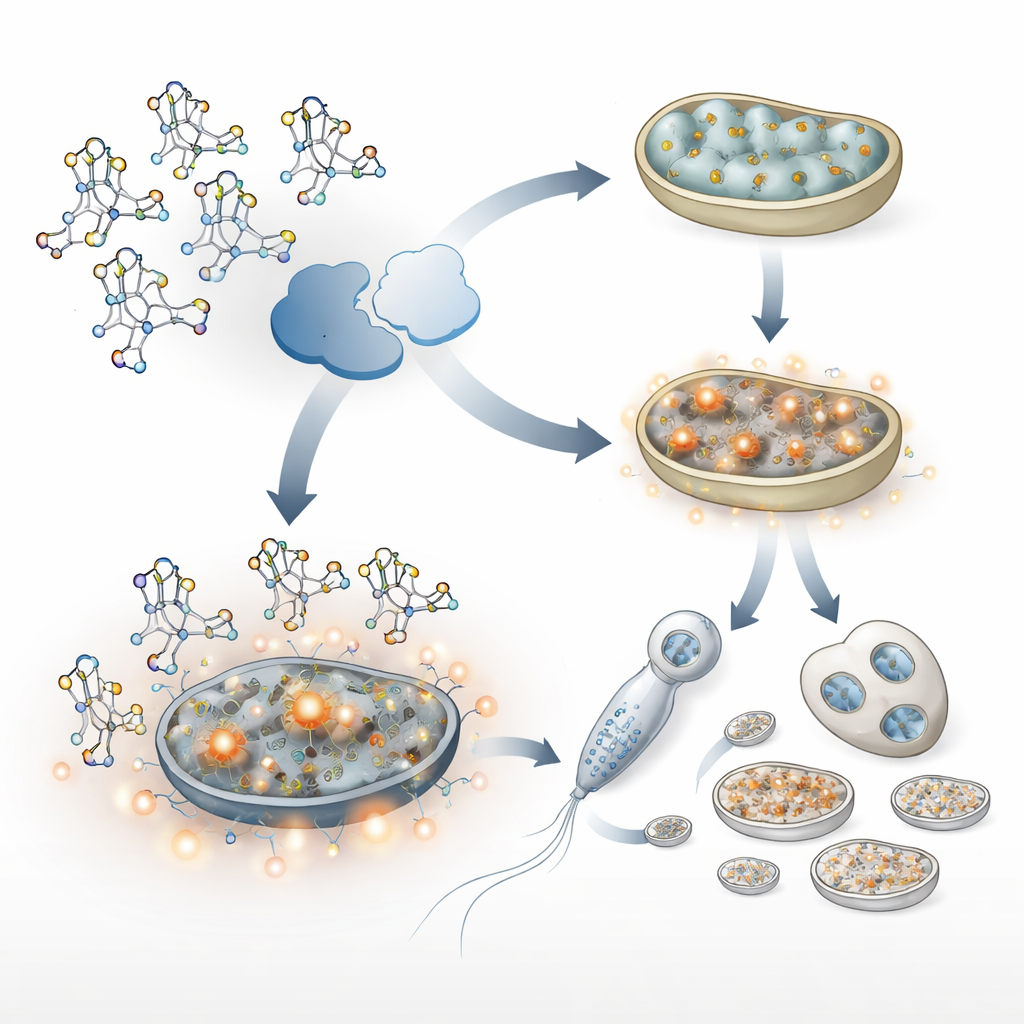
Stresssignalen die vaderlijke mitochondriën beschermen—en per ongeluk behouden
Gestreste mitochondriën produceren vaak meer reactieve zuurstofsoorten, chemisch agressieve bijproducten van de stofwisseling. In de ALKB-1-deficiënte wormen stegen deze reactieve moleculen sterk. Dat schakelde op zijn beurt twee belangrijke stressresponssystemen in: één gereguleerd door een factor vergelijkbaar met de menselijke Nrf2 (SKN-1 in wormen genoemd), en een andere bekend als de mitochondriale unfolded protein response. Gezamenlijk verhoogden deze routes de productie van nieuwe mitochondriën en stimuleerden ze het kopiëren van mitochondriaal DNA, met name in sperma. Hoewel deze respons cellen helpt schade te verwerken, had ze ook een onbedoeld bijeffect: er stapelden zich meer vaderlijke mitochondriën en mitochondriaal DNA op en deze waren moeilijker te verwijderen na de bevruchting. Het blokkeren van deze stressroutes, of het verminderen van oxiderende schade met antioxidanten, herstelde een meer normale verwijdering van vaderlijke mitochondriën.
Wanneer de schoonmaak faalt, lijden vruchtbaarheid en embryo’s
De vertraagde verwijdering van vaderlijke mitochondriën was niet slechts een microscopische curiositeit. Mannetjeswormen zonder normale ALKB-1-activiteit kregen minder nakomelingen en de embryo’s die ze hielpen maken stierven vaker. Toch werd sperma in normale aantallen gevormd en zag het er structureel intact uit, wat suggereert dat het belangrijkste probleem lag bij de kwaliteitscontrole van mitochondriën en niet bij het vormen van sperma zelf. De studie stelt voor dat door ALKB-1 gecontroleerde tRNA-markeringen fungeren als een epigentisch checkpoint: als dit systeem werkt, blijft de balans van mitochondriale eiwitten behouden, blijft stress onder controle en worden vaderlijke mitochondriën veilig geëlimineerd. Als het faalt, blijven gestreste en overmatige vaderlijke mitochondriën achter, wat de vruchtbaarheid en de vroege ontwikkeling schaadt. Hoewel deze experimenten in wormen zijn uitgevoerd, werpen ze licht op een fundamenteel principe—dat kleine chemische bewerkingen aan RNA kunnen sturen hoe we onze cellulaire energiecentrales erven en mogelijk uiteindelijk de reproductieve gezondheid bij complexere dieren, inclusief mensen, beïnvloeden.
Bronvermelding: Luo, Z., Li, Y., He, C. et al. ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination. Nat Commun 17, 2144 (2026). https://doi.org/10.1038/s41467-026-68813-6
Trefwoorden: mitorchondriale overerving, vaderlijke mitochondriën, tRNA-methylering, oxiderende stress, mannelijke vruchtbaarheid