Clear Sky Science · nl
Het functionele landschap van alternatieve splicing bij de beslissing van hematopoëtische lijnen
Hoe kleine correcties in genen ons bloed vormen
Ieder seconde maakt je lichaam miljoenen nieuwe bloedcellen. Achter dit stille wonder schuilt een moleculair redactiesysteem dat stukken van genetische boodschappen op verschillende manieren kan knippen en plakken, waardoor licht verschillende versies van hetzelfde eiwit ontstaan. Deze studie onderzoekt hoe dat bewerkingsproces, alternatieve splicing genoemd, helpt onrijpe stamcellen te sturen richting rode bloedcellen, witte bloedcellen of andere bloedceltypen — en wat er gebeurt als één bewerkt fragment ontbreekt.
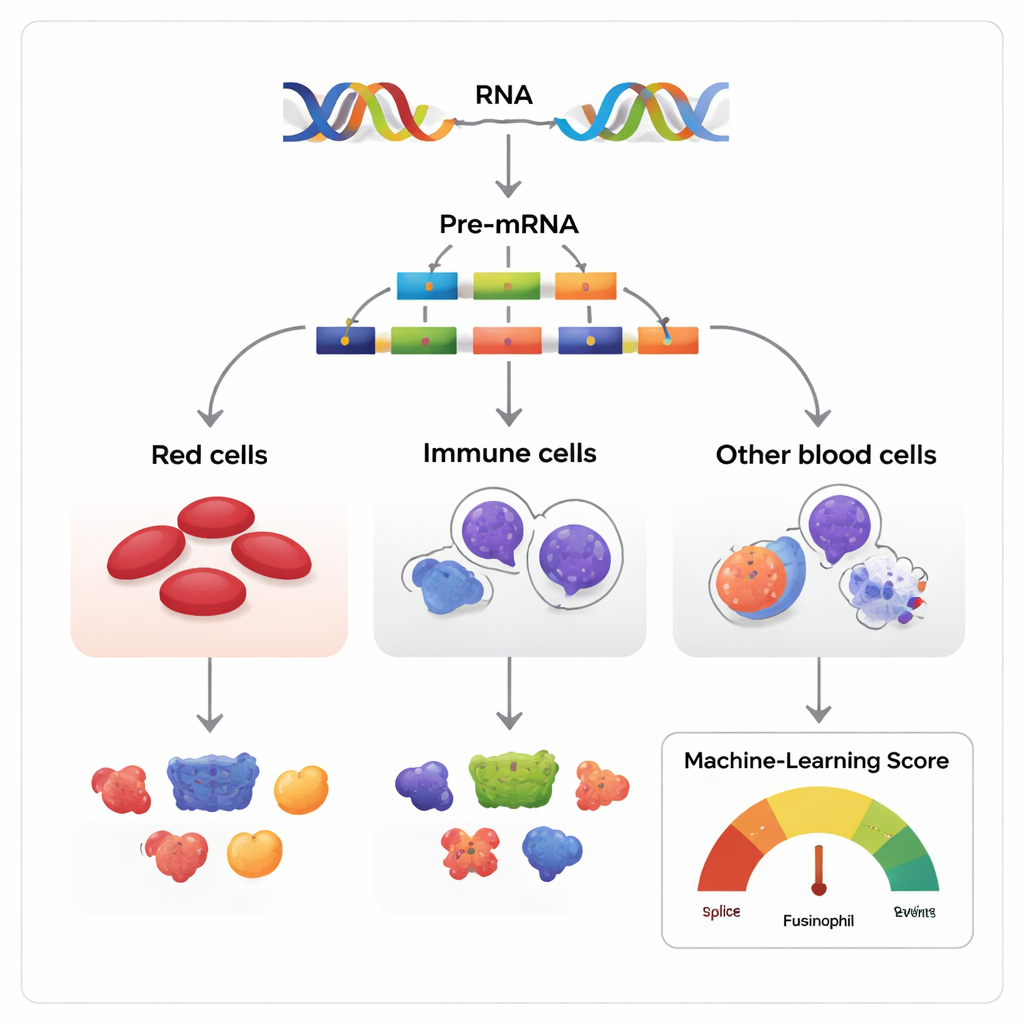
Veel versies uit hetzelfde genetische script
Genen worden vaak omschreven als bouwplannen, maar in werkelijkheid lijken ze meer op scripts die herschikt kunnen worden. Wanneer een gen wordt afgelezen, bevat de initiële RNA-kopie segmenten die exonen worden genoemd en die vóór de omzetting naar eiwit behouden of overgeslagen kunnen worden. De auteurs bestudeerden dit proces, bekend als exon skipping, in weefsels die bloed vormen bij mensen, muizen en verschillende andere gewervelden. Ze verzamelden meer dan 270 RNA-datasets die samen bloedstam- en voorlopercellen volgen terwijl ze rijpen naar drie hoofdgroepen: erytroïde cellen die rode cellen produceren, myeloïde cellen die infecties bestrijden, en lymfoïde cellen die antilichamen maken.
Rangschikken welke splice-wijzigingen echt van belang zijn
Aangezien de meeste genen met meerdere exonen op vele manieren gespliced kunnen worden, is de centrale uitdaging onschuldige variaties te onderscheiden van die welke werkelijk de celdifferentiatie beïnvloeden. De onderzoekers bouwden een machine-learningmodel, de Functional AS Score (FAScore), om dit probleem aan te pakken. Voor elk exon-skippinggebeurtenis bekijkt het model 19 informatie-elementen, zoals hoe sterk het gebruik verandert tijdens celdifferentiatie, hoe goed het omliggende DNA over soorten heen geconserveerd is, of het bekende eiwitdomeinen wijzigt, en of het plekken bevat voor chemische modificaties van het eiwit. Het algoritme, getraind met een positive–unlabeled strategie en een random forest-classifier, geeft een score tussen 0 en 1 die aangeeft hoe waarschijnlijk het is dat een gegeven splice-gebeurtenis functionele gevolgen heeft.
Het vinden van geconserveerde, lijnafhangende schakelaars
Door FAScore toe te passen op tienduizenden exon-skippinggebeurtenissen, classificeerde het team ze als waarschijnlijk functioneel, niet-functioneel of onzeker. Gebeurtenissen die als functioneel werden voorspeld, kwamen vaker voor in eiwitregio’s die belangrijk zijn voor interacties, in evolutionair geconserveerde sequenties, en in segmenten die chemische tags herbergen zoals fosforylering of SUMOylatie. Veel van deze gebeurtenissen waren ook alleen actief in specifieke bloedlijnen of tijdens de foetale bloedvorming, wat suggereert dat ze als fijn afgestelde schakelaars in bepaalde ontwikkelingsvensters fungeren. De studie toonde verder aan dat sommige van de oudste splice-gebeurtenissen — die al honderden miljoenen jaren bij gewervelden gemeenschappelijk zijn — bijzonder waarschijnlijk functioneel zijn, in lijn met het idee dat oudere genen vaak kernbiologische rollen vervullen.
Experimenteel bewijs: het bijsturen van bloedceluitkomsten
Om de voorspellingen van het model te testen, kozen de auteurs meerdere hooggescoorde exonen in genen die actief zijn in verschillende bloedlijnen en verwijderden die exonen in muizenbloedstam- en voorlopercellen met CRISPR. De resultaten kwamen overeen met de verwachtingen van het model: het weghalen van bepaalde exonen in de genen KLF6 en SSBP3 verminderde de vorming van myeloïde kolonies zonder de productie van rode bloedcellen te schaden, terwijl het verwijderen van exonen in EPB41L1 en TBC1D23 de erytroïde kolonievorming veranderde. Met name het overslaan van exon 15 van TBC1D23 verminderde de productie van voorlopercellen voor rode bloedcellen in muizen en zebravissen, wat leidde tot minder circulerende rode cellen en lagere hemoglobinewaarden, terwijl witte bloedcellen grotendeels gespaard bleven.
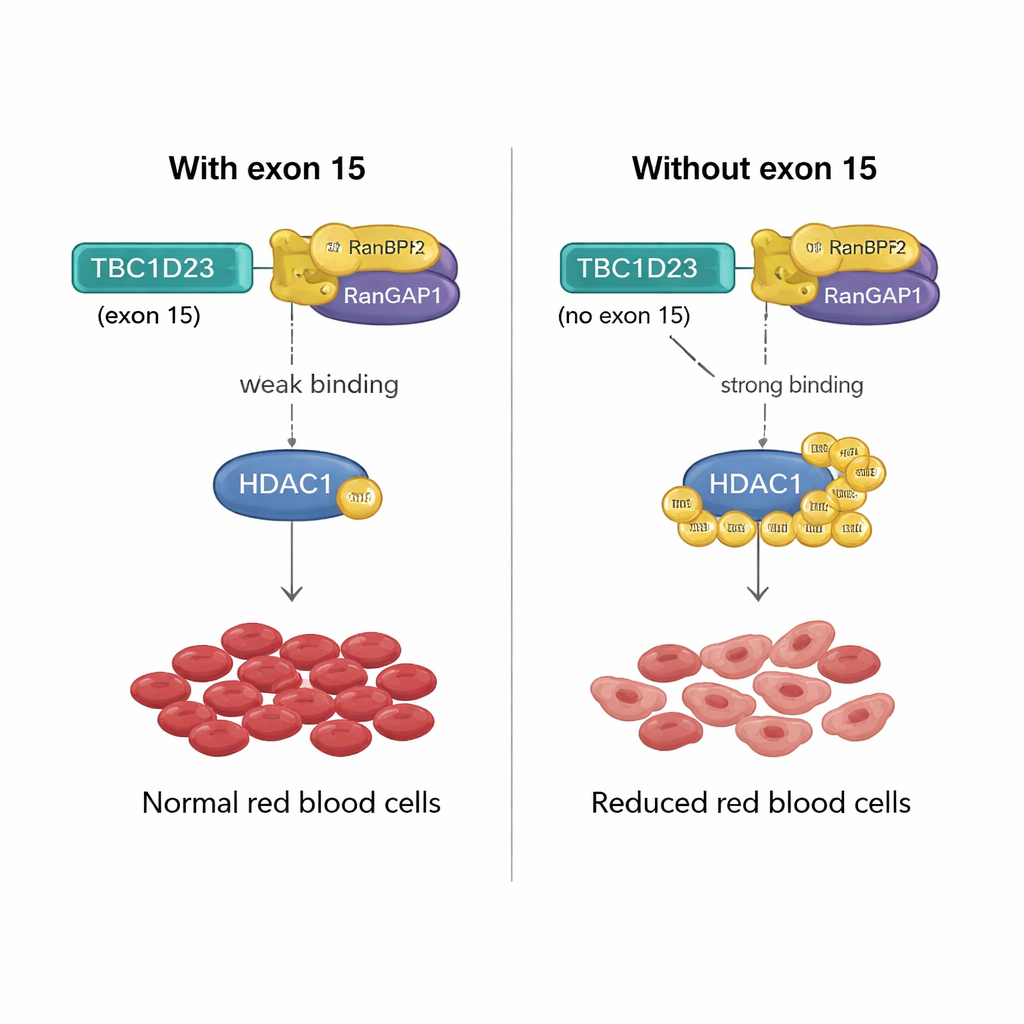
Een moleculaire hefboom voor de aanmaak van rode bloedcellen
Hoe kan een 15-aminozuur lange reeks gecodeerd door exon 15 van TBC1D23 zo’n effect hebben? Het team ontdekte dat het opnemen van dit exon de binding van TBC1D23 aan een eiwitkoppel genaamd RANBP2/RANGAP1 verzwakt, dat samenwerkt om SUMO-tags aan andere eiwitten te bevestigen. Zonder exon 15 bindt TBC1D23 sterkere aan dit koppel, wat de SUMOylatie van een sleutelenzym, HDAC1, versterkt. Deze versterkte etikettering verandert de activiteit van vele transcriptiefactoren — de hoofdregelaars van genexpressie — en verstoort daardoor de genprogramma’s die nodig zijn voor de juiste rijping van rode bloedcellen. Toen de onderzoekers een versie van HDAC1 engineerden die op twee cruciale posities niet SUMO-gelabeld kan worden, herstelde dat de vorming van rode cellen in cellen die exon 15 van TBC1D23 misten, wat bevestigt dat deze chemische tagging de kritische stap is.
Waarom dit belangrijk is voor gezondheid en toekomstige therapieën
Voor niet-specialisten is de boodschap van dit werk dat niet alle genetische veranderingen gelijk zijn: soms ligt het verschil tussen gezond bloed en bloedarmoede in de vraag of een klein segment van een gen in het eindbericht behouden of overgeslagen wordt. Door grootschalige RNA-data te combineren met een verfijnd scoresysteem levert de studie een routekaart om te herkennen welke splice-varianten het meest waarschijnlijk beïnvloeden hoe stamcellen hun loten kiezen. Deze benadering verdiept niet alleen ons begrip van hoe bloedcellen ontstaan in gezondheid en ziekte, maar biedt ook een algemene strategie om belangrijke splice-gebeurtenissen in andere organen te identificeren, wat mogelijk toekomstige gen-gebaseerde therapieën en precisiebehandelingen kan sturen.
Bronvermelding: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Trefwoorden: alternatieve splicing, hematopoëse, machine learning, rode bloedcellen, genregulatie