Clear Sky Science · nl
Structurele basis voor transcriptieregulatie door de celdelingsregulator MraZ in Mycoplasma genitalium
Hoe een piepkleine bacterie bepaalt wanneer ze deelt
Elke levende cel moet beslissen wanneer ze in tweeën splitst, en die beslissing kan het verschil betekenen tussen gezonde groei en ongecontroleerde infectie. Deze studie kijkt in één van de meest eenvoudige bekende bacteriën, Mycoplasma genitalium, en onthult op atomair niveau hoe een enkel eiwit, MraZ genoemd, zich aan DNA hecht en sleutelgenen voor celdeling aan- of uitzet. Door dit minimalistische regelsysteem te begrijpen, hopen wetenschappers algemene principes van bacteriële groei te ontrafelen die op termijn nieuwe typen antibiotica of synthetische "minimale cellen" kunnen inspireren.
Een uitgeklede cel met grote lessen
Mycoplasma genitalium is beroemd om zijn kleine genoom: slechts een fractie van het DNA dat voorkomt in gebruikelijke bacteriën zoals E. coli. Die kleine omvang maakt het een krachtig model om uit te zoeken welke genen en regelsystemen echt essentieel zijn voor leven. Veel bacteriën bewaren hun celdelings- en celwandgenen bij elkaar in een cluster dat dcw wordt genoemd. In wandloze mycoplasma’s zijn de meeste van die genen verdwenen, maar een paar zijn gebleven, waaronder mraZ helemaal aan het begin van de cluster. MraZ fungeert als een verkeersregelaar en beheert de activiteit van zijn naburige genen, die op hun beurt bepalen hoe en wanneer de cel deelt.
Een herhaald DNA-patroon als schakel
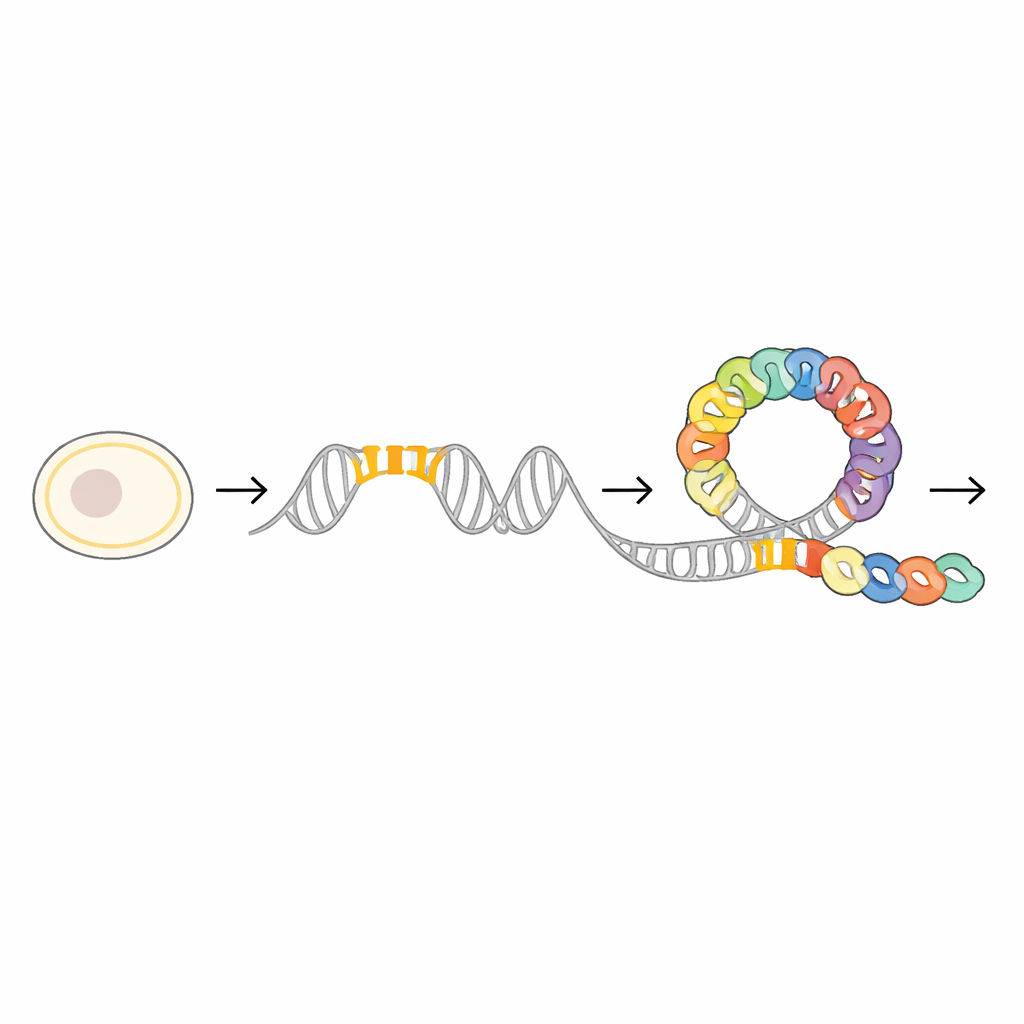
Een ringvormig eiwit dat opent om DNA te omvatten
Om te zien hoe dit regelpaneel op atomair niveau werkt, gebruikten de wetenschappers kryo-elektronenmicroscopie en röntgendiffractie om meerdere driedimensionale structuren van MraZ alleen en gebonden aan DNA op te lossen. Op zichzelf vormen MraZ-moleculen ringachtige assemblages van acht of negen identieke subunits. Deze ringen hebben een kenmerkend "wieglijk" oppervlak gevormd door een kleine beta-sheetstructuur, anders dan de spiraalvormige helices die vaak bij DNA-bindende eiwitten worden gezien. Wanneer MraZ zijn vier-vakjes-DNAsegment ontmoet, gaat de ring niet simpelweg bovenop de helix zitten; in plaats daarvan buigt hij open en herschikt zich zodat vier van zijn subunits langs het DNA uitlijnen, elk één vakje in de major groove wiegend.
Sleutelcontactpunten die de DNA-code lezen
De hoogresolutionele structuren toonden dat elke DNA-contactmakende subunit drie positief geladen zijketens gebruikt—specifieke punten op het eiwitoppervlak—om de DNA-sequentie te lezen. Deze chemische "vingers" reiken in de groeve van de dubbele helix en vormen precieze waterstofbruggen met bepaalde basenparen in de geconserveerde vakjes. Toen de onderzoekers één van deze drie residuen wijzigden, verloor MraZ grotendeels zijn vermogen om aan DNA te binden en het proefreportergen stil te leggen. Aanvullende contacten met de suikerruggengraat van het DNA helpen het complex te stabiliseren maar zijn minder sequentiespecifiek. Samen laten deze bevindingen zien hoe MraZ een sterk gespecialiseerd leesgedeelte combineert met een flexibel multi-subunit lichaam om zijn doelregio te herkennen. 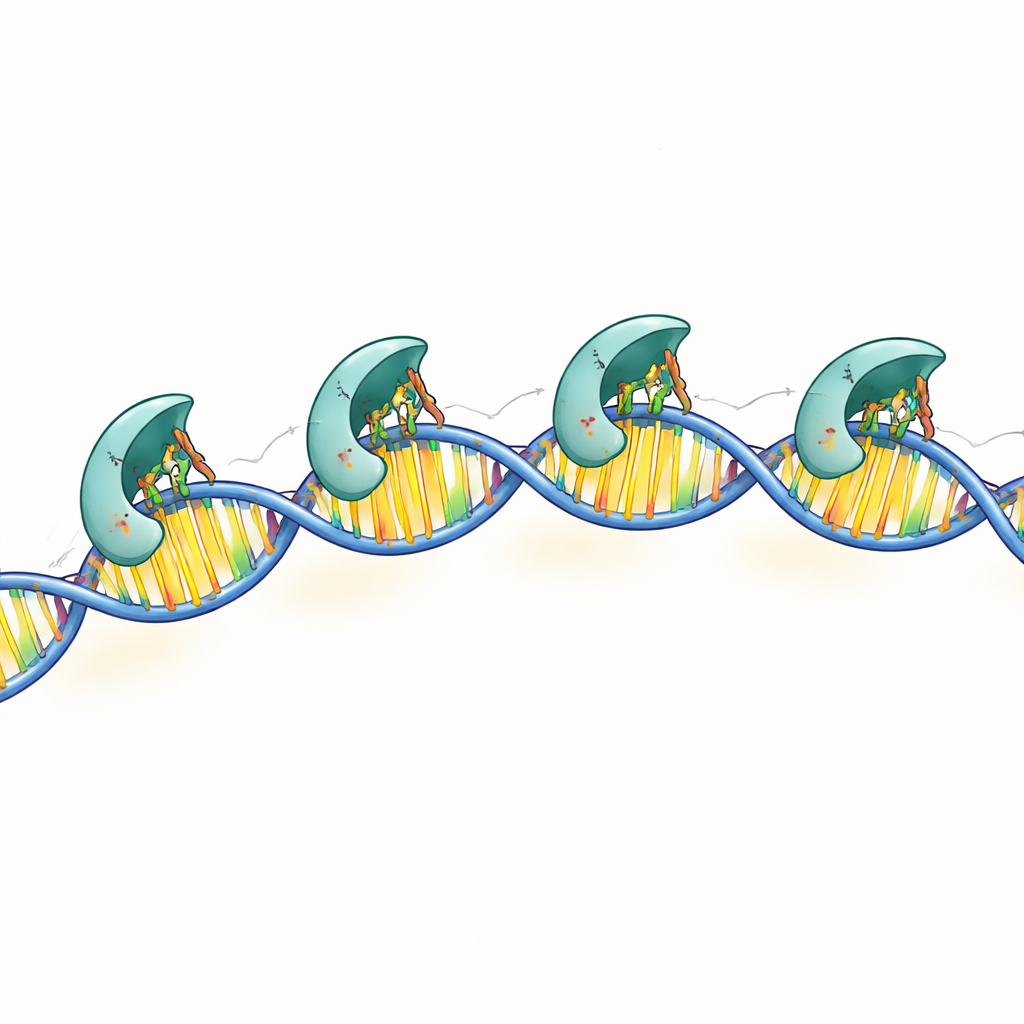
Oligomeren die de sterkte van controle bijstellen
Omdat MraZ ringen en andere multi-eenheidsvormen vormt, vroegen de onderzoekers zich af of deze clustering noodzakelijk is voor DNA-binding of die binding slechts bijstuurt. Door een versie van MraZ te ontwerpen die zich niet langer tot ringen kon samenvoegen, ontdekten ze dat het eiwit nog steeds aan de vier-vakjes-DNAsequentie bond, maar met zwakkere affiniteit. Deze monomere vorm had vooral moeite wanneer de afstand tussen vakjes was veranderd, wat suggereert dat het volledige oligomeer helpt om afgelegen vakjes te overbruggen en uit te lijnen, en zo de lokale concentratie van bindplaatsen langs het DNA verhoogt. De auteurs stellen een dynamisch model voor waarin MraZ schakelt tussen een gesloten ring en een open, met DNA geassocieerde vorm, waarbij de assemblagetoestand fungeert als een regelknop om te bepalen hoe sterk het eiwit op de promotor klemt.
Wat dit betekent voor bacteriën en daarbuiten
In eenvoudige termen verklaart dit werk hoe een klein eiwit in een minimale bacterie een herhaald patroon op DNA vastpakt en gebruikt als hoofdschakel voor celdelingsgenen. De combinatie van een wiegachtig leesgedeelte en een flexibel ringlichaam stelt MraZ in staat zijn doel met hoge precisie te herkennen terwijl het zich aan verschillende DNA-ordningen kan aanpassen. Omdat soortgelijke eiwitten en DNA-motieven in veel bacteriën voorkomen, is de hier onthulde mechaniek waarschijnlijk een gedeelde strategie om groei en deling te coördineren. Inzichten uit dit uitgeklede systeem kunnen onderzoekers helpen bij het ontwerpen van gestroomlijnde genetische circuits in synthetische cellen en op de lange termijn bijdragen aan nieuwe manieren om bacteriële groei bij ziekte te verstoren.
Bronvermelding: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Trefwoorden: bacteriële celdeling, DNA–eiwitinteractie, transcriptieregulatie, kryo-elektronenmicroscopie, Mycoplasma genitalium