Clear Sky Science · nl
Cellulaire en transcriptie-trajecten van neurale bestemmingsspecificatie in zeeanemonen onthullen twee modi van volwassen neurogenese
Hoe een eenvoudig zeediertje constant nieuwe hersencellen blijft maken
De meeste dieren, waaronder mensen, vormen het merendeel van hun neuronen vroeg in het leven en stoppen daarna grotendeels. Toch blijven sommige ogenschijnlijk eenvoudige organismen, zoals zeeanemonen, gedurende hun volwassen leven nieuwe zenuwcellen toevoegen. Deze studie onderzoekt hoe de zeesteranemoon (Nematostella vectensis) haar diffuse zenuwstelsel voortdurend vernieuwt en herschaalt, en onthult strategieën die mogelijk echo’s zijn van oude oplossingen voor het laten groeien en herstellen van hersenen.
Een groeiend lichaam heeft een groeiend zenuwnet nodig
Zeeanemonen hebben geen hersenen; in plaats daarvan hebben ze een webachtig zenuwnet verspreid door hun lichaamswand. Terwijl deze dieren groeien of krimpen afhankelijk van voedselbeschikbaarheid, moet hun zenuwnet meeschalen. Met een lichtgevoelig fluorescerend eiwit als tijdstempel markeerden de auteurs bestaande neuronen in jong-volwassen dieren en observeerden vervolgens de nieuwgeboren cellen die in de daaropvolgende week verschenen. Ze vonden talrijke nieuwe neuronen verspreid langs de lichaamsas, niet beperkt tot een speciale groeizone. Deze verse cellen verschenen zowel aan de mondzijde als aan de tegenovergestelde kant van het dier, wat aantoont dat volwassen neurogenese ruimtelijk wijdverspreid en aanhoudend is.
De oorsprong van nieuwe zenuwcellen traceren
Om te achterhalen waar deze nieuwe neuronen vandaan komen, combineerden de onderzoekers live-imaging met single-cell RNA-sequencing, een techniek die leest welke genen actief zijn in duizenden individuele cellen. Ze concentreerden zich op cellen met fluorescerende "reporters" die worden aangestuurd door drie sleutelgenen: FoxL2, SoxC en Elav. FoxL2 markeert een brede pool van delende, multipotente progenitorcellen; SoxC wordt kort geactiveerd zodra cellen beginnen te specialiseren; en Elav is sterk actief in peptiderge neuronen, die voornamelijk communiceren via kleine signaalpeptiden. Het team toonde aan dat een populatie FoxL2-positieve, Piwi1-positieve progenitorcellen zich gedraagt als stamcellen: zij vernieuwen zichzelf terwijl ze continu diverse afstammelingen genereren, waaronder neuronen, stekende cellen genaamd cnidocyten, en secretorische cellen. SoxC en Elav worden daarentegen alleen geactiveerd wanneer cellen deze progenitorpool verlaten en zich aan specifieke neurale bestemmingen toewijden.
Twee verschillende wegen naar volwassen neuronen
Door de timing van de reporters te koppelen aan het genexpressieprofiel van elke cel, ontdekte de studie twee duidelijke routes naar rijpe neurale cellen. Peptiderge neuronen volgen een directe weg: ze ontstaan uit progenitoren die al een "peptidergisch-gecommitteerd" moleculair profiel dragen en differentiëren vervolgens snel in een verscheidenheid aan neuronaal subtypes. Nieuwe leden van elk subtype verschijnen in verhouding tot hoe algemeen dat subtype al is, wat suggereert dat het systeem een evenwichtige mix van neuronale types onderhoudt in plaats van bepaalde types te bevoordelen. In deze afstammingslijn is er geen duidelijke reeks tussenstations; in plaats daarvan ontstaan nauw verwante neuronaal subtypes parallel uit vergelijkbaar geprimede progenitorcellen. 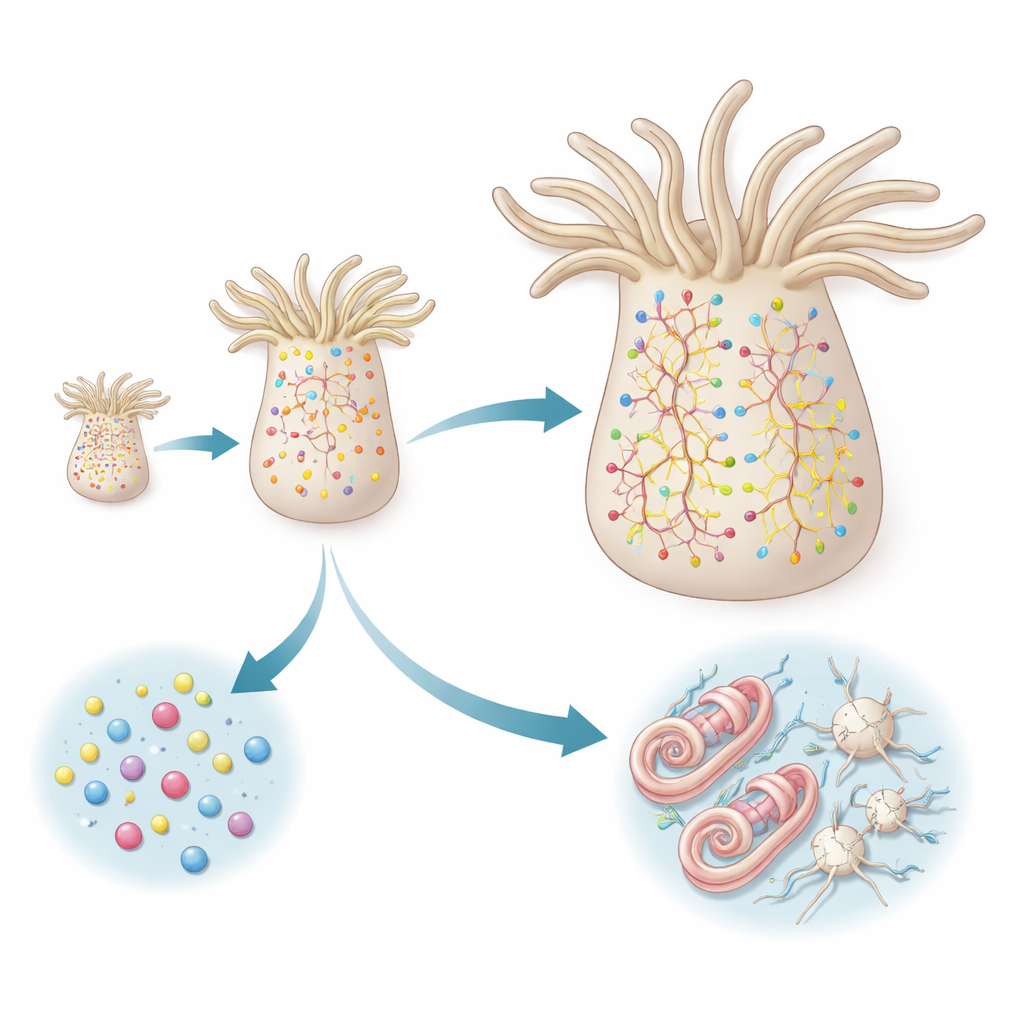
De bijzondere zaak van stekende cellen
Cnidocyten, de stekende cellen die uniek zijn voor cnidariërs, volgen een meer stapsgewijze route. Ze doorlopen eerst een "capsule-bouwfase", waarin ze hun karakteristieke onder druk staande organellen opbouwen die een microscopisch harpoen kunnen afvuren. Deze fase vereist een specifieke set regulatorische genen en structurele eiwitten die grotendeels afwezig zijn in andere celtypen. Pas nadat dit tussentijdse programma is voltooid, schakelen cnidocyten een tweede, meer conventioneel neuronaal programma in, waarbij ionkanalen en andere componenten voor elektrische signalering worden toegevoegd. Genetische gegevens uit mutanten die in de vroege fase vastlopen versterken dit tweefasenmodel: het blokkeren van de overgang voorkomt dat de latere neurale kenmerken verschijnen. 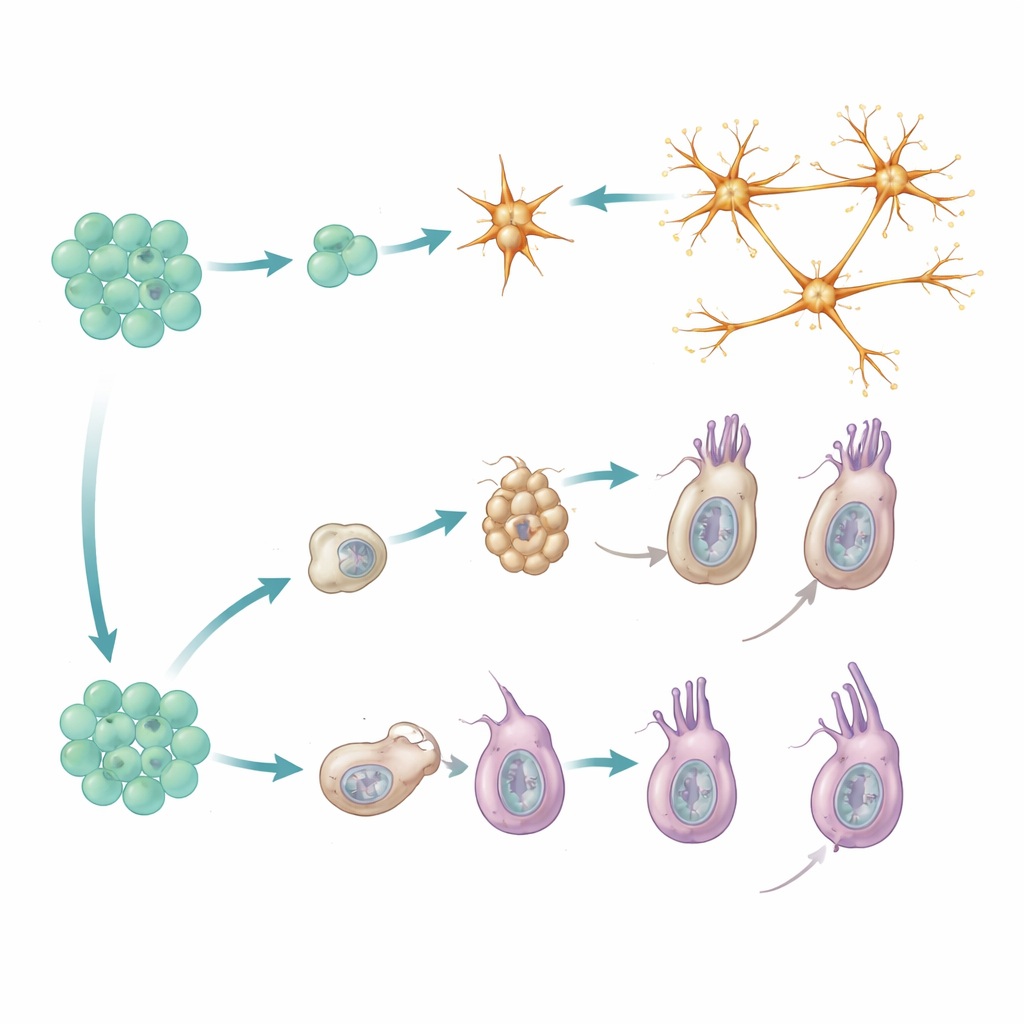
Gedeelde regels en oude wortels
Ondanks hun verschillende routes vertrouwen peptiderge neuronen en cnidocyten op overlappende families van regulatorische genen om hun identiteit vast te leggen. Brede neurale kenmerken correleren met bHLH- en bZIP-transcriptiefactoren, terwijl de fijnmazige identiteit van elk neuronaal subtype wordt gespecificeerd door unieke combinaties van homeodomein- en zinkvingergenen — een "code" die doet denken aan hoe neurontypen worden gedefinieerd in complexere dieren, waaronder wormen en gewervelden. De auteurs stellen dat deze modulaire strategieën — stamachtige progenitoren, transiënte SoxC-activiteit tijdens toewijding, en subtype-definiërende homeodomeincodes — mogelijk diep geconserveerde principes van neurogenese vertegenwoordigen. Bij zeeanemonen ondersteunen ze levenslange vernieuwing en opschaling van het zenuwnet; bij andere dieren kunnen verwante mechanismen zowel beperkte volwassen neurogenese als de opmerkelijke regeneratieve vermogens in sommige lijnen onderbouwen.
Bronvermelding: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Trefwoorden: volwassen neurogenese, zeeanemoon, neurale progenitorcellen, cnidocyten, single-cell transcriptomics