Clear Sky Science · nl
Aflevering van peptide-coacervaten om stabiele interactiehubs in cellen te vormen
Nieuwe “werkstations” binnen cellen bouwen
Onze cellen zitten vol kleine werkruimtes waar belangrijke taken—zoals energieproductie of stressreacties—plaatsvinden. In de loop van de tijd, of bij ziekte, kunnen deze natuurlijke werkstations minder goed functioneren. In deze studie wordt onderzocht hoe je gloednieuwe “interactiehubs” in levende cellen kunt brengen met eenvoudige, in het lab gemaakte druppels opgebouwd uit korte peptiden. Deze synthetische hubs kunnen specifieke eiwitten vangen, concentreren en zelfs helpen afbreken, wat nieuwe strategieën suggereert voor toekomstige therapieën en celengineering.
Waarom cellen aangepaste werkruimtes nodig hebben
Cellen houden orde door verschillende taken in afzonderlijke compartimenten te scheiden. Sommige compartimenten zijn omgeven door membranen, zoals mitochondriën; andere zijn zachtere, druppelachtige structuren die ontstaan wanneer bepaalde eiwitten en RNA’s samenklonteren. Deze fluïde druppels, of condensaten, fungeren als reactieve centra die bepaalde biochemische routes versnellen of uitschakelen. Wetenschappers hebben eerder zulke compartimenten geïmproviseerd door cellen speciale scaffold-eiwitten te laten maken via ingevoegde genen. Hoewel krachtig, vereist die methode genlevering en beperkt het hoeveel materiaal de cel kan produceren. De auteurs van deze studie wilden DNA helemaal omzeilen en in plaats daarvan kant-en-klare compartimenten buiten de cel bouwen en die direct afleveren als stabiele, micrometers grote druppels.
Peptide-druppels die stabiele hubs vormen
Het team werkte met korte, gedesordeerde peptiden bekend als HBpep en een redox‑gevoelige variant, HBpep‑SA. Onder licht zure omstandigheden blijven deze peptiden opgelost, maar wanneer de pH naar ongeveer fysiologische waarden verschuift—of wanneer de temperatuur verlaagd wordt—scheiden ze in fasen en vormen zachte, gelachtige druppels van ongeveer 1–5 micrometer. Door de peptideconcentratie aan te passen konden de onderzoekers zowel de grootte als het aantal druppels regelen. Met fluorescentietechnieken toonden ze aan dat peptidemoleculen in deze druppels langzaam bewegen, wat duidt op een geltoestand die stevig genoeg is om verdunning en behandeling te doorstaan. Wanneer ze aan culturen van menselijke kankercellen, muismelanomacellen en primaire menselijke immuuncellen werden toegevoegd, werden de druppels efficiënt opgenomen en stapelden ze zich op in het cytoplasma. Vooral grotere druppels bleven ten minste vijf dagen intact en fungeerden zo als langlevende synthetische organellen binnen levende cellen.
Beladen en richten van de hubs
Om nuttig te zijn moeten deze hubs ladingen vast kunnen houden en ordenen. De onderzoekers verbeterden eerst het laden door een korte HBpep‑afgeleide tag aan een modelproteïne, GFP, te koppelen. Deze tag stimuleerde GFP om sterk in de druppels te partitioneren en, wat interessant is, zich te concentreren nabij hun oppervlakken, waardoor een kern‑schilorganisatie ontstond. Vervolgens plaatsten ze nanobodies—compacte, antilichaamachtige eiwitten die sterk aan gekozen doelwitten binden—binnen de druppels. Een GFP‑bindende nanobody stelde de hubs in staat om GFP selectief te vangen zowel in buisjes als binnen cellen. Omdat de peptidegel relatief dicht is, verzamelde het grootste deel van het gevangen GFP aanvankelijk aan het druppeloppervlak. Maar wanneer de interne structuur gedeeltelijk werd losgemaakt, hetzij door redoxomstandigheden te veranderen, hetzij door de druppels te helpen ontsnappen uit omringende endosomale membranen, begon GFP ook het interieur binnen te dringen. In cellen verhoogden chemische hulpstoffen die endosomale ontsnapping bevorderen sterk het aandeel hubs dat succesvol hun doelwitten rekruteerde.
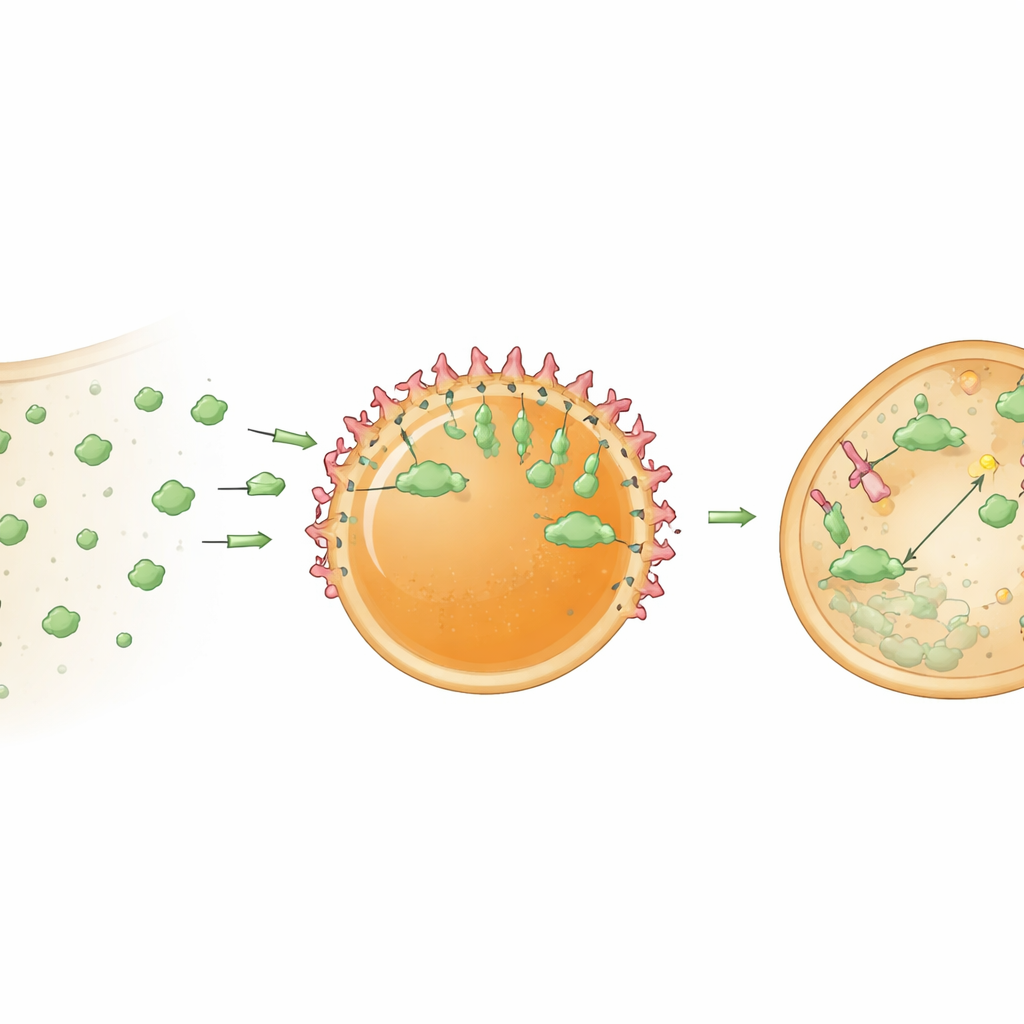
Hubs omvormen tot eiwitverwerkers
De auteurs upgradeden deze hubs vervolgens van passieve vallen naar actieve verwerkingscentra. Ze beladen de druppels met een bioPROTAC—een fusie-eiwit dat een doelbindende nanobody combineert met een deel van een enzymadapter die eiwitten markeert voor vernietiging door het cellulaire afvalverwijderingssysteem. Wanneer deze “degradosoom”‑druppels in cellen werden gebracht die stabiel GFP tot expressie brachten, daalde het cytosolische GFP‑niveau met ongeveer 78 procent binnen een dag. Controlehubs die alleen de nanobody bevatten, sequestreerden GFP maar verlaagden het totale niveau niet merkbaar, wat bevestigt dat de sterke afname voortkwam uit gerichte degradatie in plaats van loutere vangst. De bevindingen suggereren dat het clusteren van bioPROTACs in een geconcentreerde microomgeving ze veel krachtiger maakt dan wanneer ze vrij in het cytoplasma verspreid zijn.
Wat dit kan betekenen voor toekomstige therapieën
Kort gezegd toont dit werk aan dat wetenschappers peptide‑gebaseerde druppels in een reageerbuis kunnen fabriceren, ze kunnen vullen met aangepaste eiwitgereedschappen en ze vervolgens in levende cellen kunnen afleveren waar ze zich gedragen als nieuwe, langlevende organellen. Deze synthetische hubs kunnen selectief natuurlijke eiwitten aantrekken en, wanneer uitgerust met afbraakmachinerie, actief gekozen doelwitten uit de cel verwijderen. Omdat dit platform vermijdt het genoom van de cel te wijzigen en modulair is in wat het kan dragen, opent het een pad naar therapieën die cellair gedrag herstellen of herschrijven—zoals het opruimen van schadelijke eiwitten of het herbekabelen van defecte signaalroutes—door simpelweg nieuwe, programmeerbare “werkstations” in onze cellen te installeren.
Bronvermelding: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Trefwoorden: synthetische organellen, peptide-coacervaten, intracellulaire levering, eiwitafbraak, celengineering