Clear Sky Science · nl
CRISPR-Cas9 trans-splitsel wordt belemmerd door een omgeven R-loop, een verlengde spacer en een inactieve HNH-domain
Waarom kleine DNA-sneden ertoe doen
CRISPR-Cas9 staat bekend als een moleculair scalpel die DNA op gekozen plaatsen kan knippen, maar dit gereedschap heeft een tweede, minder bekende eigenschap: eenmaal geactiveerd kan het ook aan andere stukjes genetisch materiaal in de buurt knabbelen. Begrijpen wanneer deze "nevensnijding" aan- of uitgaat is cruciaal om veiligere genbewerkingstherapieën en gevoeliger diagnostiek te ontwikkelen. Deze studie ontleedt de fysieke kenmerken van het Cas9–DNA–RNA-complex die bepalen of Cas9 alleen zijn bedoelde knip maakt, of ook begint andere enkelstrengs DNA-fragmenten af te breken.
Hoe de CRISPR-schaar op gang komt
Om te werken bindt Cas9 een kort stukje gids-RNA dat het naar een bijpassende DNA-sequentie in een genoom stuurt. Wanneer Cas9 zijn doel vindt, paart het gids-RNA met één DNA-streng, waardoor de twee strengs uit elkaar worden geduwd en een DNA–RNA-hybride regio ontstaat die een R-loop wordt genoemd. In zijn klassieke rol knipt Cas9 vervolgens beide DNA-strengen op die plek. Maar recent werk toonde aan dat zodra Cas9 op deze wijze geactiveerd is, het RuvC-knipdomein ook niet-gerelateerde enkelstrengs DNA kan doorsnijden, zoals poly(T)-reeksen, elders in de oplossing. De auteurs vroegen zich af: welke exacte geometrische en structurele kenmerken van het doel-DNA en het gids-RNA maken deze nevensnijding sterk, zwak of afwezig?
Korte versus lange doelen: ruimte geven aan Cas9
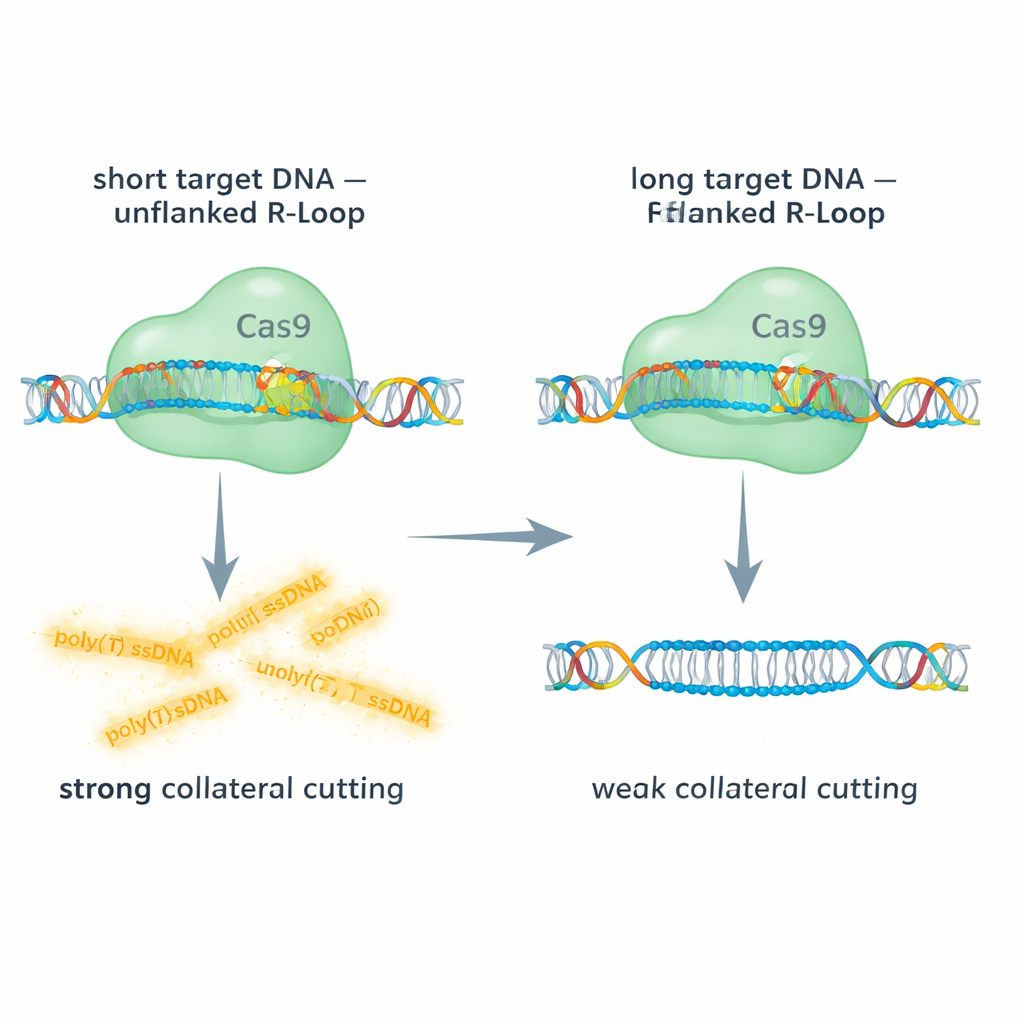
Het team vergeleek Cas9 dat werkt op korte en lange dubbelstrengs DNA-doelen, met behulp van fluorogene signalen om zowel de on-target knip als de nevensnijding van een enkelstrengs DNA-probe te volgen. Bij korte DNA-doelen is de R-loop aan het 5′-einde van het gids-RNA "onomgeven" — er is geen extra dubbelstrengs DNA dat voorbij de hybride regio doorloopt. Onder deze omstandigheden toonde Cas9 robuuste nevensnijding van enkelstrengs DNA. In contrast, wanneer ze langere DNA-segmenten gebruikten die extra dubbelstrengs DNA naast de R-loop lieten liggen, daalde de nevensnijding dramatisch, soms met ongeveer 90%, hoewel de belangrijkste on-target knip nog steeds plaatsvond. Gericht op lange enkelstrengs DNA, wat de R-loop volledig wegneemt, herstelde de nevensnijding grotendeels. Deze vergelijkingen laten zien dat een dubbelstrengs "kap" naast de R-loop het complex verstevigt en fysiek de toegang of flexibiliteit belemmert die nodig is voor Cas9’s RuvC-domein om andere strengen te knippen.
Fijnregeling met gidslengte en mismatches
De onderzoekers onderzochten vervolgens hoe het gids-RNA dit gedrag afstemt. Ze introduceerden kleine mismatches tussen de gids en het doel-DNA en volgden hoe goed Cas9 nog steeds knipte. De voornaamste on-target knip verdroeg veel enkelvoudige basismismatches, maar nevensnijding was fragieler en hing sterk af van de precieze locatie van de mismatch, wat de gevoeligheid benadrukt. Daarna verlengden ze systematisch de gids-RNA-spacer voorbij de gebruikelijke 20 bouwstenen. Hoewel Cas9 het doel-DNA nog steeds kon binden en knippen, nam de nevensnijding bijna lineair af met toenemende spacerlengte: het toevoegen van slechts twee extra basen halveerde de nevensnijding ongeveer, en vier extra basen verminderden die nog verder. In praktische tests met SARS-CoV-2-genetisch materiaal gaven alleen DNA-amplicons die zo waren opgesteld dat ze een onomgeven R-loop produceerden met een gids van standaardlengte een sterk nevensnijdingssignaal, wat benadrukt hoe primer- en gidsontwerp CRISPR-gebaseerde detectieassays kunnen maken of breken.
Een essentiële helperdomein achter de schermen
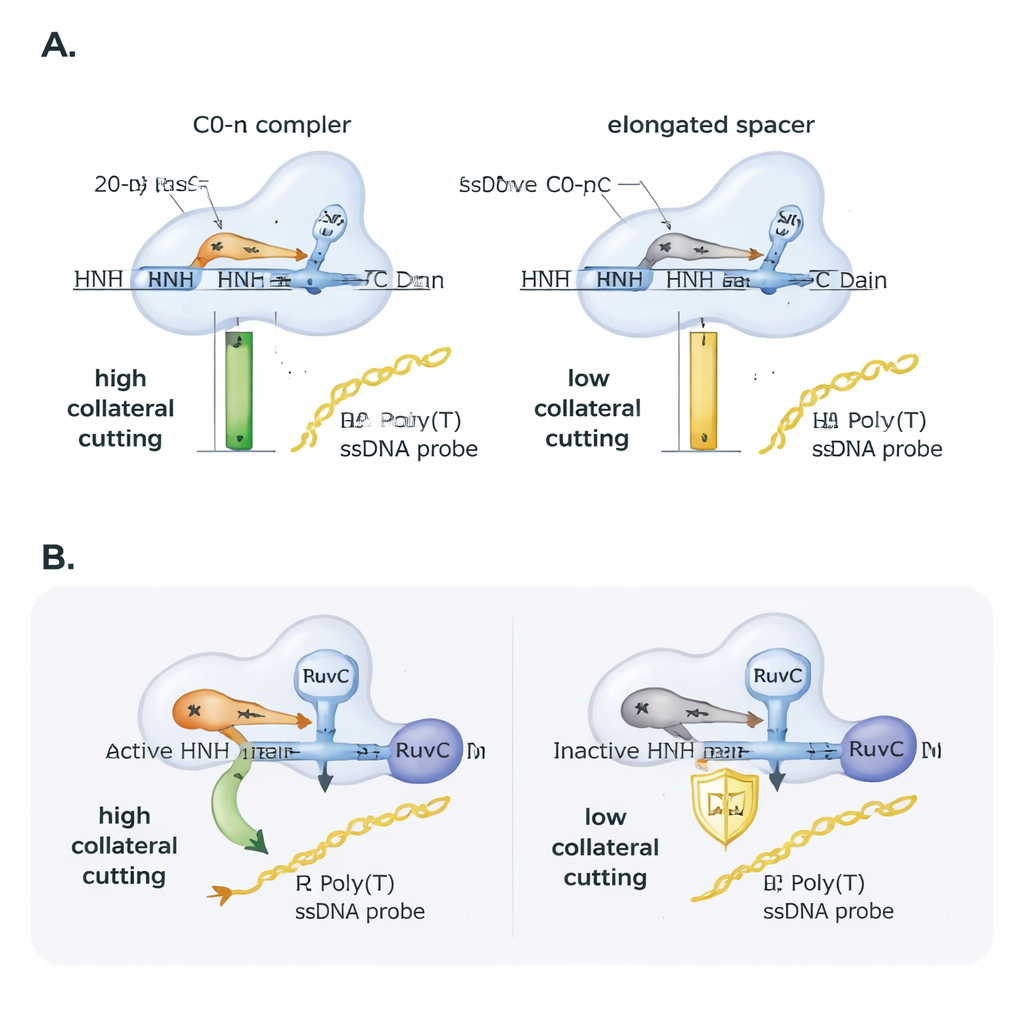
Cas9 heeft twee knipdomeinen, RuvC en HNH. Eerder werk koppelde nevensnijding direct aan RuvC, maar deze studie toont aan dat HNH toch van belang is. Wanneer de auteurs een Cas9-variant met een inactief HNH-domein gebruikten, daalde de nevensnijding sterk, hoewel binden aan het doel en nicks in het DNA bleven bestaan. Interessant genoeg herwon de inactieve-HNH-variant de nevensnijding vergelijkbaar met het normale enzym als ze Cas9 een DNA-doel gaven dat al in één streng was genaaid (genickt). Dit suggereert dat de rol van HNH deels mechanisch is: door de getargete streng te knippen of losser te maken helpt het eiwit zich te vormen in een conformatie die RuvC blootstelt aan nabijgelegen enkelstrengs DNA. Structurele analyses van bestaande 3D-modellen ondersteunden dit beeld en toonden dat onomgeven R-loops en gidsen van standaardlengte het 5′-einde van het RNA tegen Cas9 kunnen laten "kapen" en de katalytische regio’s gunstig positioneren, terwijl omgeven R-loops en verlengde gidsen het eiwit compacter pakken en waarschijnlijk het RuvC-terrein tegen losse strengen afschermen.
Wat dit betekent voor toekomstige gereedschappen
Voor niet-specialisten is de belangrijkste boodschap dat het gedrag van Cas9 geen alles-of-niets is: kleine geometrische details — hoe ver het DNA doorloopt, hoe lang de gids is en of een helperdomein zijn knip kan voltooien — bepalen of het enzym zich aan zijn hoofdtaak houdt of ook nabijgelegen enkelstrengen versnippert. Korte doelen die de R-loop onomgeven laten, gidsen van standaard 20 basen en een actief HNH-domein bevorderen samen sterke nevensnijding; lang aangehecht DNA, uitgerekte gidsen of een inactief HNH-domein onderdrukken die activiteit. Deze inzichten geven onderzoekers een preciezer regelmechanisme om Cas9 af te stemmen, waardoor ze veiliger genbewerking kunnen ontwerpen die ongewenste nevenschade vermijdt, of krachtigere diagnostische assays die deze nevensnijding doelbewust benutten om zeer kleine hoeveelheden viraal of genetisch materiaal op te sporen.
Bronvermelding: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Trefwoorden: CRISPR-Cas9, nevensnijding, R-loop, gids RNA spacer, nucleïnezuurdiagnostiek