Clear Sky Science · nl
Collageenbindende adhesine beperkt huidinfectie door Staphylococcus aureus
Waarom het “klittenband” van een huidbacterie ertoe doet
Staphylococcus aureus is de belangrijkste oorzaak van pijnlijke huidpuistjes en abcessen, en medicijnresistente stammen zoals MRSA maken deze infecties moeilijk te behandelen. Deze studie onderzoekt een onverwachte wending: een bacterieel oppervlakte-eiwit genaamd Cna dat fungeert als klittenband voor collageen, het belangrijkste structurele eiwit van de huid en wonden. In plaats van infecties te verergeren, blijkt dit collageen-grijpende eiwit de huidaandoening bij muizen juist te verzachten door te bepalen hoe immuuncellen de bacteriën aanvallen.
Een kleverig eiwit met een verrassende rol
Collageen is het meest voorkomende eiwit in ons lichaam en essentieel om de huid bij elkaar te houden en wonden te laten helen. Sommige S. aureus-stammen dragen Cna, een eiwit dat in de bacteriële celwand verankerd zit en sterk bindt aan collageen en aan een collageenachtig staartstuk van een bloedproteïne genaamd C1q. C1q helpt normaal gesproken microben te markeren voor vernietiging door het immuunsysteem. Eerder onderzoek koppelde Cna aan ernstige infecties in gewrichten en ogen, maar de rol ervan bij huidaandoeningen was onduidelijk. De onderzoekers gebruikten een muismodel voor huidabcessen en genetisch gemodificeerde bacteriën die óf Cna maakten, het misten, of het terugkregen via een plasmide, om te onderzoeken hoe deze enkele adhesine het verloop van de infectie verandert.
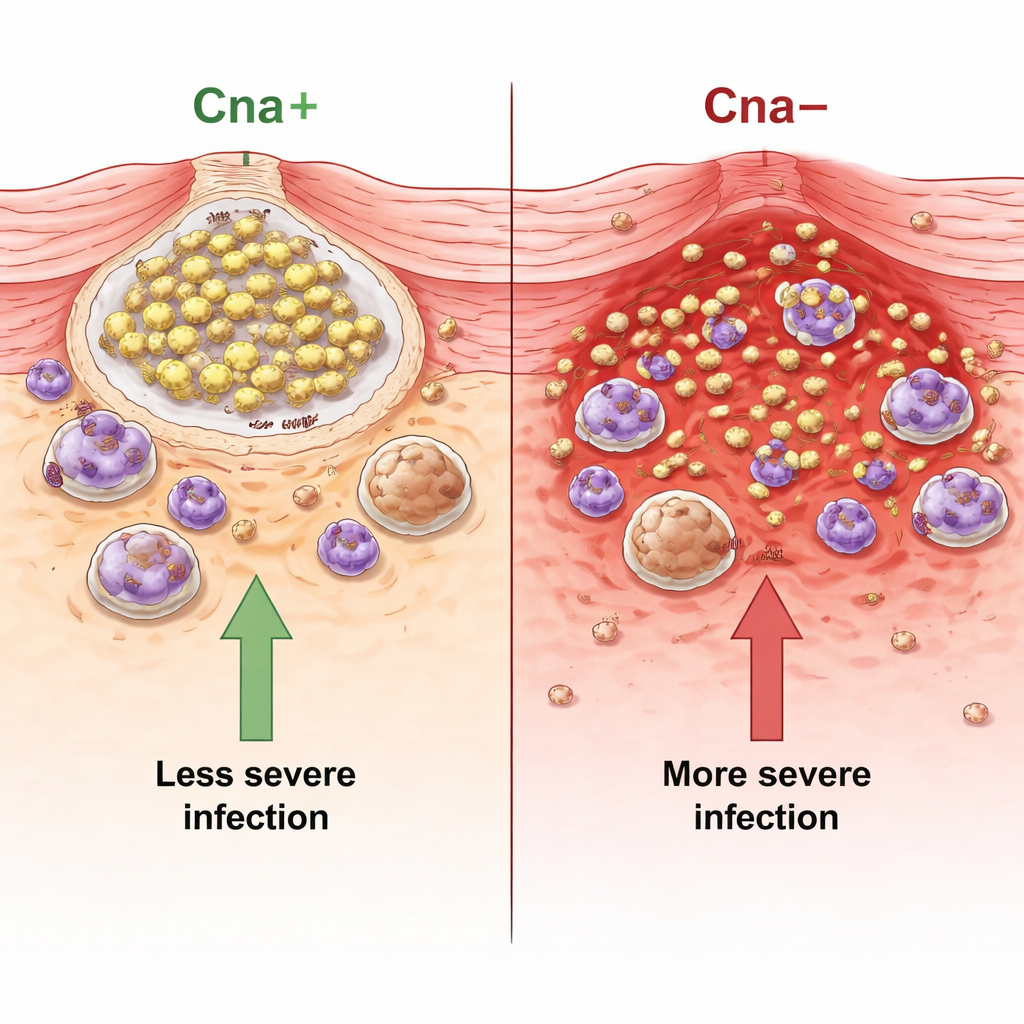
Als bacteriën collageen niet kunnen grijpen, worden infecties erger
Bij muizen die geïnjecteerd werden met Cna-positieve S. aureus bleven de huidlaesies kleiner, verloren de dieren minder gewicht en werden veel minder bacteriën uit de abcessen teruggevonden dan bij muizen die geïnfecteerd waren met Cna-negatieve mutanten. Het herstellen van Cna keerde deze effecten om, wat toonde dat het eiwit zelf verantwoordelijk was. Het team testte ook USA300, een veelvoorkomende MRSA-stam die van nature geen Cna heeft en berucht is bij menselijke huidinfecties. Ook bij deze stam verminderde het toevoegen van Cna de laesiegrootte en het aantal bacteriën. Inventarisaties van patiëntisolaten van huidinfecties, neusdragers en longontstekingen toonden aan dat de meeste circulerende S. aureus-stammen het cna-gen helemaal niet dragen, wat suggereert dat het verliezen van dit eiwit juist agressievere, zich verspreidende ziekte kan bevorderen.
Hoe collageen bacteriën beschermt en ontsteking tempert
Weefseldoorsneden van muizenabcessen vertelden een duidelijk verhaal. Infecties met Cna-positieve bacteriën lieten compacte bacteriële clusters zien omwikkeld door collageen, met immuuncellen zoals neutrofielen en macrofagen aan de randen. Cna-negatieve infecties waren daarentegen rommelig en infiltrerend, vol dode immuuncellen en intense ontsteking. Chemische analyse van het weefsel toonde aan dat Cna-negatieve infecties hogere niveaus van ontstekingssignalen zoals IL-6, TNF-α en IL-1β veroorzaakten, en van enzymen genaamd matrixmetalloproteases (MMP-9 en MMP-12) en de lipidemediator leukotrieen B4, die allemaal de instroom van immuuncellen en weefselschade versterken. Flowcytometrie en beeldvorming bevestigden dat neutrofielen in Cna-negatieve abcessen veel vaker dood of stervend waren, terwijl levende immuuncellen relatief schaars waren.
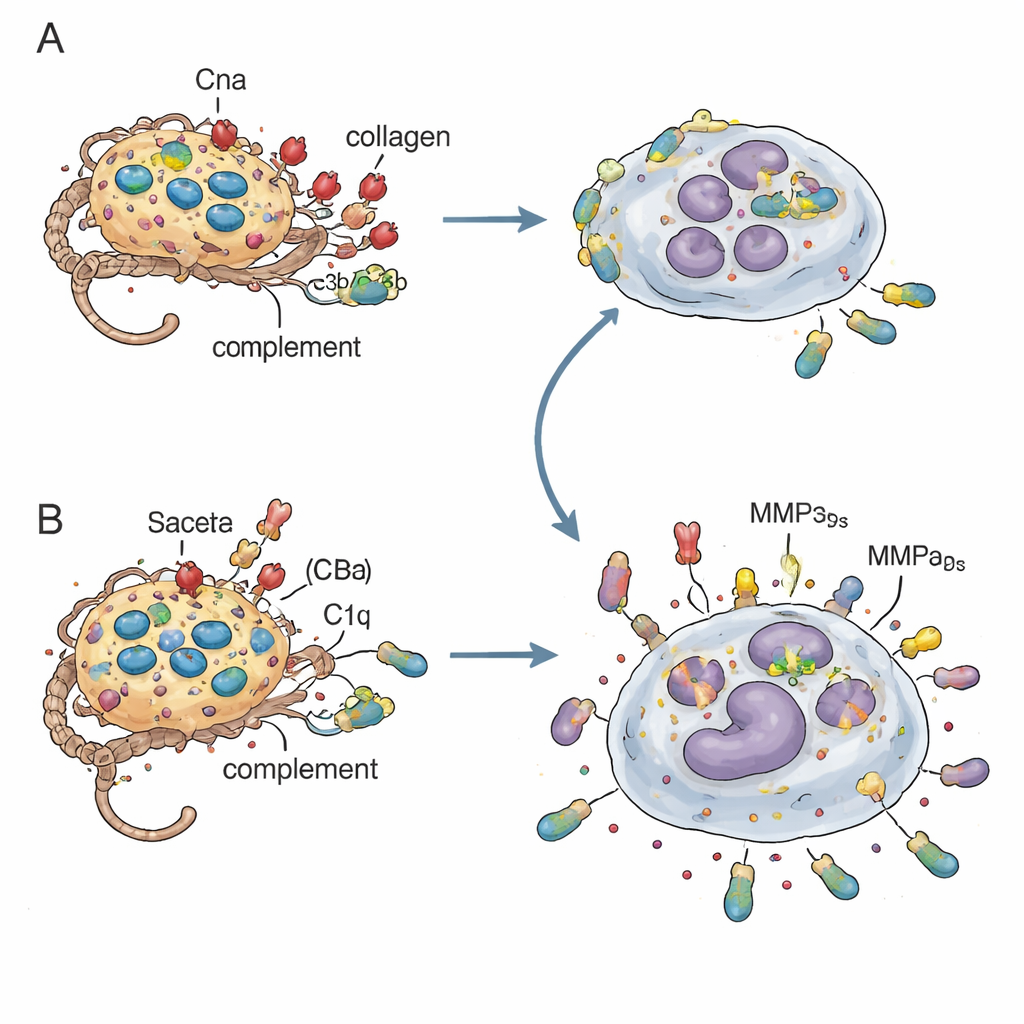
Het complementsysteem kapen om een dodelijke omhelzing te vermijden
De sleutel-mechanistische schakel was C1q, een startmolecule van het complementsysteem die bacteriën coating geeft zodat neutrofielen ze kunnen opnemen. In proefbuisexperimenten stapelden bacteriën zonder Cna meer complementcomponenten (C4b en C3b) op hun oppervlak op en werden ze door menselijke neutrofielen actiever opgenomen. Maar deze overdreven opname liep uit op een averechts effect: neutrofielen volgeladen met Cna-negatieve bacteriën neigden te lysere, waardoor levende bacteriën en ontstekingsmoleculen terug in het weefsel werden vrijgegeven. Toen de onderzoekers serum zonder C1q gebruikten, of muizen genetisch zonder C1q, werden de verschillen tussen Cna-positieve en Cna-negatieve infecties kleiner, wat aantoont dat Cna’s binding aan de collageenachtige staart van C1q het complementstagging dempt en de overreactie van neutrofielen tempert. Tegelijkertijd lijkt collageen dat rond Cna-positieve bacteriën gebonden is een fysieke barrière te vormen, waardoor direct contact met neutrofielen vertraagt en gecontroleerdere doding mogelijk wordt.
Verdediging en schade in balans bij huidinfecties
Voor niet‑specialisten is de hoofdboodschap dat niet alle bacteriële “plakkerigheid” infecties verergert. In dit geval roepen S. aureus-stammen die aan collageen en C1q kunnen blijven hangen een meer gedoseerde immuunreactie op: minder neutrofielen gaan explosief dood, de ontsteking is lager en huidschade wordt beperkt, ook al zijn de bacteriën nog aanwezig. Stammen die Cna missen, waaronder veel belangrijke MRSA-clonen, worden gemakkelijker door het complement gemarkeerd, veroorzaken een storm van neutrofiele activiteit en leiden tot grotere, destructievere abcessen. Begrijpen van deze fijne balans tussen bacterieel verbergen en immuunoveryreactie kan nieuwe strategieën informeren om huidinfecties te behandelen—ofwel door te richten op hoe bacteriën interageren met collageen en C1q, of door de ontstekingsenzymen en -lipiden te moduleren die een ingekapseld abces in een schadelijke laesie veranderen.
Bronvermelding: Bhattacharya, M., Spencer, B.L., Kwiecinski, J.M. et al. Collagen binding adhesin restricts Staphylococcus aureus skin infection. Nat Commun 17, 1980 (2026). https://doi.org/10.1038/s41467-026-68788-4
Trefwoorden: Staphylococcus aureus, huidabces, collageen, neutrofielen, complementsysteem