Clear Sky Science · nl
NatA vormt multifactorcomplexen bij de uitgang van de ribosomale polypeptidetunnel
Hoe cellen nieuwe eiwitten bijsturen terwijl ze ontstaan
Elke seconde produceren je cellen duizenden nieuwe eiwitten op kleine machines die ribosomen heten. Zodra elke eiwitketen verschijnt, moet deze correct worden bijgesneden, gemarkeerd en gevouwen, anders kan het verkeerd functioneren en bijdragen aan ziekte. Deze studie onderzoekt een van de belangrijkste markeersystemen, een modificatie genaamd N-terminale acetylatie, en laat zien hoe een centraal enzymcomplex, NatA, samenwerkt met meerdere partners precies daar waar nieuwe eiwitten de ribosoomuitgang passeren. Inzicht in deze choreografie verklaart hoe cellen hun eiwitfabrieken soepel laten draaien.
De kleine chemische markering die ertoe doet
De meeste eiwitten beginnen hun leven met hetzelfde eerste bouwblok, het aminozuur methionine. Vaak wordt deze initiële methionine verwijderd en vervangen door een kleine chemische markering, een acetylgroep. Deze groep, toegevoegd aan de uiterste tip van het eiwit (de N-terminus), kan beïnvloeden hoe lang het eiwit overleeft, waar het in de cel terechtkomt en hoe het functioneert. Twee hoofdtypen enzymen bevinden zich bij de uitgang van de ribosoomtunnel om deze eerste make-over te regelen: methionine-aminopeptidases (MAPs), die de start-methionine afknippen, en N-terminale acetyltransferases (NATs), die de acetylgroep toevoegen. Onder de NATs is NatA de werkpaard in menselijke cellen en kan mogelijk bijna 40% van alle eiwitten modificeren. Omdat veel eiwitten gelijktijdig worden gemaakt, moet de cel deze enzymen organiseren zodat het trimmen en markeren snel en in de juiste volgorde kan plaatsvinden.
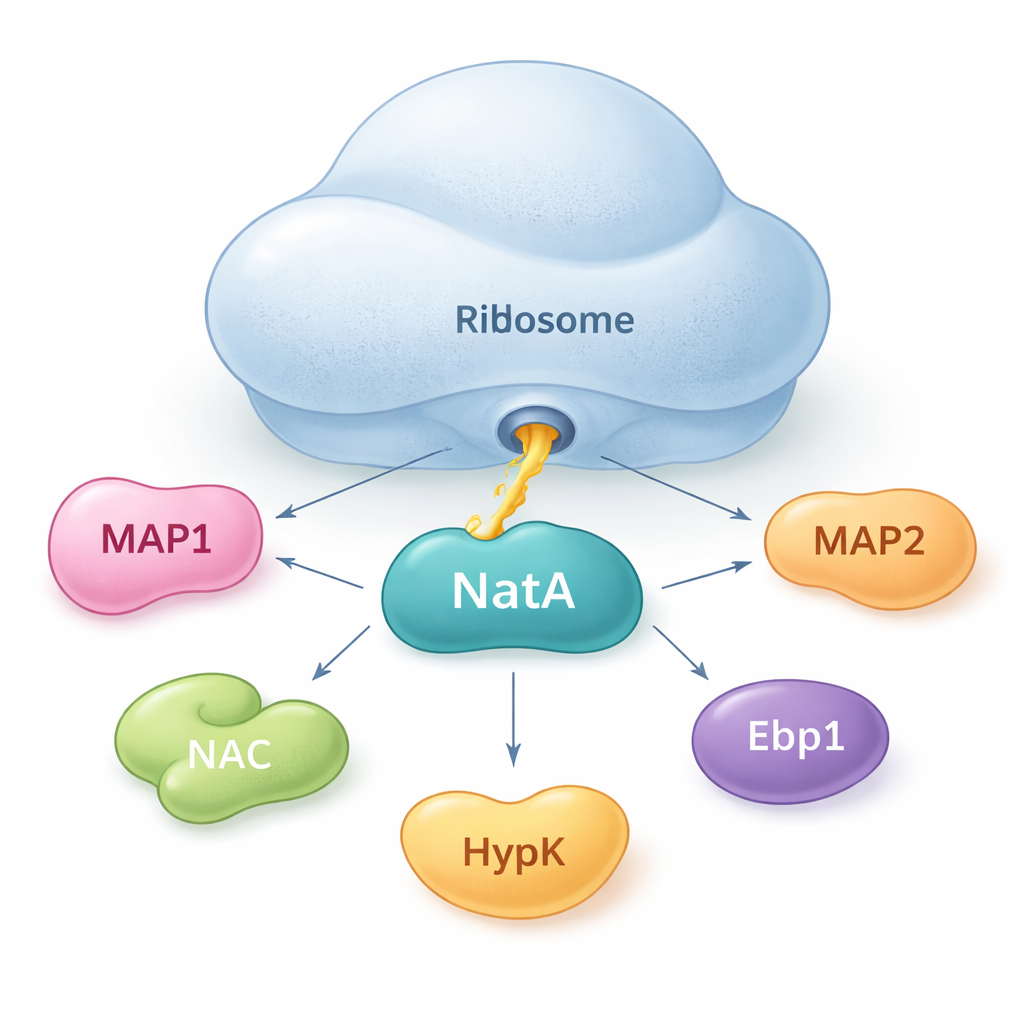
NatA als ontmoetingspunt voor eiwithelpers
De auteurs tonen aan dat NatA niet alleen werkt. In plaats daarvan functioneert het als een knooppunt dat meerdere hulpproteïnen samenbrengt, zowel op als los van het ribosoom. Met gevoelige bindingsmetingen in oplossing vonden zij dat NatA strakke complexen kan vormen met MAP1, het nascent polypeptide–associated complex (NAC), het regulatorische eiwit HypK en een ander enzym, Naa50, zelfs zonder het ribosoom aanwezig. NAC kan NatA met MAP1 verbinden, waardoor zowel het knip- als het markeerstapje in één samenstelling gekoppeld kunnen plaatsvinden. HypK, dat normaal gesproken NatA’s activiteit dempt, kan echter voorkomen dat NAC bindt. Dit suggereert dat cellen NatA kunnen schakelen tussen een meer actieve, NAC-gekoppelde toestand en een geremde, HypK-gebonden toestand, afhankelijk van hun behoeften.
Een tweede bevestigingsplek direct bij de tunneluitgang
Met cryo-elektronenmicroscopie, een techniek die grote moleculen tot bijna atomair detail afbeeldt, ontdekten de onderzoekers dat NatA aan het ribosoom in twee verschillende posities kan binden. Een site, eerder bekend, ligt iets verwijderd van de tunneluitgang. De nieuw ontdekte “proximale” plek positioneert NatA’s katalytische kern zeer dicht bij waar de groeiende eiwitketen naar buiten komt, waardoor de afstand die de keten moet afleggen om gemodificeerd te worden korter wordt. Intrigerend genoeg kunnen beide posities tegelijk bezet zijn, wat betekent dat twee NatA-complexen hetzelfde ribosoom kunnen bezetten. De meer afgelegen kopie fungeert als een scaffold en anker, terwijl de proximale kopie optimaal gepositioneerd is om nieuwe eiwitten te markeren. De twee NatA-moleculen raken elkaar ook aan, wat aangeeft dat NatA zijn eigen duplicaten kan coördineren in multi-enzymteams.
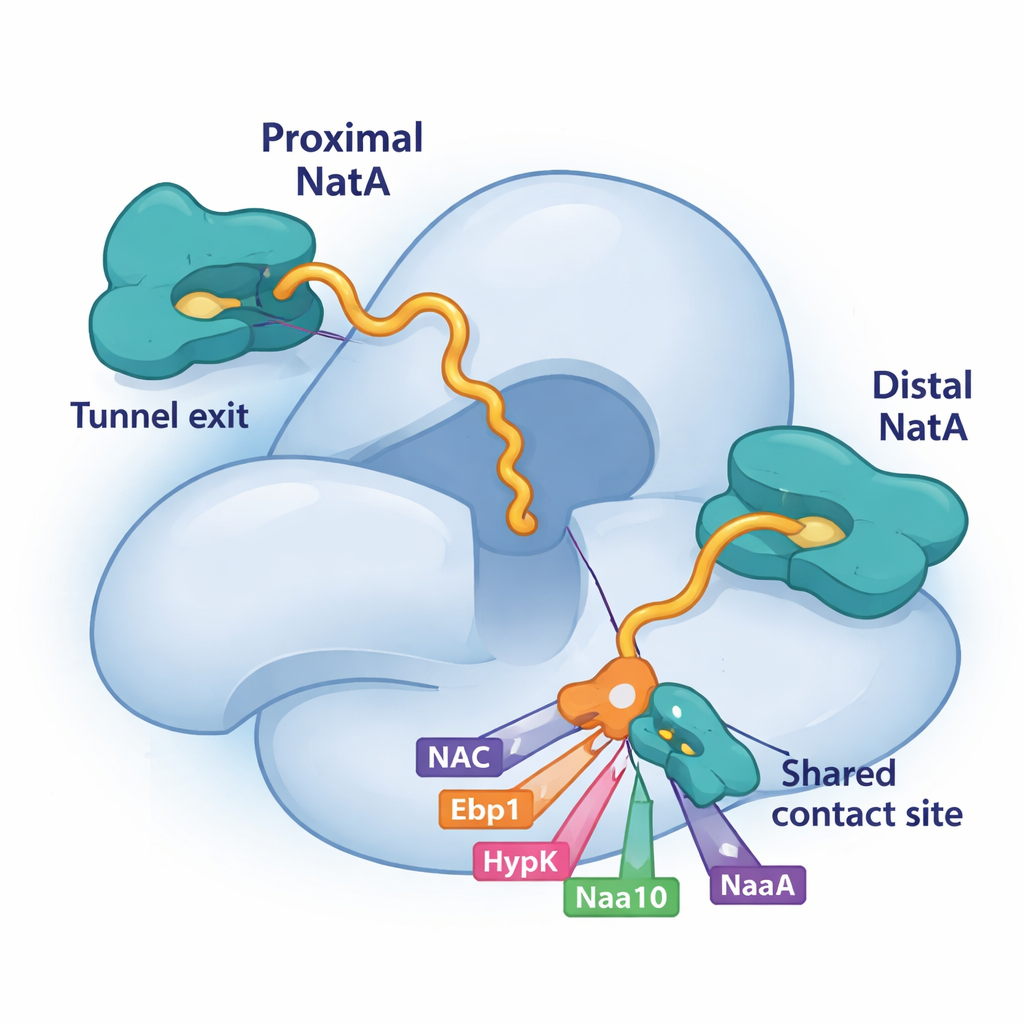
Competitie om een gedeelde aanmeerplaats op NatA
Een cruciaal onderdeel van deze puzzel is een kleine groef op de grote NatA-subunit, Naa15. De studie toont aan dat vier verschillende ribosoomgeassocieerde factoren—NAC, HypK, Ebp1 en zelfs een staartsegment van NatA’s eigen katalytische subunit, Naa10—korte helices gebruiken om zich aan precies hetzelfde plekje op Naa15 vast te hechten. Omdat ze allemaal vertrouwen op deze gedeelde aanmeerplaats, moeten ze concurreren om toegang. Wanneer HypK de site bezet, dempt het niet alleen NatA’s activiteit maar voorkomt het ook dat NatA met NAC paart of NatA–NatA-dimeren vormt. Wanneer NAC, het pseudo-enzym Ebp1 of proximale Naa10 daarentegen binden, kunnen zij NatA’s positie of verbindingen aan het ribosoom herevalueren. Deze competitieve binding geeft de cel een flexibele manier om te kiezen welke partners op elk moment rond NatA assembleren.
Een pseudo-enzym als verkeersregelaar
Het eiwit Ebp1 is bijzonder intrigerend. Het lijkt op een van de methionine-verwijderende enzymen maar mist katalytische activiteit; het is een “pseudo-enzym.” Eerder werk toonde aan dat Ebp1 op het ribosoom nabij de tunneluitgang kan zitten en een lange RNA-sequentie kan klemmen. In deze studie vinden de auteurs dat wanneer NatA zich bij het ribosoom voegt, Ebp1 van positie verschuift, het RNA loslaat en in plaats daarvan zijn eigen helix gebruikt om dezelfde bindingsplaats op Naa15 te bezetten die NAC en HypK gebruiken. Deze herordening suggereert dat Ebp1 kan fungeren als plaatsvervanger of organisator: het kan de lokale RNA-omgeving vormen en vervolgens de controle overdragen aan actieve enzymen zoals MAPs en NatA, zonder zelf direct chemie uit te voeren.
Waarom deze moleculaire drukte ertoe doet
Voor een niet-specialist kunnen de details van helices en bindingsplaatsen abstract klinken, maar de kernboodschap is eenvoudig: cellen voeren een hoogst georkestreerd, meerstaps kwaliteitscontrolesysteem uit precies waar eiwitten ontstaan. NatA zit in het midden van dit systeem en kan verschillende partners rekruteren of loslaten, afhankelijk van welke factoren toegang krijgen tot een cruciale dockingplek en welke ribosomale site NatA bezet. Dit flexibele netwerk helpt ervoor te zorgen dat trimmen en acetylatie plaatsvinden met de juiste timing en volgorde voor duizenden verschillende eiwitten. Aangezien fouten in N-terminale verwerking worden gelinkt aan ontwikkelingsstoornissen, neurodegeneratie en kanker, geeft het in kaart brengen van hoe NatA en zijn partners assembleren onderzoekers een duidelijker stappenplan voor hoe vroege eiwitverwerking wordt gecontroleerd—en hoe die aangetast kan worden wanneer het misgaat.
Bronvermelding: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Trefwoorden: eiwitkwaliteitstoezicht, N-terminale acetylatie, ribosomaire tunneluitgang, NatA-complex, co-translationele modificatie