Clear Sky Science · nl
Plantaire fucosyltransferase FUT11 vervormt de suikeracceptor om via een tijdelijk oxocarbenium-intermediair te katalyseren
Hoe planten de suikers op hun eiwitten fijnregelen
Eiwitten in onze cellen, en in planten, zijn vaak voorzien van complexe suikerketens die functioneren als streepjescodes en bepalen hoe die eiwitten vouwen, hoe lang ze meegaan en met welke partners ze kunnen binden. Deze studie richt zich op een plantaire enzym genaamd FUT11 dat een kleine suiker, fucose, aan deze ketens toevoegt. Door te onthullen hoe FUT11 op atomair niveau werkt, laten de auteurs een verrassend trucje zien: het enzym buigt kort de suikerpartner uit vorm om een moeilijke chemische stap mogelijk te maken. Het begrijpen van dit proces is niet alleen van fundamenteel biologisch belang, maar ook van belang voor het ontwerpen van veiligere in planten geproduceerde geneesmiddelen die vermijden dat ze ongewenste immuunreacties bij mensen veroorzaken.
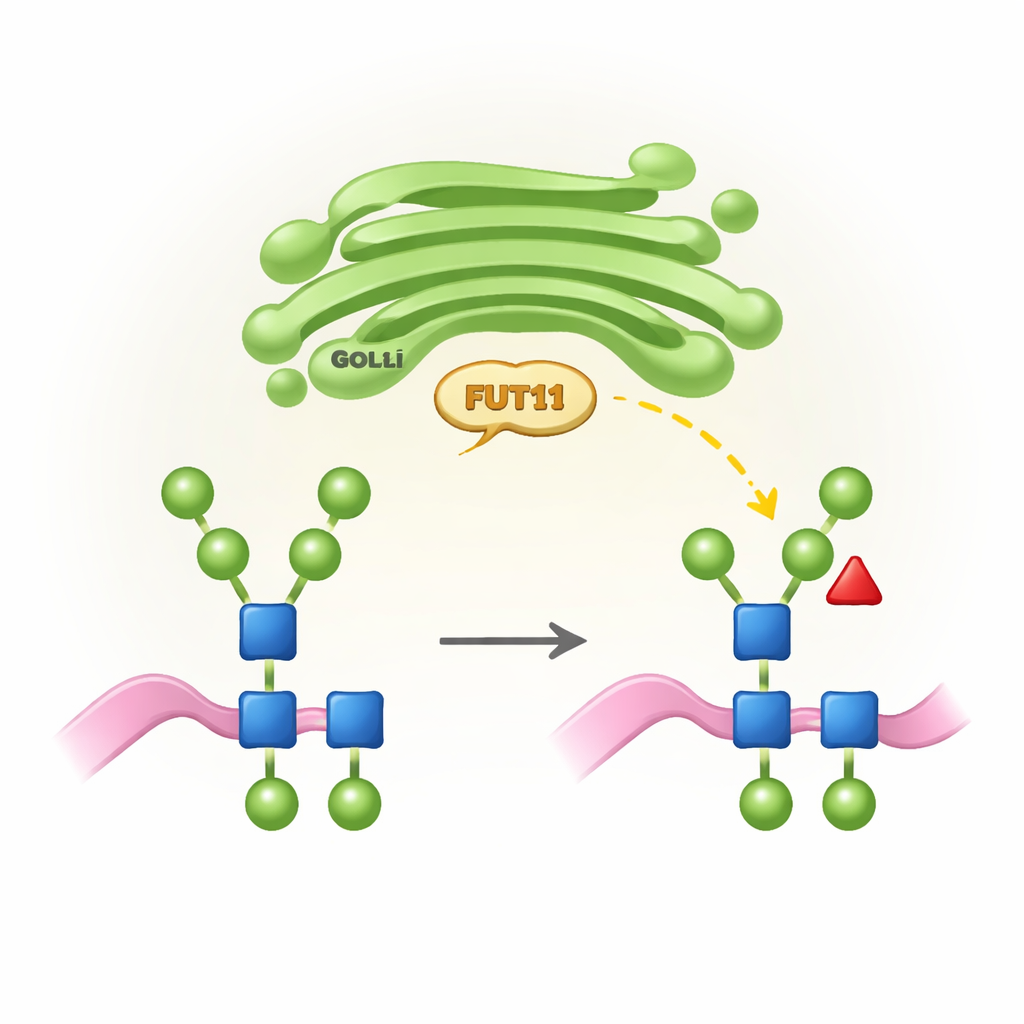
Plantaire, specifieke suikertags en waarom ze ertoe doen
Alle hogere organismen gebruiken een proces dat N-glycosylering heet om suikerketens (N-glycanen) aan bepaalde plaatsen op eiwitten te koppelen. Bij dieren worden deze ketens in het Golgi-apparaat van de cel omgebouwd tot uitgewerkte structuren die vaak eindigen met sialzuren en een kernfucose op één specifieke positie bevatten. Planten volgen echter een andere “ontwerpregel”: hun N-glycanen missen doorgaans siaalzuur maar dragen een kernfucose op een andere positie (genoemd b1,3) plus een extra xylose-suiker. Deze plantaire kenmerken zijn essentieel voor normale groei en vruchtbaarheid, maar kunnen door het menselijk immuunsysteem als vreemd worden herkend. FUT11 is één van de sleutelenzymen in planten die deze kernfucose plaatsen, en zijn activiteit bepaalt zowel de plantontwikkeling als hoe in planten gemaakte therapeutische eiwitten in ons lichaam worden gezien.
In kaart brengen waar FUT11 kan werken op complexe suikervertakkingen
Om te begrijpen wat FUT11 herkent, testten de onderzoekers het enzym op een microarray met 144 verschillende N-glycanstructuren. Ze vonden dat FUT11 behoorlijk selectief is voor één tak van de suikertak — de zogenaamde b1,3-arm — die een specifiek bouwblok moet dragen (een terminale N-acetylglucosamine, of GlcNAc) zodat de reactie kan verlopen. Tegelijkertijd is FUT11 tolerant ten opzichte van andere versieringen: het werkt nog steeds wanneer de centrale mannose een plantaire xylose draagt, en zelfs wanneer een andere fucose al op de dierlijke positie van de kern is geplaatst. De tegenoverliggende tak (b1,6) ligt grotendeels bloot aan het oplosmiddel en maakt slechts zwakke contacten met het enzym, wat verklaart waarom FUT11 een grote verscheidenheid aan modificaties daar kan verdragen. Deze bindingsvoorkeuren helpen verklaren waarom planten een karakteristieke set N-glycanstructuren produceren en laten zien hoe FUT11 gebruikt of vermeden kan worden bij het engineereren van plantencellen voor biotechnologie.
Een uniek structureel ontwerp om suikers vast te grijpen en te positioneren
Met röntgenkristallografie loste het team de driedimensionale structuur van FUT11 op gebonden aan zijn suikerdonor (GDP-fucose) en een N-glycanacceptor. Het enzym heeft een tweelobbige “GT-B”-architectuur: de ene lob ondersteunt de GDP-fucose, terwijl een uitzonderlijk uitgebreide acceptorlob, inclusief een plantaire N-terminale subdomein, zich om het N-glycan heen vouwt. Dit extra subdomein, verbonden met de rest van het enzym door disulfidebruggen, verankert het centrale deel van het glycan en helpt het reactieve GlcNAc-bestanddeel naar de donor te richten. Mutaties van sleutelaminozuren bevestigden hun rollen: het veranderen van een enkele glutamaat (Glu158) elimineerde de activiteit, terwijl het wijzigen van twee nabijgelegen residuen de fucosylatie in geïngineerde humane cellen sterk verzwakte. Deze resultaten koppelen structurele momentopnamen aan echte cellulaire functie en tonen precies welke delen van het eiwit onmisbaar zijn voor binding en katalyse.
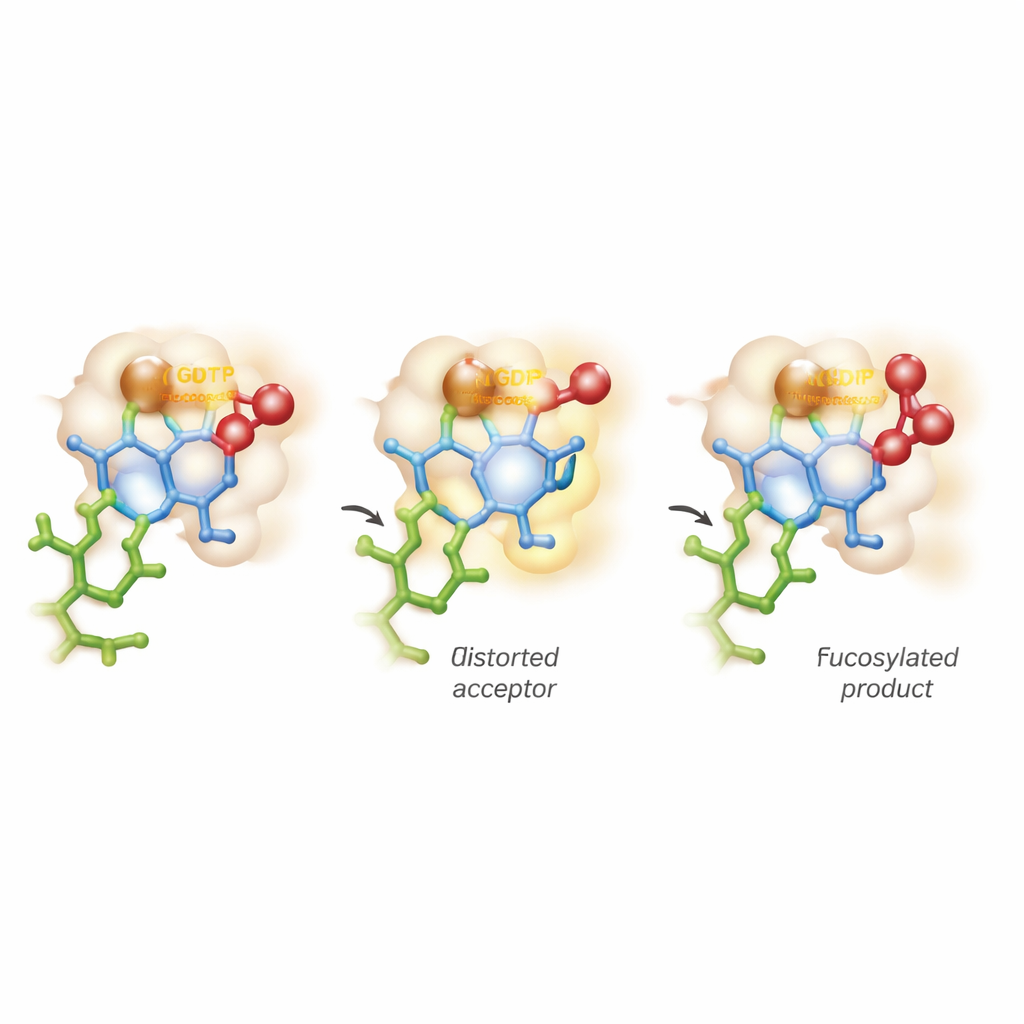
De suiker buigen en balanceren tussen twee reactiepaden
Het meest opvallende inzicht komt uit geavanceerde computersimulaties die kwantummechanica en moleculaire dynamica combineren. Traditionele opvattingen veronderstellen dat de acceptorsuiker zijn stabiele, stoel-achtige vorm behoudt terwijl het enzym alleen de donor activeert. Hier gedraagt FUT11 zich agressiever: interacties aangedreven door Glu158 vervormen tijdelijk de binnenste GlcNAc-ring naar een minder stabiele, geplooide vorm. In deze gespannen houding is de kritische hydroxylgroep perfect uitgelijnd om de fucosedonor aan te vallen. De berekeningen tonen aan dat wanneer de chemische binding met GDP verbreekt, er een kortstondige, positief geladen „oxocarbenium-achtige” toestand op de suiker verschijnt, voordat de nieuwe binding met de acceptor volledig is gevormd. Dit betekent dat de reactie zich niet netjes in de klassieke SN1- of SN2-categorieën laat vangen, maar verloopt langs een continuüm, op een asynchrone, bijna stapgewijze manier.
Verborgen flexibiliteit en evolutionaire echo’s
Door FUT11 te vergelijken met een verwant humaan enzym, FUT9, vonden de auteurs dat het plantaardige enzym ook, zij het zwak, een ander suikermotief (LacNAc) kan modificeren om een structuur bekend als Lewis X te vormen. Deze nevenactiviteit is waarschijnlijk niet biologisch belangrijk in planten, waar Lewis X normaal niet voorkomt, maar benadrukt hoe vergelijkbare eiwitscaffolds in de evolutie kunnen worden hergebruikt om op verschillende suikercontexten te werken. De studie suggereert dat FUT11 en zijn verwanten een modulair raamwerk delen voor het herkennen van N-glycanen, met subtiele aanpassingen die de specificiteit verschuiven tussen plantaardige kernen en dierlijke antennes.
Waarom dit buigtrucje van belang is voor wetenschap en geneeskunde
Samengevat laat het werk zien dat FUT11 meer doet dan twee suikerpartners bij elkaar brengen: het buigt actief de acceptorsuiker in een reactieve houding en kanaliseert de chemie via een vluchtig, geladen intermediair. Voor de niet-specialist betekent dit dat de suiker op het eiwit geen starre aanhechtingsplaats is, maar een flexibel deelnemer die het enzym in de gewenste vorm knedet. Deze nieuwe kijk op “conformationele katalyse” helpt verklaren hoe enzymen zowel snelheid als selectiviteit bereiken en biedt een blauwdruk voor het herontwerpen van glycosyleringsroutes. In praktische termen kan het precies weten hoe FUT11 plantaardige N-glycanen herkent en wijzigt, het ontwerpen van landbouwplanten en plantaardige productiesystemen sturen om immuunreactieve suikerpatronen in humane therapieën te minimaliseren, of om designer-glycoproteïnen met aangepaste biologische eigenschappen te creëren.
Bronvermelding: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Trefwoorden: plantaire glycosylering, fucosyltransferase FUT11, N-glycanen, enzymmechanisme, glyco-engineering