Clear Sky Science · nl
Ruggenmergstimulatie als therapie tegen loopproblemen bij de ziekte van Parkinson: een dubbelblind, gerandomiseerd haalbaarheidsonderzoek met een open verlenging
Wanneer lopen een dagelijkse strijd wordt
Veel mensen met de ziekte van Parkinson ervaren dat lopen niet langer een automatische handeling is, maar een voortdurende uitdaging wordt. Hun voeten kunnen zich plots “aan de vloer geplakt” voelen, waardoor alledaagse taken risicovol en uitputtend zijn. Deze studie stelde een eenvoudige maar belangrijke vraag: kan een klein geïmplanteerd apparaat dat zachte elektrische pulsen naar het ruggenmerg stuurt deze patiënten veilig helpen beter te lopen, en is het de moeite waard om dit in grotere onderzoeken te testen?
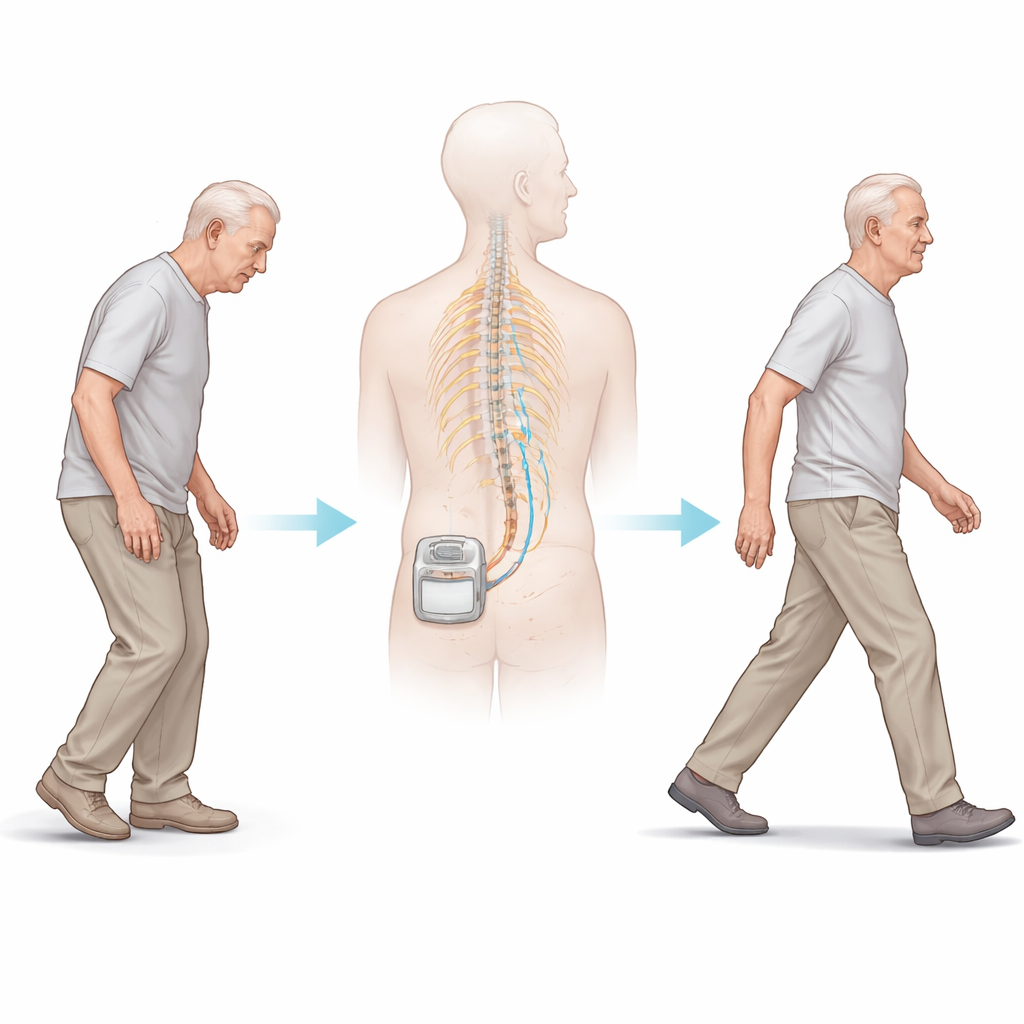
Een nieuwe toepassing voor een pijntherapie
Ruggenmergstimulatie wordt al gebruikt om ernstige, langdurige pijn te verlichten. Chirurgen plaatsen een dunne elektrode langs de wervelkolom en verbinden deze met een batterijgevoede pulsgenerator onder de huid. Het apparaat geeft kleine elektrische pulsen af naar zenuwbanen. In het afgelopen decennium meldden artsen dat sommige mensen met Parkinson die deze behandeling voor rugpijn kregen, ook schijnbaar gemakkelijker gingen lopen. Die observatie inspireerde de STEP-PD proef, die een specifiek “burst”-stimuleringspatroon testte dat geen tintelingen veroorzaakt, waardoor een eerlijke vergelijking mogelijk werd tussen echte stimulatie en een schijnconditie (apparaat uit).
Opzet van de proef
De onderzoekers rekruteerden mensen met de ziekte van Parkinson die last hadden van bevriezingen tijdens het lopen ondanks goed afgestelde medicatie. Na een operatie om de ruggenmergstimulator in de middenrug te plaatsen, gingen twaalf deelnemers een zes maanden durende dubbelblinde fase in: de helft kreeg toevallig geselecteerd burst-stimulatie, de andere helft had het apparaat uitgeschakeld. Noch de patiënten, noch de onderzochte artsen wisten wie in welke groep zat. Alle deelnemers gingen daarna door met nog eens zes maanden in een open fase waarin iedereen actieve stimulatie kreeg. Gedurende het onderzoek maten de onderzoekers balans en lopen met standaard bewegingsscores, eenvoudige looptesten, thuissensoren en vragenlijsten over mobiliteit en kwaliteit van leven. Hersenscans met twee typen PET‑beeldvorming volgden veranderingen in hersenactiviteit en in een chemisch signalsysteem dat te maken heeft met aandacht en beweging.
Veiligheid eerst, signalen daarna
De proef toonde aan dat dit type ruggenmergstimulatie grotendeels veilig en acceptabel was. De meeste problemen hielden verband met de operatie zelf, zoals tijdelijke pijn, zwelling of de noodzaak een elektrode te verplaatsen, en deze kwesties werden zonder blijvende schade behandeld. Belangrijk is dat de hoofdklinische uitkomst—een totaalscore voor balans- en loopproblemen—niet significant verbeterde na zes maanden burst-stimulatie vergeleken met de schijngroep. Toch vonden de onderzoekers bij nadere analyse bemoedigende signalen: stijfheid en traagheid in de benen verbeterden tijdens stimulatie, en een gedetailleerde score voor het onderlichaam en lopen nam in de loop van de tijd af, vooral na een volledig jaar behandeling. Bij vergelijking met een vergelijkbare groep uit een grote Parkinson-database neigden patiënten zonder stimulatie eroverheen het jaar slechter te worden, terwijl degenen met stimulatie geneigd waren stabiel te blijven of licht te verbeteren.
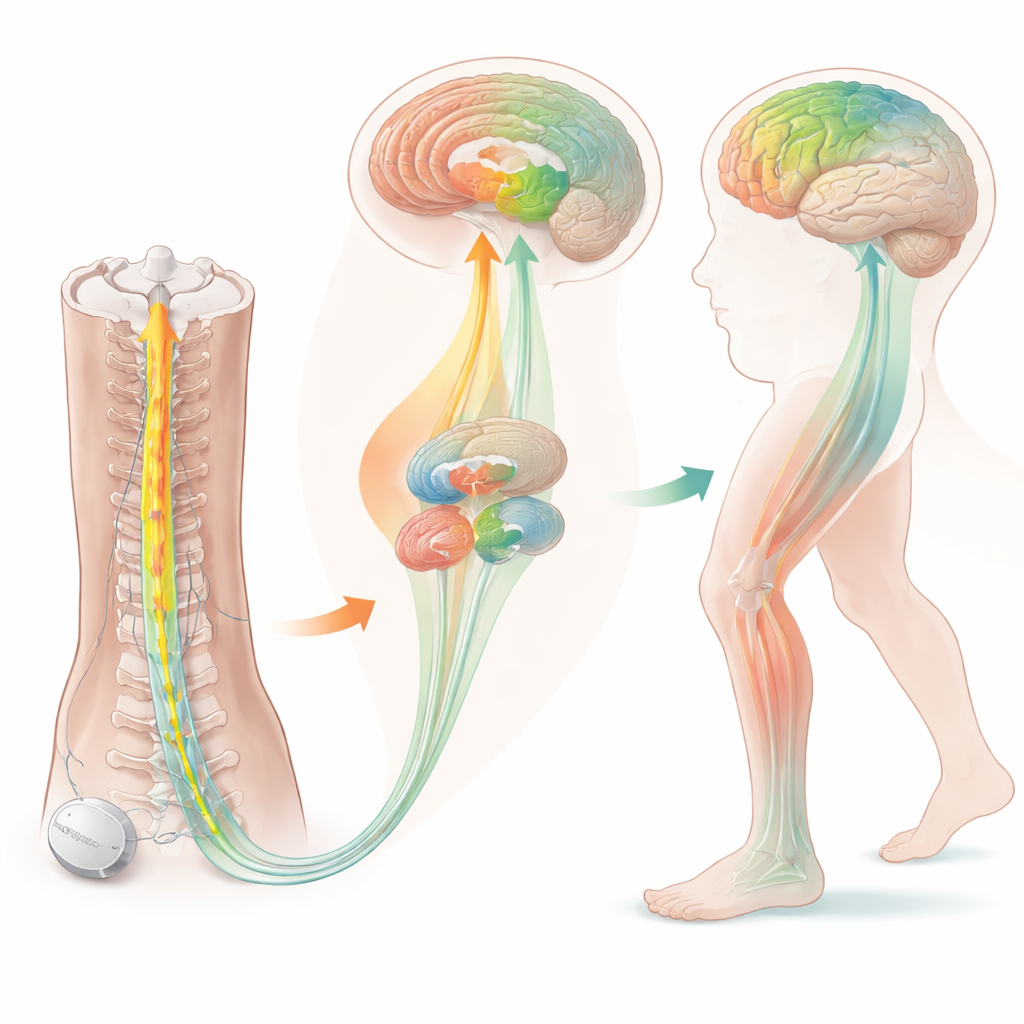
Wat de hersenscans aantoonden
De beeldvorming gaf inzicht in hoe stimulatie mogelijk werkt. Voor de behandeling toonden mensen met bevriezingen tijdens het lopen ongebruikelijke activiteit in hersengebieden die betrokken zijn bij aandacht en bewegingscontrole, waaronder het rechter frontale gebied en een knooppunt dat de anterior insula heet. Na enkele maanden stimulatie daalde het glucoseverbruik in de thalamus—een schakelstation dat helpt bij het coördineren van beweging—en namen signalen van bepaalde cholinerge (acetylcholine-gebruikende) zenuwuiteinden in motorische en aandachtsregio’s ook af. In plaats van schade aan te tonen, weerspiegelen deze verschuivingen waarschijnlijk een normalisatie van overactieve circuits die de hersenen hadden ingezet om te compenseren voor loopproblemen. Deze biologische veranderingen kwamen overeen met de geleidelijke vermindering van beenstijfheid en traagheid die in klinische testen werd waargenomen.
Waarom grotere, slimmer opgezette onderzoeken nodig zijn
Voor leken is de boodschap gemengd maar hoopgevend. Dit kleine, zorgvuldig gecontroleerde onderzoek vond dat burst‑ruggenmergstimulatie geen duidelijke, kortetermijnoplossing bood voor loopproblemen bij de ziekte van Parkinson, en kan daarom nog niet worden aanbevolen als bewezen therapie voor lopen. De behandeling leek echter veilig en leek na verloop van tijd stijfheid en traagheid in de benen te verlichten, met hersenscans die wezen op betekenisvolle verschuivingen in bewegingsnetwerken. De studie leverde ook belangrijke lessen op over proefopzet—wie te includeren, welke scores het meest gevoelig zijn, en hoe lang te behandelen—die grotere, meer doorslaggevende onderzoeken zullen sturen. Met andere woorden: hoewel ruggenmergstimulatie nog geen genezing voor lopen is, kan het deel worden van een toekomstige gereedschapskist om mensen met Parkinson langer en veiliger op de been te houden.
Bronvermelding: Terkelsen, M.H., Hvingelby, V.S., Johnsen, E.L. et al. Spinal cord stimulation therapy for gait impairment in Parkinson’s disease: a double-blinded, randomised feasibility trial with an open extension. Nat Commun 17, 2168 (2026). https://doi.org/10.1038/s41467-026-68782-w
Trefwoorden: Ziekte van Parkinson, loopstoornis, ruggenmergstimulatie, diepe hersennetwerken, neuromodulatie