Clear Sky Science · nl
Proteomische profilering van UV-schadeherstelplekken onthult histonchaperonnes met centrale functies in chromatineherstel
Hoe onze cellen zonlichtschade herstellen
Elke keer dat onze huid sterk zonlicht opvangt, ontstaan er onzichtbare beschadigingen in het DNA van onze cellen. Blijven deze kleine littekens onbehandeld, dan kunnen ze zich opstapelen en bijdragen aan veroudering en kanker. DNA ligt echter niet bloot; het is zorgvuldig gewikkeld rond eiwitten die histonen worden genoemd en zo een structuur vormt die chromatine heet en die helpt de identiteit van elke cel te definiëren. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: wanneer cellen UV-schade in hun DNA herstellen, hoe bouwen ze dan die ingewikkelde chromatine-architectuur weer op zodat de celidentiteit behouden blijft in plaats van verstoord te raken?
De verborgen herstelzone blootleggen
Om dit te beantwoorden moesten de onderzoekers specifiek kijken naar de plekken in het genoom waar herstel actief plaatsvond, in plaats van het hele kerngebied in één keer te onderzoeken. Ze ontwikkelden een aanpak genaamd IPOND-R die korte stukjes pas gevormd DNA tijdens herstel chemisch labelt, en niet tijdens de normale duplicatie van het genoom. Door deze gemarkeerde DNA-“herstelpatches” samen met alle daaraan gebonden eiwitten naar beneden te trekken en die eiwitten vervolgens met hoogresolutie-massaspectrometrie te identificeren, maakten ze een tijdgerelateerde catalogus van wie er verschijnt, en wanneer, tijdens de reactie op UV-schade in menselijke cellen. Dit gaf hen een onbevooroordeeld momentopname van de gespecialiseerde eiwitbuurt die zich direct op herstelplaatsen vormt.
Een drukke menigte op het herstelraamwerk
De IPOND-R-methode bracht honderden eiwitten aan het licht die na UV-blootstelling verrijkt waren op DNA dat hersteld werd. Zoals verwacht waren bekende DNA-herstelfactoren aanwezig die UV-geïnduceerde laesies herkennen en uitknippen. Maar de dataset ging veel verder en ving ook eiwitten op die betrokken zijn bij genregulatie, nucleaire architectuur en, cruciaal, chromatineorganisatie. Veel van deze bezoekers waren histonchaperonnes—gespecialiseerde eiwitten die histonen begeleiden op en van het DNA. Vergelijking van vroege en late tijdpunten liet zien dat de meeste van deze chaperonnes slechts tijdelijk aanwezig zijn, wat wijst op een zorgvuldig gechoreografeerde volgorde van chromatinedemontering en -heropbouw die nauw gekoppeld is aan het DNA-herstelproces.
Nieuwe leveranciers en recyclers van histonen
Onder de eiwitten die verrijkt waren op herstelpatches vielen twee histonchaperonnes op: DNAJC9 en MCM2. Deze factoren waren eerder vooral bekend vanwege hun rollen bij DNA-replicatievorken, waar het genoom wordt gekopieerd, maar waren niet eerder verbonden met UV-schadeherstel. Hier toont het team aan dat DNAJC9 een centrale leverancier is van verse histoneenheden (specifiek H3–H4-paren) tijdens herstel. Met fluorescent gelabelde histonen die nieuwe van oude onderscheiden, vonden ze dat het verminderen van DNAJC9-niveaus sterk de komst van nieuw gemaakte histonvarianten naar UV-beschadigde locaties verminderde, terwijl de kernstappen van DNA-herstel intact bleven. DNAJC9 werkt upstream van de bekende histonafzettere chaperonnes CAF-1 en HIRA en voedt hen met nieuwe histonen zonder hun eigen aanwezigheid op schadekernen te veranderen.
Het balanceren van oude en nieuwe bouwstenen
Het herstellen van chromatine is niet simpelweg een kwestie van nieuwe onderdelen inzetten. De oorspronkelijke histonen dragen ook chemische markeringen die epigenetische informatie bewaren—signalen die een cel vertellen welke genen aan of uit moeten blijven. De studie toont aan dat DNAJC9 ook helpt deze ouderlijke histonen terug te brengen nadat ze tijdelijk waren weggeschoven van beschadigde gebieden. Wanneer DNAJC9 werd uitgeput, keerden oude histonen niet volledig terug en daalde de algehele histondichtheid op herstelplaatsen. De onderzoekers ontdekten vervolgens dat DNAJC9 samenwerkt met MCM2 om dit delicate evenwicht te coördineren: beide zijn nodig voor efficiënte recycling van oude histonen en voor juiste afzetting van nieuwe, zelfs in cellen die hun DNA niet actief repliceren. Dit wijst op een replicatie-onafhankelijke rol voor MCM2 en legt een functioneel partnerschap tussen de twee chaperonnes op herstelplaatsen vast.
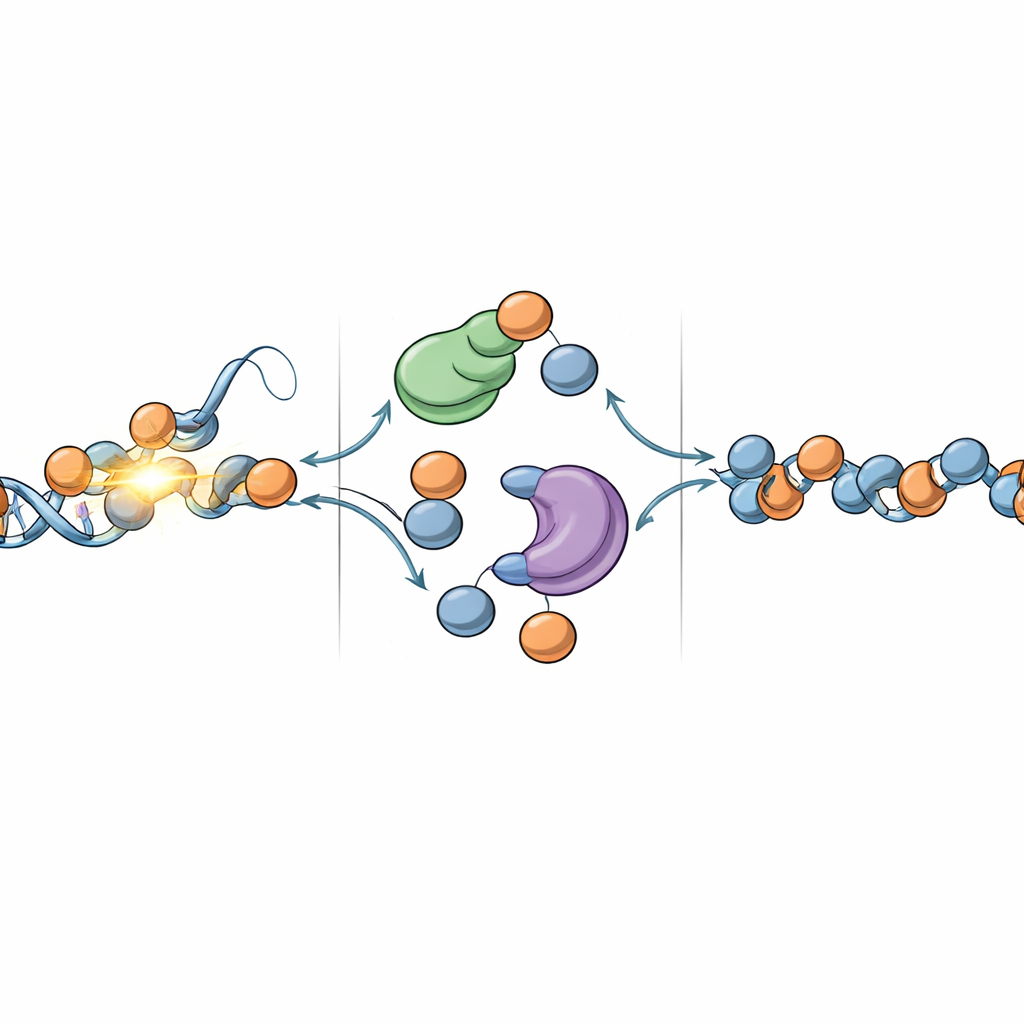
Waarom dit belangrijk is voor celidentiteit en ziekte
Het werk schetst chromatineherstel als een tweezijdige operatie: beschadigd DNA wordt gerepareerd terwijl het omliggende histonlandschap wordt opgebouwd met een mengsel van hergebruikte en vers geleverde componenten. DNAJC9 en MCM2 staan op een kruispunt in dit proces en coördineren de stroom van oude en nieuwe histonen zodat cellen na UV-schade niet alleen de genetische code kunnen herstellen, maar ook de epigenetische patronen die hun identiteit bepalen. Omdat vergelijkbare uitdagingen optreden bij veel typen DNA-schade, biedt dit raamwerk een basis voor het begrijpen hoe cellen een stabiel epigeoom behouden onder stress—een kwestie die centraal staat bij veroudering, kanker en andere ziekten waarbij chromatineregulatie verstoord raakt.
Bronvermelding: Plessier, A., Chansard, A., Petit, E. et al. Proteomic profiling of UV damage repair patches uncovers histone chaperones with central functions in chromatin repair. Nat Commun 17, 2127 (2026). https://doi.org/10.1038/s41467-026-68781-x
Trefwoorden: DNA-schadeherstel, chromatine, histonchaperonnes, UV-straling, epigeoomstabiliteit