Clear Sky Science · nl
Structurele basis en pathologische implicaties van het dimerische OS9-SEL1L-HRD1 ERAD-kerncomplex
Het cellulaire schoonmaakteam onder de microscoop
In elke cel van ons lichaam draait een drukke fabriek die genetische instructies omzet in functionele eiwitten. Net als in elke fabriek gebeuren er fouten. Wanneer eiwitten verkeerd vouwen, kunnen ze het systeem blokkeren en bijdragen aan ziekte. Deze studie zoomt in op een van de belangrijkste kwaliteitscontrolemachines van de cel — het SEL1L‑HRD1-complex — om de gedetailleerde 3D-structuur bloot te leggen en te laten zien hoe kleine genetische veranderingen deze machinerie kunnen beschadigen en mogelijk tot menselijke aandoeningen kunnen leiden.
Een verborgen transportband in de cel
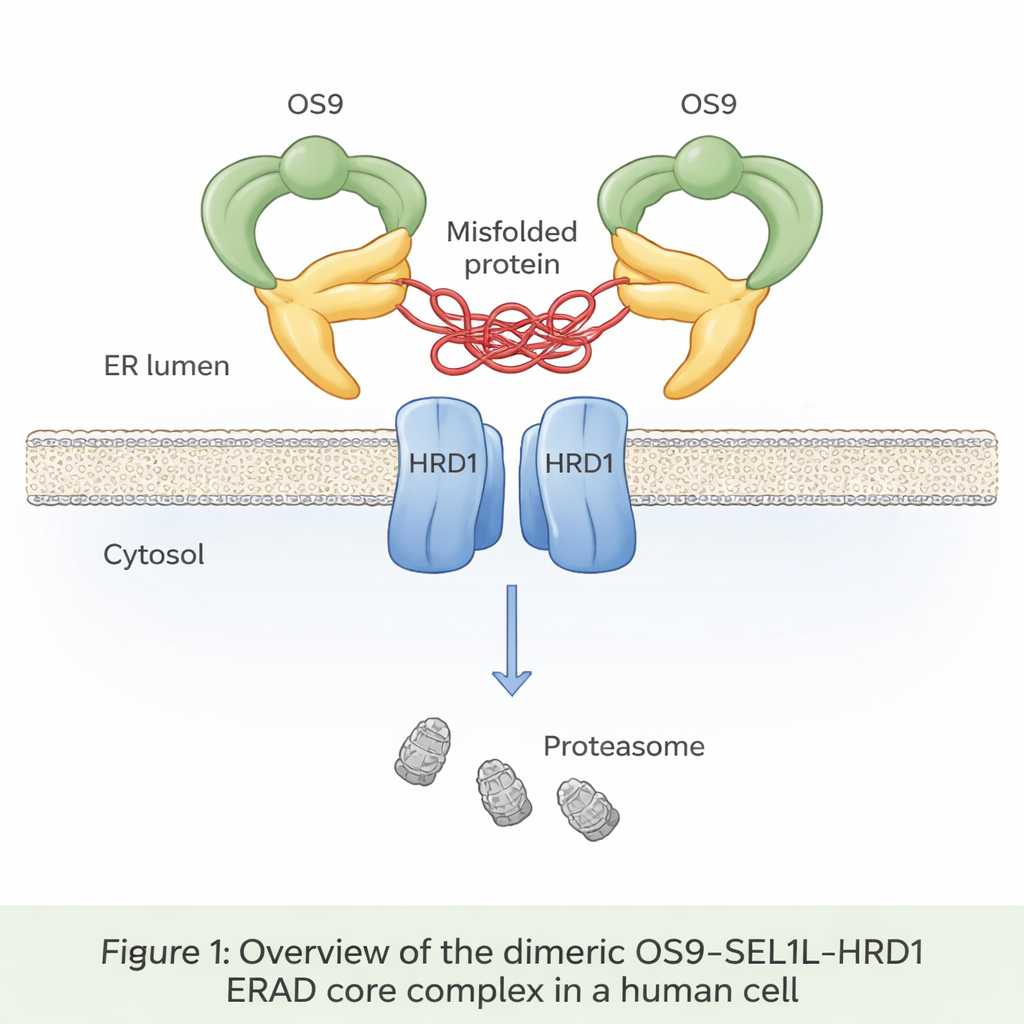
Tot een derde van alle pas gemaakte eiwitten betreedt een compartiment dat het endoplasmatisch reticulum (ER) wordt genoemd, waar ze worden gevouwen en gecontroleerd. Verkeerd gevouwen eiwitten worden normaal herkend, terug uit het ER getrokken en afgebroken in een proces dat bekendstaat als ER‑associated degradation (ERAD). In het hart van een belangrijk ERAD-pad bevindt zich een trio eiwitten: OS9, SEL1L en HRD1. OS9 werkt als sensor voor defecte, suikergemarkeerde eiwitten; SEL1L dient als een raamwerk; en HRD1 markeert gedoemde eiwitten met kleine ubiquitine-vlaggetjes die ze bestempelen voor vernietiging door de afvalverwerkingsunits van de cel, de proteasomen. Tot nu toe had echter nog niemand in atomair detail gezien hoe deze drie onderdelen in menselijke cellen samenkomen.
De vorm van de kernmachine onthuld
De auteurs gebruikten cryo-elektronenmicroscopie, een techniek die in snel bevroren moleculen afbeeldt met bijna-atomaire resolutie, om het uit menselijke cellen gezuiverde OS9‑SEL1L‑HRD1-complex te visualiseren. Ze ontdekten dat het een dimer vormt — in wezen twee identieke kopieën die met elkaar verbonden zijn — in plaats van als losse eenheden te blijven bestaan. Aan de kant van het ER-lumen (de binnenkant van het ER) assembleren twee OS9- en twee SEL1L-moleculen zich tot een krabklauwachtige ring met een centrale opening die lijkt ontworpen om verkeerd gevouwen eiwitten te grijpen. Binnen het membraan zelf koppelen twee HRD1-moleculen om een gedeeld kanaal te vormen. Deze rangschikking positioneert de “klauw” direct boven de HRD1-deur, waardoor een continue route ontstaat voor verkeerd gevouwen eiwitten om van het ER-lumen, door het membraan heen, naar afbraak in het cytosol te bewegen.
Hoe kleine veranderingen een groot systeem breken
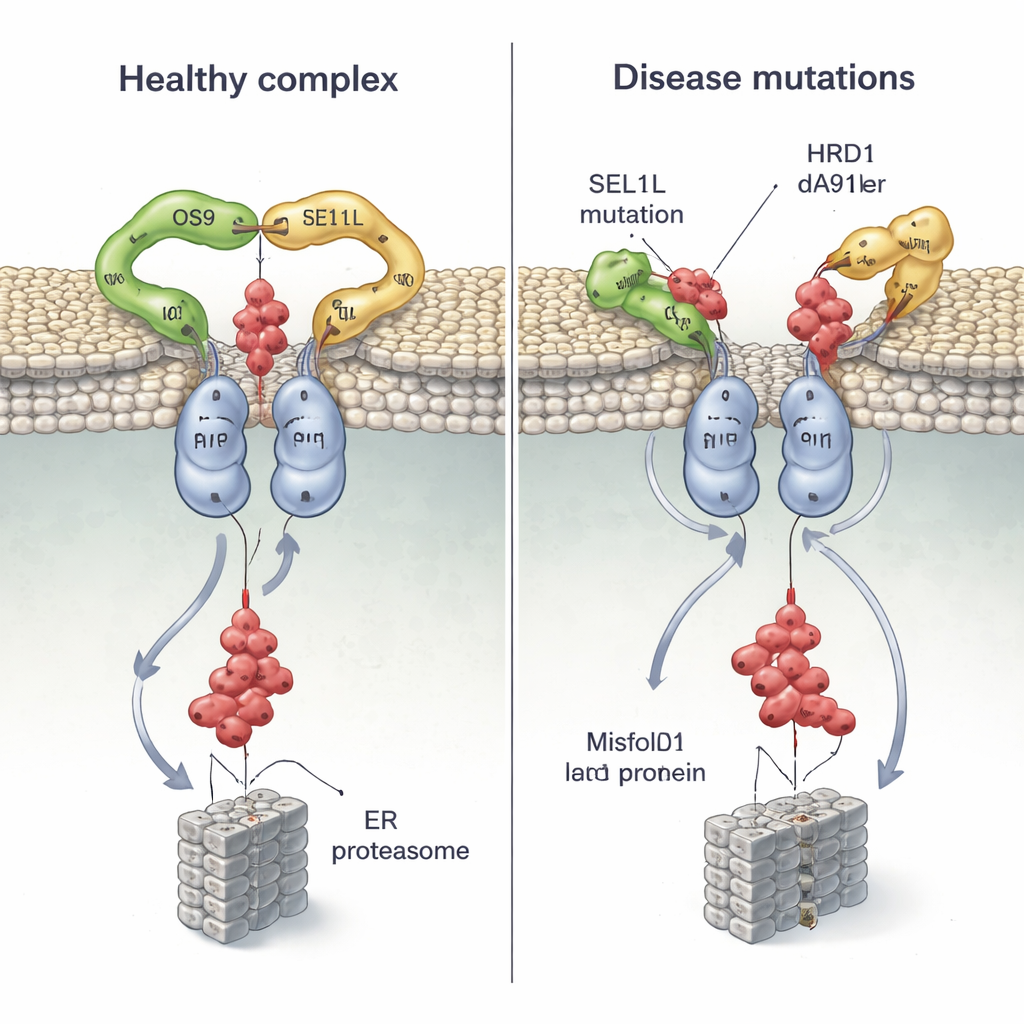
Aangezien mutaties in SEL1L en HRD1 zijn gevonden bij patiënten met ernstige neuroontwikkelings- en andere stoornissen, plaatste het team meerdere aan ziekten gelinkte varianten op hun structuur en testte hoe ze zich in cellen gedragen. Twee SEL1L-mutaties, G585D en S658P, bevinden zich precies op de contactpunten met respectievelijk OS9 en HRD1. In celexperimenten verminderde G585D vrijwel volledig het vermogen van SEL1L om aan OS9 te binden, terwijl S658P zijn greep op HRD1 sterk verzwakte; het combineren van beide mutaties maakte het kerncomplex feitelijk kapot, terwijl andere partners intact bleven. Als gevolg daarvan hadden de cellen moeite om een verkeerd gevouwen hormoonvoorloper te markeren en te verwijderen, waardoor defecte eiwitten langere tijd aanwezig bleven.
Een ziekte-mutatie in het membraankanalen
De structuur toont ook dat transmembranaire segment 3 van HRD1 de sleutelinterface is waar twee HRD1-moleculen elkaar ontmoeten om het kanaal te vormen. De onderzoekers introduceerden cysteïne-"handvatten" op specifieke posities en gebruikten chemische kruisverbindingen om te bevestigen dat deze regio’s in levende cellen nauw contact maken, waarmee werd aangetoond dat HRD1 daadwerkelijk dimeriseert in vivo. Toen ze een enkel, sterk geconserveerd residu (T93) in deze interface verstoorden, viel het dimer uit elkaar en stortte de ERAD-activiteit in, ook al assembleerde het complex nog wel met OS9 en SEL1L. Ze onderzochten vervolgens een recent ontdekte patiëntvariant, HRD1 A91D, gevonden bij een kind met hart‑ en longproblemen. Deze verandering, eveneens in de dimerinterface, halveerde ruwweg de HRD1-dimerisatie en belemmerde sterk de verwijdering van verkeerd gevouwen eiwitten, opnieuw zonder de algemene binding aan partners te verstoren.
Een nieuwe blik op eiwitkwaliteitscontrole en ziekte
Door structurele biologie te combineren met celgebaseerde tests toont dit werk aan dat het OS9‑SEL1L‑HRD1-complex functioneert als een gepaarde, dimerische machine: een klauwachtige vanger gekoppeld aan een gedeeld kanaal dat defecte eiwitten uit het ER voert. Mutaties die de greep van de klauw verslappen of het HRD1‑paar destabiliseren, wijzigen niet slechts de efficiëntie — ze kunnen het systeem effectief blokkeren, waardoor beschadigde eiwitten zich ophopen en bijdragen aan menselijke ziekte. Voor niet‑specialisten is de belangrijkste boodschap dat zelfs enkele letters in ons DNA de vorm van essentiële cellulaire machines subtiel kunnen vervormen, met verstrekkende gevolgen voor hersenontwikkeling, immuniteit en orgaanfunctie.
Bronvermelding: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Trefwoorden: eiwitkwaliteitscontrole, endoplasmatisch reticulum, ERAD, SEL1L-HRD1 complex, eiwitmisvouwing