Clear Sky Science · nl
Profilering van exondeleties in enkele cellen onthult spaisevenementen die genexpressie en celtoestanddynamiek vormgeven
Hoe kleine wijzigingen in RNA celgedrag kunnen veranderen
Onze cellen lezen en spleisen voortdurend RNA-instructies om te beslissen welke eiwitten ze maken en hoe ze reageren op stress, groeien of delen. Deze studie laat zien dat het veranderen van hele kleine stukjes van die RNA-berichten — afzonderlijke segmenten die exons worden genoemd — sterk de genactiviteit kan hervormen en zelfs kan verschuiven hoe cellen door de celcyclus bewegen. Het werk introduceert een krachtig hulpmiddel waarmee wetenschappers veel van deze kleine RNA-keuzes tegelijk, cel voor cel, kunnen scannen, wat nieuwe wegen opent om ziekte te begrijpen en geneesmiddeldoelen te ontdekken.
Geselecteerde woorden uit het genetische script knippen
Genen zijn geschreven als lange reeksen DNA, maar cellen lezen ze niet rechttoe rechtaan. In plaats daarvan knippen en plakken ze kleinere blokken, exons genoemd, samen om een RNA-bericht te bouwen. Door te kiezen welke exons behouden blijven, kunnen cellen meerdere eiwitversies uit één gen maken, vergelijkbaar met het produceren van verschillende montages van dezelfde rauwe filmbeelden. Veel ziekten, waaronder kanker en autisme, worden in verband gebracht met fouten in dit proces, maar voor de meeste exon-keuzes weten we nog niet wat ze precies doen. De auteurs gingen dit veranderen door een grootschalig systeem te bouwen dat specifieke exons uit vele genen kan verwijderen en vervolgens, in duizenden individuele cellen tegelijk, kan volgen hoe die wijzigingen het interne netwerk van de cel beïnvloeden.
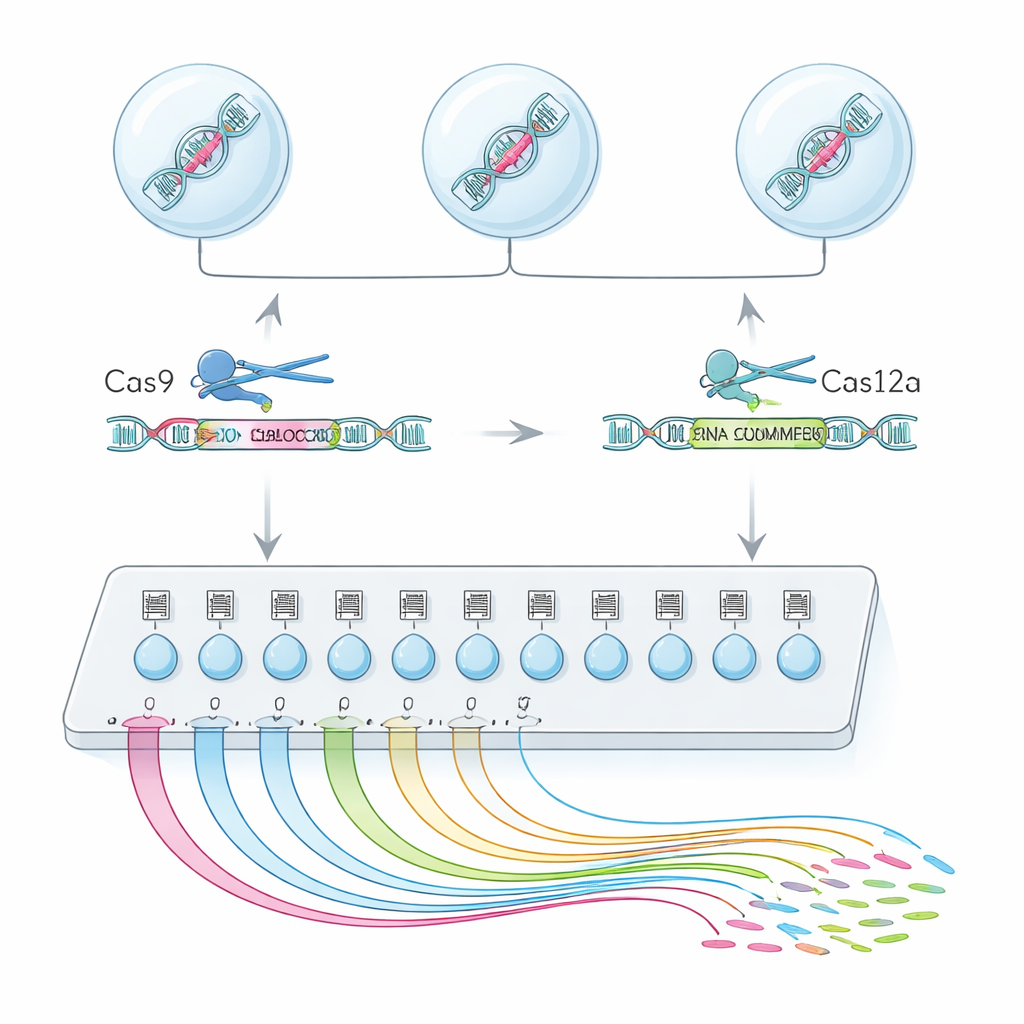
Een single-cell "zoekmachine" voor exonfunctie
Om dit te bereiken combineerde het team twee genoombewerkingsenzymen, Cas9 en Cas12a, tot een hybride platform genaamd CHyMErA. Elk enzym wordt naar DNA geleid door korte RNA-"adressen". Door de twee enzymen te richten om net vóór en net ná een gekozen exon te knippen, kunnen ze dat segment keurig verwijderen terwijl de rest van het gen intact blijft. De nieuwe methode, scCHyMErA-Seq, koppelt deze precieze kniptechniek aan single-cell RNA-sequencing. Het RNA van elke cel wordt vastgelegd in een druppel samen met een barcode en de gids-RNA's die specificeren welk exon verwijderd is. Sequencing onthult vervolgens, voor tienduizenden cellen, zowel de wijziging die elke cel ontving als het gedetailleerde patroon van genen die aan- of uitgingen.
Het gereedschap zo ontwerpen dat beide "messen" zichtbaar zijn
Een belangrijke uitdaging was het betrouwbaar detecteren van de Cas12a-gidsen naast Cas9 in hetzelfde single-cell-experiment. Beginontwerpen slaagden er ofwel niet in de Cas12a-gids-RNA's vast te leggen, of schaadden de bewerkings-efficiëntie. De onderzoekers losten dit op door de Cas12a-handlesequentie zorgvuldig te herontwerpen om reeksen te verwijderen die de transcriptie voortijdig stopzetten, en door een klein stabiliserend RNA-element en een gerichte amplificatiestap toe te voegen. Deze aanpassingen verhoogden het vermogen om beide gidsen in ongeveer 90 procent van de cellen te zien, terwijl sterke exondeletie behouden bleef. Met deze geoptimaliseerde opzet screenden de auteurs 224 alternatieve exons over 161 genen in menselijke cellen en profileerden ze meer dan 200.000 hoogwaardige single cells.
Exons ontdekken die genprogramma's en celcycli regelen
Toen het team de genactiviteit van bewerkte cellen met controles vergeleek, veroorzaakte bijna de helft van de geteste exons substantiële verschuivingen in honderden andere genen. Exons van genen die betrokken zijn bij RNA-verwerking en transcriptie neigden ertoe samen te clusteren, produceerden gelijkaardige expressievingerafdrukken en onthulden gedeelde biologische routes, zoals ribosoomopbouw of RNA-afbraak. In sommige gevallen had het verwijderen van een enkel exon een duidelijk en interpreteerbaar effect: het verwijderen van een exon in de genen TAF5 of LSM11 verstoorde de juiste verwerking van histon-RNA's, wat leidde tot een ongebruikelijke ophoping van gepolyadenyleerde histonboodschappen. De dataset benadrukte ook tientallen exons waarvan het verlies veranderde hoeveel cellen in verschillende fasen van de celcyclus werden gevonden, en verbond specifieke splicing-evenementen rechtstreeks met beslissingen over wanneer een cel pauzeert, zijn DNA kopieert of zich voorbereidt om te delen.
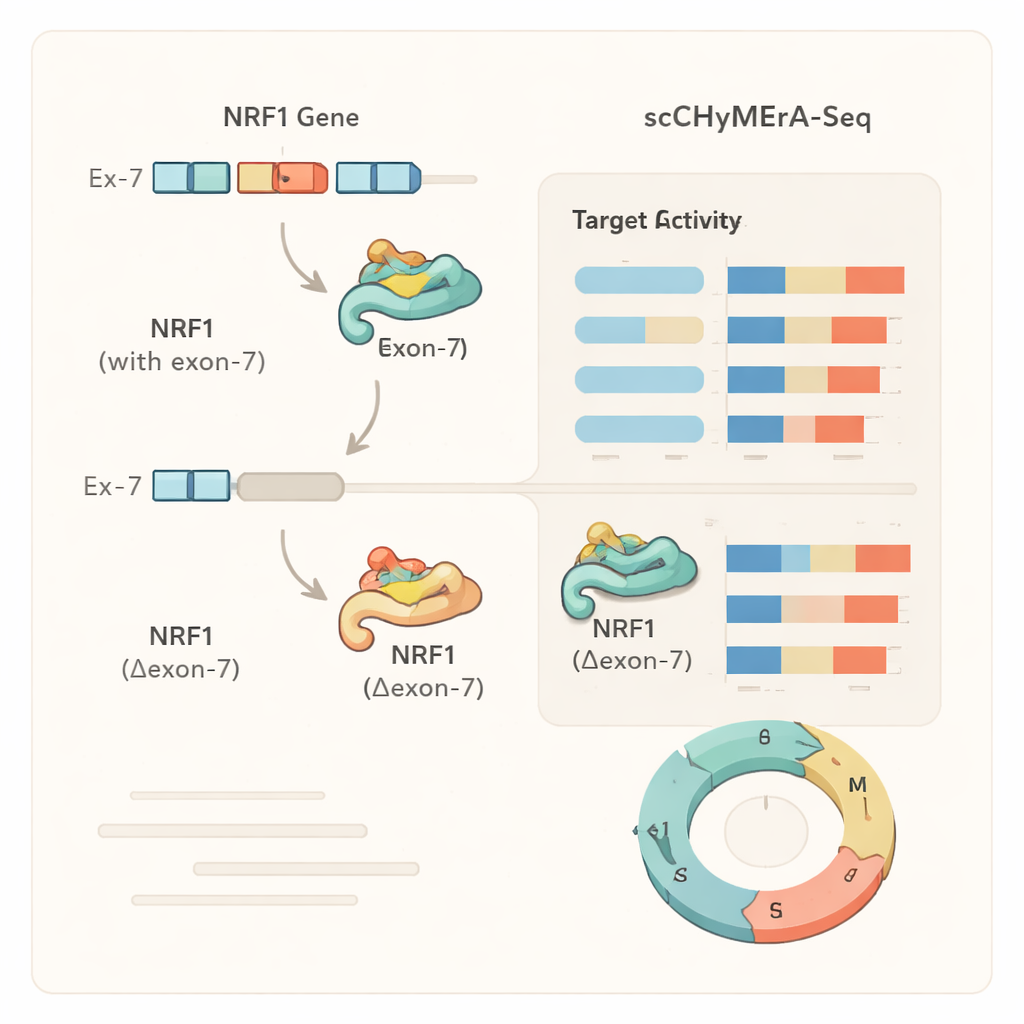
Een casestudy: één exon dat een meesterregelaar afstelt
Een opvallend voorbeeld was exon 7 in het gen NRF1, een transcriptiefactor die veel genen reguleert die betrokken zijn bij cellulaire energieproductie. Dit exon overlapt deels NRF1's DNA-bindingsgebied. Toen exon 7 werd verwijderd, veranderden honderden door NRF1 gereguleerde genen hun activiteit, en gedetailleerde experimenten toonden aan dat het verkorte NRF1-eiwit veel minder goed in staat was zijn doelpromoters in het genoom te binden. De auteurs identificeerden ook een specifieke splicingregulator, SRSF3, die de opname van dit exon bevordert, waarmee een keten van een splicingfactor, via een exonkeuze in NRF1, naar brede veranderingen in cellulaire genprogramma's en metabolisme werd onthuld. Vergelijkbare analyses lieten zien dat bij sommige genen exondeletie een volledige genuitval nabootste, terwijl het bij andere een verfijndere, toestandsafhankelijke verandering produceerde, wat suggereert dat alternatieve exons het eiwitgedrag subtiel kunnen moduleren in plaats van het simpelweg aan of uit te zetten.
Waarom dit belangrijk is voor gezondheid en toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat cellen vertrouwen op het opnemen of overslaan van zeer korte RNA-segmenten om te bepalen hoe genen werken, en dat deze fijne aanpassingen grote eigenschappen kunnen verschuiven, zoals hoe cellen delen of op stress reageren. Het scCHyMErA-Seq-platform werkt als een hoogdoorvoer laboratoriumtest voor deze splicingkeuzes, en wijst aan welke exons echte functionele impact hebben en hoe ze cellulaire toestanden hervormen. Omdat veel vormen van kanker en neurologische aandoeningen betrokken zijn bij verkeerd gespliceerde exons of veranderde transcriptiefactoren, kan deze benadering helpen prioriteren welke splicevarianten in de toekomst met geneesmiddelen of RNA-therapieën moeten worden gericht, en een routekaart bieden om te begrijpen hoe kleine wijzigingen in het genetische script uitwaaieren naar grote veranderingen in celgedrag.
Bronvermelding: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Trefwoorden: alternatief splicing, single-cell RNA-sequencing, CRISPR-screening, genregulatie, celcyclus