Clear Sky Science · nl
Granzyme B-mimetisch nanozym voor nanovesikel-gerichte antikankerapplicaties
De kankerdoders van het lichaam heruitvinden
Ons immuunsysteem beschikt over gespecialiseerde cellen die kanker kunnen opsporen en doden, maar in veel solide tumoren hebben ze moeite om binnen te dringen, raken ze snel uitgeput of vallen ze de verkeerde doelen aan. Deze studie beschrijft een volledig kunstmatig nanoschaalsysteem dat een van de krachtigste wapens van het immuunsysteem nabootst en het direct in tumorcellen aflevert. Het werk is belangrijk omdat het wijst op kankerbehandelingen die zich gedragen als levende immuuncellen, maar zijn gemaakt van stabiele, controleerbare materialen in plaats van kwetsbare menselijke cellen.
Een natuurlijke moordenaar als blauwdruk
Cytotoxische T-cellen, een type witte bloedcel, doden gevaarlijke cellen met een enzym genaamd granzyme B. Zodra ze een doel herkennen, maken ze kleine gaatjes in het membraan en injecteren granzyme B, dat zelfmoordprogramma’s binnen de cel activeert. Deze strategie ligt ten grondslag aan moderne therapieën zoals CAR-T-cellen, die sommige bloedkankers kunnen genezen. In solide tumoren falen CAR-T-cellen vaak echter omdat ze niet alle tumorgebieden bereiken, uitgeput raken of per ongeluk gezond weefsel aantasten. De auteurs vroegen zich af of ze een niet-levend, nanoschaalapparaat konden bouwen dat de belangrijkste functie van granzyme B reproduceert — het inschakelen van de zelfvernietigingsmechanismen van de cel — zonder afhankelijk te zijn van levende T-cellen.
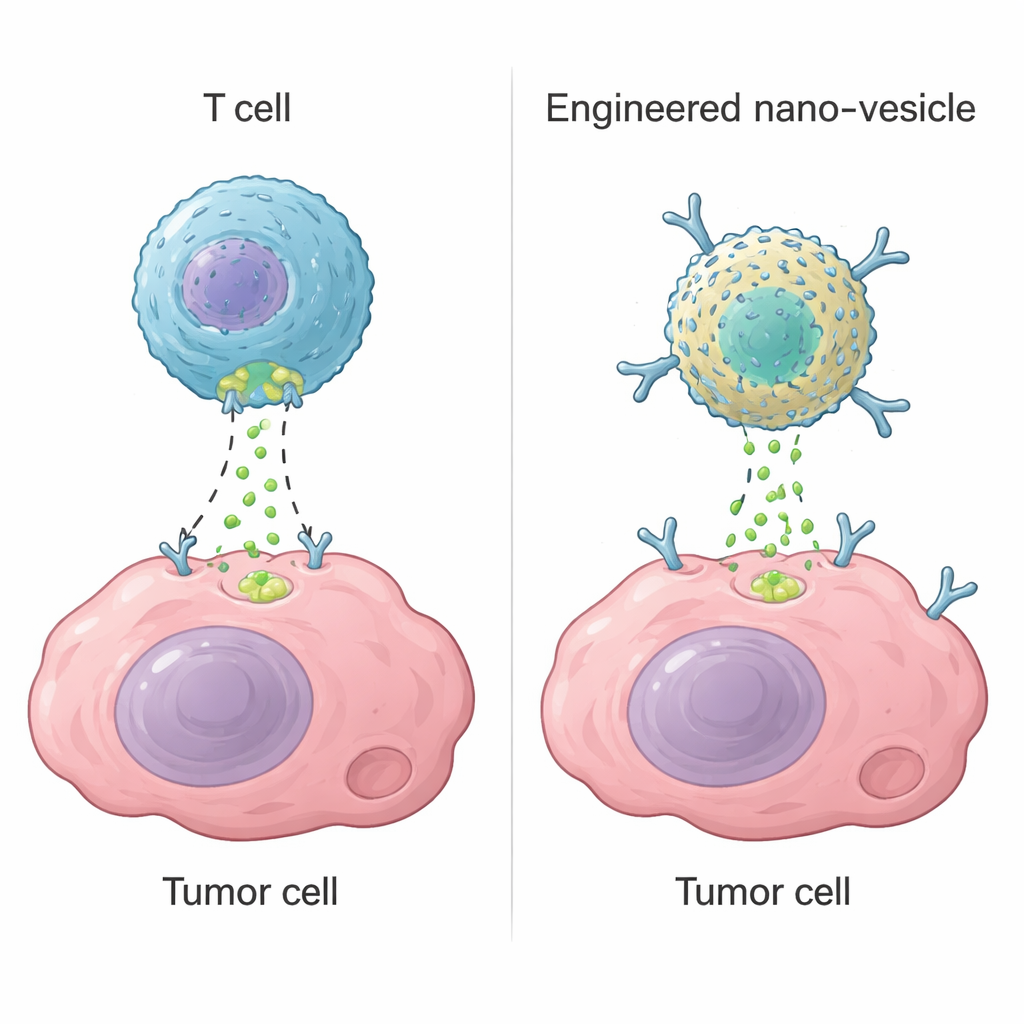
Een piepklein kunstmatig enzym ontwerpen
Het team begon met ferritine, een natuurlijk eiwit dat holle nanokokers vormt en gemakkelijk in grote hoeveelheden te produceren is. Door palladiumionen aan menselijke ferritine te binden, creëerden ze een “nanozym” met enzymachtige eigenschappen. Zorgvuldige structurele studies toonden aan dat twee palladiumatomen zich nestelen in een specifieke pocket aan het eiwitoppervlak, op hun plaats gehouden door zwavel- en stikstofhoudende aminozuren en watermoleculen. Dit binucleaire metaalcentrum fungeert als een kunstmatige knipplaats die dezelfde korte sequentie herkent die granzyme B gebruikt op een cruciaal doelwit bekend als caspase-3. In laboratoriumtests knipte het nanozym efficiënt caspase-3 op de juiste plaats en activeerde het, terwijl het nauw verwante eiwitten negeerde. Het kunstmatige enzym was iets minder efficiënt dan natuurlijk granzyme B maar opvallend stabieler over een breed scala aan temperaturen en zuurgraad.
Het nanozym de tumorcellen insmokkelen
Enzymen zoals granzyme B werken alleen als ze het binnenste van tumorcellen bereiken. Om dit te bereiken verpakte het team hun palladium–ferritine-nanozym in lipide nanovesikels — kleine, zachte belletjes gemaakt van vetachtige moleculen. Ze coatten deze vesikels vervolgens met fragmenten van antilichamen die HER2 herkennen, een eiwit dat vaak overmatig aanwezig is op borst- en blaaskankercellen. Wanneer deze gecamoufleerde vesikels HER2-rijke cellen tegenkomen, binden ze sterk en versmelten met het celmembraan, waardoor de nanozym-lading rechtstreeks het cytoplasma binnen kan glippen in plaats van in cellulair recyclecompartiment te worden gevangen en afgebroken. Microscopen toonden de vesikels die aan het celoppervlak bleven hangen terwijl het nanozym naar binnen diffundeerde, wat de voorwaarden schept voor gecontroleerde zelfvernietiging van binnenuit.
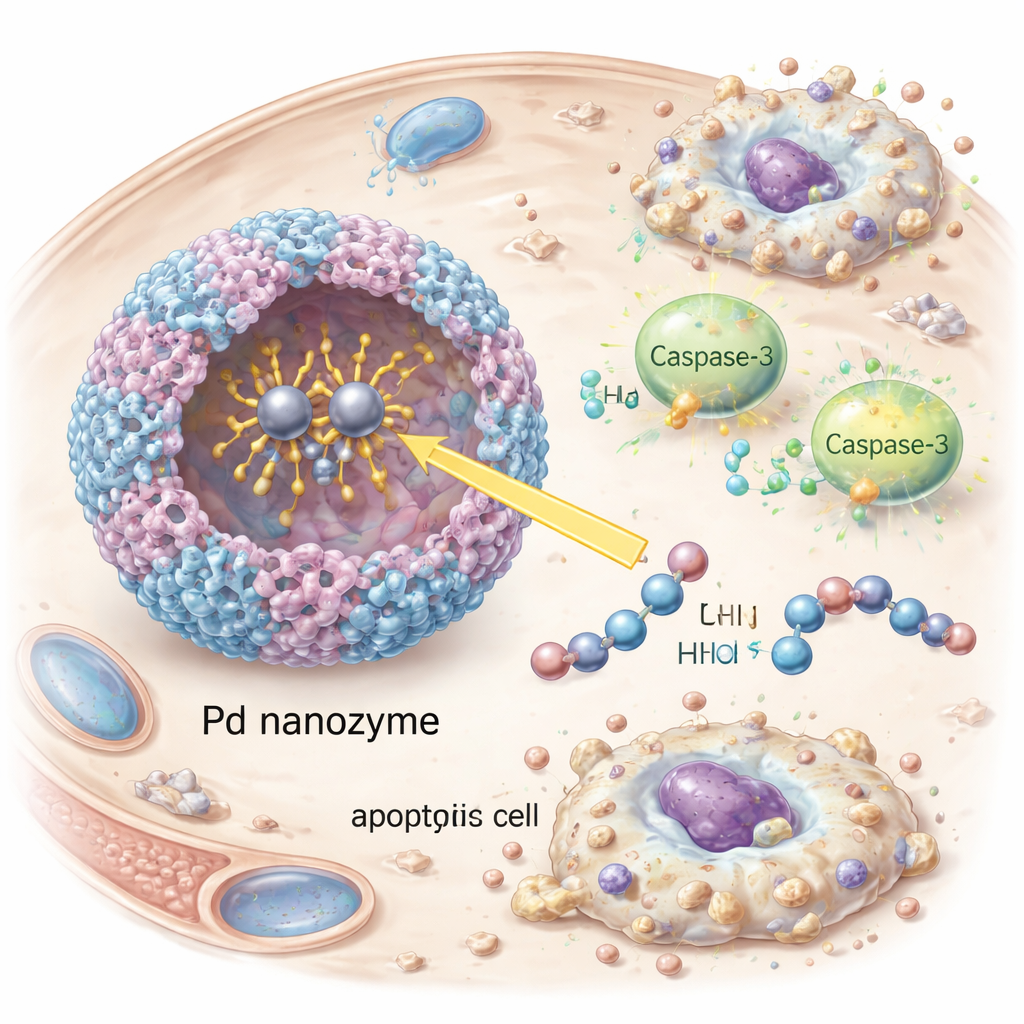
Met precisie zelfmoord van kankercellen triggeren
Eens binnen in kankercellen schakelde het nanozym caspase-3 in, een centrale uitvoerder van geprogrammeerde celdood. De onderzoekers observeerden het verschijnen van geactiveerd caspase-3 en zijn downstream-doel PARP, evenals duidelijke tekenen van apoptose — cellen die krimpen en fragmenteren — in gekweekte HER2-positieve tumorcellen. Het stilleggen van caspase-3 met RNA-interferentie verminderde de celdood dramatisch, wat bevestigt dat het effect afhankelijk was van deze route en niet van niet-specifieke schade. Bij muizen met HER2-positieve tumoren circuleerden de met antilichamen versierde vesikels langer in de bloedbaan, hoopten ze zich sterker op in tumoren en vertraagden ze de tumorgroei effectiever dan vesikels zonder ofwel de targeterende antilichamen of de nanozym-lading. Belangrijk is dat behandelde dieren geen duidelijke gewichtsverlies, bloedafwijkingen of weefselschade in belangrijke organen vertoonden, wat in deze vroege tests wijst op een gunstig veiligheidsprofiel.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat de onderzoekers een klein, niet-levend apparaat hebben gebouwd dat zich gedraagt als een belangrijk onderdeel van de kankerdodende machine van ons immuunsysteem. In plaats van levende T-cellen te ontwerpen, hebben ze een stabiel nano-enzym geconstrueerd dat dezelfde zelfmoordknop in tumorcellen activeert en het ingepakt in een slimme afleveringsomhulling die zich richt op specifieke kankers. Hoewel er veel werk resteert voordat het bij mensen kan worden toegepast, biedt deze benadering een flexibele platform: in principe kan de antilichaamcoating worden verwisseld om op andere tumormarkers te mikken, en het kunstmatige enzym kan verder geoptimaliseerd worden. De studie toont een veelbelovende route naar celvrije immunotherapie, waarbij zorgvuldig ontworpen nanomaterialen, in plaats van levende immuuncellen, worden gebruikt om solide tumoren op te sporen en te vernietigen.
Bronvermelding: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Trefwoorden: kankernanogeneeskunde, immunotherapie, granzyme B, nanozym, HER2-positieve tumoren