Clear Sky Science · nl
Homotypische membraan-gestuurde elektrochemische microfluïdische analyse van extracellulaire blaasjes voor nauwkeurige kankerdiagnostiek
Het pantser van kanker inzetten als diagnostisch instrument
De membranen die kankercellen omringen, zitten vol karakteristieke moleculaire "vlaggen". Deze studie laat zien hoe wetenschappers dat pantser kunnen afpellen, op kleine gouden chipjes kunnen verspreiden en vervolgens gebruiken om kenmerkende deeltjes uit bloed te vissen. Het resultaat is een zeer gevoelige bloedtest die niet alleen kan aantonen of borstkanker aanwezig is, maar ook welk subtype—informatie die cruciaal is voor het kiezen van de juiste behandeling.
Waarom het subtype van borstkanker ertoe doet
Borstkanker is geen eenduidige ziekte. Tumoren worden ingedeeld in subtypes zoals oestrogeenreceptor‑positief (ER+), HER2-positief en triple‑negatief, die elk verschillend reageren op hormoontherapie, gerichte middelen of chemotherapie. Tegenwoordig bepalen artsen het subtype meestal aan de hand van een weefselbiopsie direct uit de tumor. Die ingreep is invasief, kan niet vaak worden herhaald en kan veranderingen missen die optreden naarmate de ziekte voortschrijdt. Een bloedtest die deze subtypetekens in de tijd kan volgen, zou artsen in staat stellen therapie eerder en nauwkeuriger aan te passen.
Piepkleine boodschappers in het bloed
Kankercellen stoten voortdurend nanoschaalblaasjes uit, extracellulaire blaasjes (EVs) genaamd, naar de bloedbaan. EVs dragen eiwitten, vetten en genetisch materiaal die sterk lijken op die van hun oudercellen, waardoor ze aantrekkelijke kandidaten zijn voor "liquid biopsies". Er is echter een uitdaging: EVs van verschillende borstkankersubtypes kunnen er erg hetzelfde uitzien als je je op slechts één of twee eiwitten richt. Bestaande tests richten zich óf op gedeelde markeringen—waardoor subtypen moeilijk te onderscheiden zijn—óf vertrouwen op complexe genetische assays die traag zijn en misleidende resultaten kunnen geven. De auteurs wilden daarom het vollediger moleculair vingerafdrukken op EV-oppervlakken uitlezen op een eenvoudige, robuuste manier.
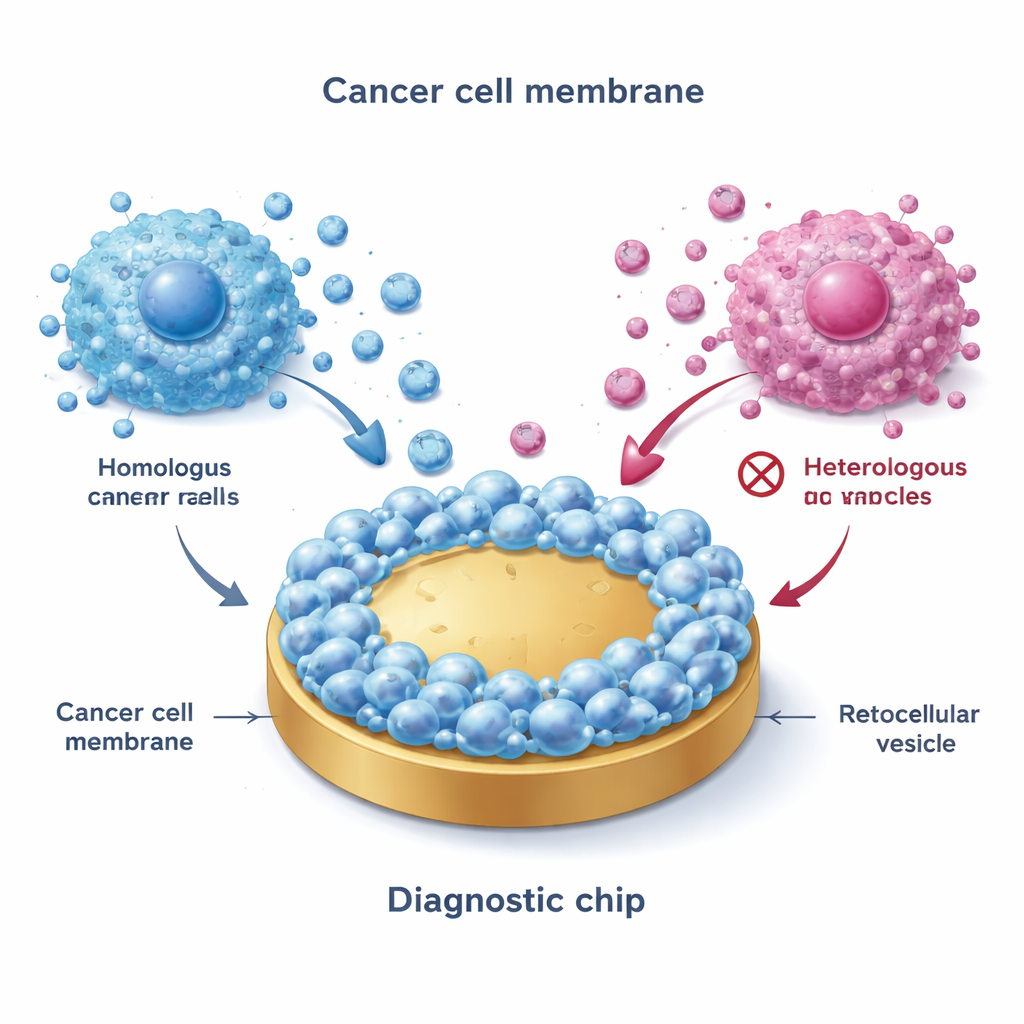
Een biomimetisch visnet bouwen
Het team begon met het winnen van membranen uit gekweekte borstkankercellen die de belangrijke subtypes vertegenwoordigen: ER+ (zoals MCF-7), HER2-positief en triple‑negatief. Met een vries‑dooiproces braken ze de cellen open, isoleerden de buitenmembranen en fuseerden deze vervolgens op vlakke goudoppervlakken. Dit creëerde een "biomimetische interface" die het exterior van de oorspronkelijke kankercellen nauwkeurig nabootst. Opmerkelijk genoeg, wanneer EVs over deze gecoate oppervlakken stroomden, bleven alleen vesikels van overeenkomende of nauw verwante kankersubtypes sterk plakken — een fenomeen dat homotypische binding wordt genoemd. Geavanceerde beeldvorming en elektrische metingen bevestigden dat de membraan‑gecoate oppervlakken ruwere texturen hadden, meer wateraantrekkend waren en veel minder vatbaar voor niet‑specifieke hechting dan bloot goud, waardoor ze goed geschikt zijn voor schone metingen in complexe vloeistoffen zoals bloed.
Vesikelvangen omzetten in een elektrisch signaal
Om binding in een afleesbaar signaal te veranderen, richtten de onderzoekers zich op een veelvoorkomend eiwit genaamd CD47 op het EV-oppervlak. Ze hechtten CD47‑antistoffen aan zilvernanodeeltjes met behulp van een korte DNA‑brug, waarmee ze kleine elektroactieve tags creëerden. Nadat het membraan‑gecoate oppervlak zijn voorkeurs‑EVs had gevangen, klikten deze tags vast aan CD47 op de gebonden vesikels. Bij blootstelling aan een zure oplossing en daaropvolgende elektrochemische meting leverde het zilver een scherpe, gemakkelijk kwantificeerbare stroom op. De sterkte van dit signaal nam lineair toe over een breed bereik van EV‑concentraties, tot slechts enkele honderden vesikels per milliliter—veel gevoeliger dan gangbare methoden zoals ELISA‑kits of nanoparticle tracking. Elk type kankermembraan genereerde een sterk signaal alleen met zijn bijpassende EVs, zelfs in aanwezigheid van vesikels van andere subtypes, bloedplaatjes of niet‑verwante cellen.
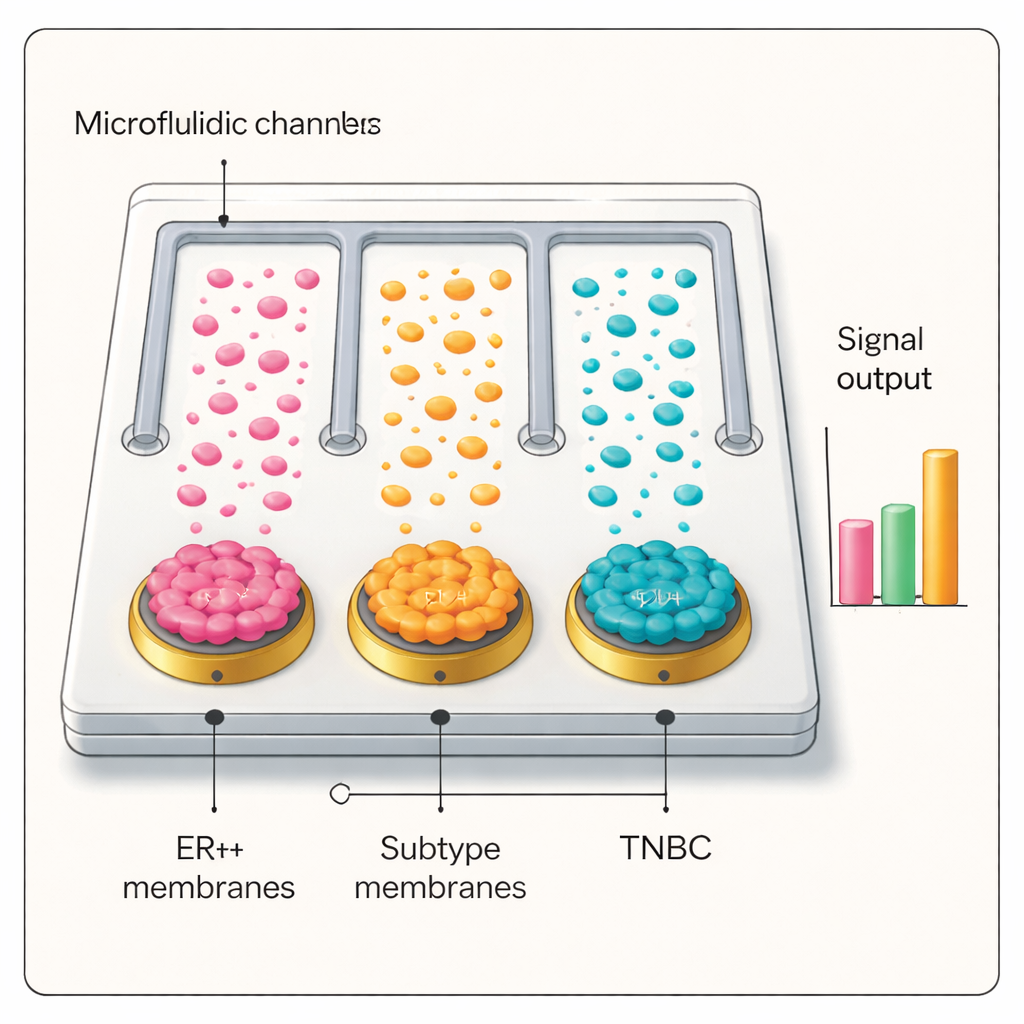
Van laboratoriumbank naar patiëntbloedmonsters
Gewapend met deze selectieve en gevoelige interface bouwde het team een microfluïdische chip met parallelle kanalen, elk gecoat met een ander borstkankercelmembraan, plus een ongecoat controlekanaal. Toen plasma van patiënten door de chip werd gevoerd en bevraagd met de zilver‑antistof tags, produceerde alleen het kanaal waarvan het membraan overeenkwam met het tumor‑subtype van de patiënt een hoog elektrisch signaal. In geblindeerde tests met tientallen personen — waaronder ER+ en triple‑negatieve borstkankerpatiënten, mensen met goedaardige borstziekten, longkankerpatiënten en gezonde vrijwilligers — onderscheidde het platform nauwkeurig kanker van niet‑kanker en identificeerde het correct subtypes van borstkanker. De diagnostische prestaties kwamen in veel gevallen overeen met of overstegen standaard pathologie en toonden potentieel voor het stadieren van de ziekte en het volgen van de progressie.
Wat dit kan betekenen voor toekomstige kankerzorg
Simpel gezegd hebben de onderzoekers het eigen buitenste pantser van kanker veranderd in een zeer selectief lokaas voor de kleine deeltjes die tumoren in het bloed vrijgeven. Door het elektrische signaal af te lezen van welk kanaal "oplicht", zouden artsen op termijn met slechts een bloedmonster kunnen vaststellen of kanker aanwezig is en welk type het is. Hoewel het systeem nog verder verfijnd moet worden—zoals het toevoegen van meer markers en meer membraantypen en het integreren van slimme data‑analyse—wijst het op een toekomst waarin routinematige, minimaal invasieve bloedtesten helpen bij het sturen van gepersonaliseerde kankerbehandeling en het monitoren van hoe tumoren veranderen in de tijd.
Bronvermelding: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Trefwoorden: borstkanker subtypes, liquid biopsy, extracellulaire blaasjes, microfluïdische diagnostiek, celmembraan sensoren