Clear Sky Science · nl
Een gestabiliseerde tandemantigeenchimera die krachtige malaria-overdrachtsreducerende activiteit opwekt
Waarom het stoppen van muggenoverdracht belangrijk is
De momenteel gebruikte malariavaccins kunnen ernstige ziekte en sterfte bij jonge kinderen sterk verminderen, maar laten een groot lek open: mensen die zich niet ziek voelen kunnen nog steeds parasieten bij zich dragen die muggen infecteren en de overdracht in stand houden. Deze studie introduceert een volgende generatie vaccindesign dat niet slechts één persoon wil beschermen, maar de infectieketen tussen mensen en muggen wil doorbreken. Door nauwkeurig te ontwerpen hoe belangrijke parasieteneiwitten aan het immuunsysteem worden gepresenteerd, streven de onderzoekers ernaar antistoffen op te wekken die van muggen slechte gastheren voor malaria maken, waardoor gemeenschappen dichter bij eliminatie komen.
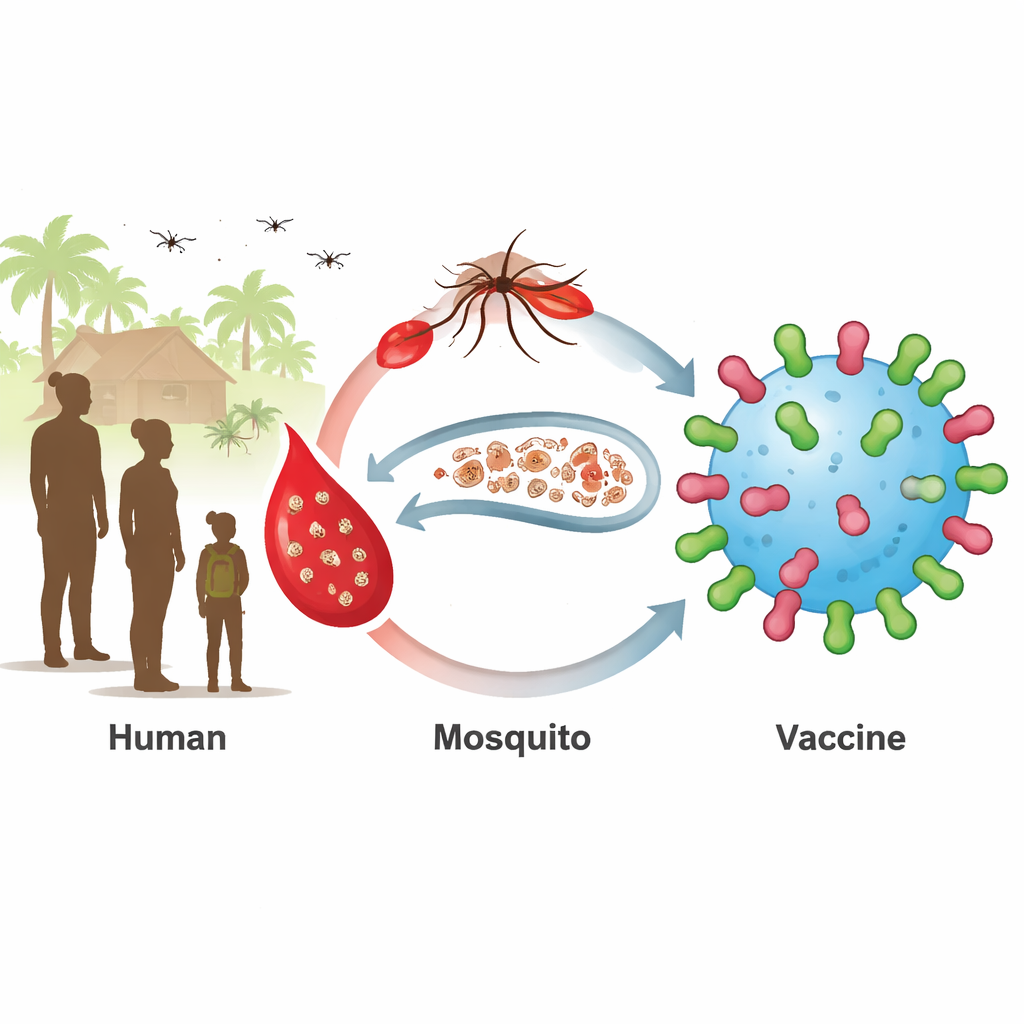
Een verborgen reservoir dat malaria in leven houdt
Huidige malariavaccins richten zich op het vroege stadium van infectie in de lever en het bloed. Ze werken het beste bij jonge kinderen, maar oudere kinderen en volwassenen herbergen vaak rijpe geslachtsstadia van de parasiet, gametocyten genoemd, zonder symptomen. Wanneer muggen deze mensen steken, nemen ze de parasieten op en verspreiden die verder. Twee parasietoppervlakte-eiwitten, bekend als Pfs230 en Pfs48/45, zitten op deze geslachtsstadia en zijn aantrekkelijke doelen voor zogenaamde transmissie-blokkerende vaccins. Vaccins tegen fragmenten van deze eiwitten zijn klinische proeven ingegaan, maar hebben moeite gehad om bij alle ontvangers sterke en blijvende antistofreacties op te wekken.
Een slimmer lokmiddel voor het immuunsysteem bouwen
Om eerdere ontwerpen te verbeteren, benaderden de auteurs het probleem vanuit structurele biologie en onderzochten zij in atomaire details hoe krachtige menselijke antistoffen binden aan Pfs230 en Pfs48/45. Ze identificeerden kleine regio’s, of epitopen, die bijzonder effectief zijn in het blokkeren van de parasietontwikkeling in muggen. Even belangrijk was dat ze “niet‑functionele” epitopen in kaart brachten die antistoffen aantrekken die wel binden maar de transmissie niet stoppen — eigenlijk verspilde immuuninspanning. Met computer‑modellering en eiwit‑engineeringtools fuseerden ze het meest krachtige deel van Pfs230 (zijn eerste domein) aan de sleutelregio van Pfs48/45 (zijn derde domein) in één zorgvuldig gerangschikt eiwit dat zij een gestabiliseerde tandemantigeenchimera, of STAC, noemen.
De nutteloze doelen verbergen, de nuttige behouden
De uitdaging was om deze twee domeinen samen te presenteren op een manier die nabootst hoe ze op de parasiet zitten, terwijl de normaal gesproken ingegraven niet‑functionele oppervlakken fysiek worden afgeschermd. Het team herontwierp iteratief de korte linker en het interfacegebied tussen de twee domeinen en testte elke versie op stabiliteit, correcte vouwing en of deze nog steeds aan een paneel van goed gekarakteriseerde antistoffen bond. Geavanceerde ontwerpsoftware suggereerde mutaties die het interface aansnoerden en de expressie in gekweekte cellen verbeterden. Structurele studies met röntgenkristallografie, small‑angle röntgenspreiding en cryo‑elektronenmicroscopie bevestigden dat in het uiteindelijke STAC‑construct de gewenste epitopen met hoge getrouwheid worden getoond, terwijl de bekende onhelpzame sites sterisch worden geblokkeerd.
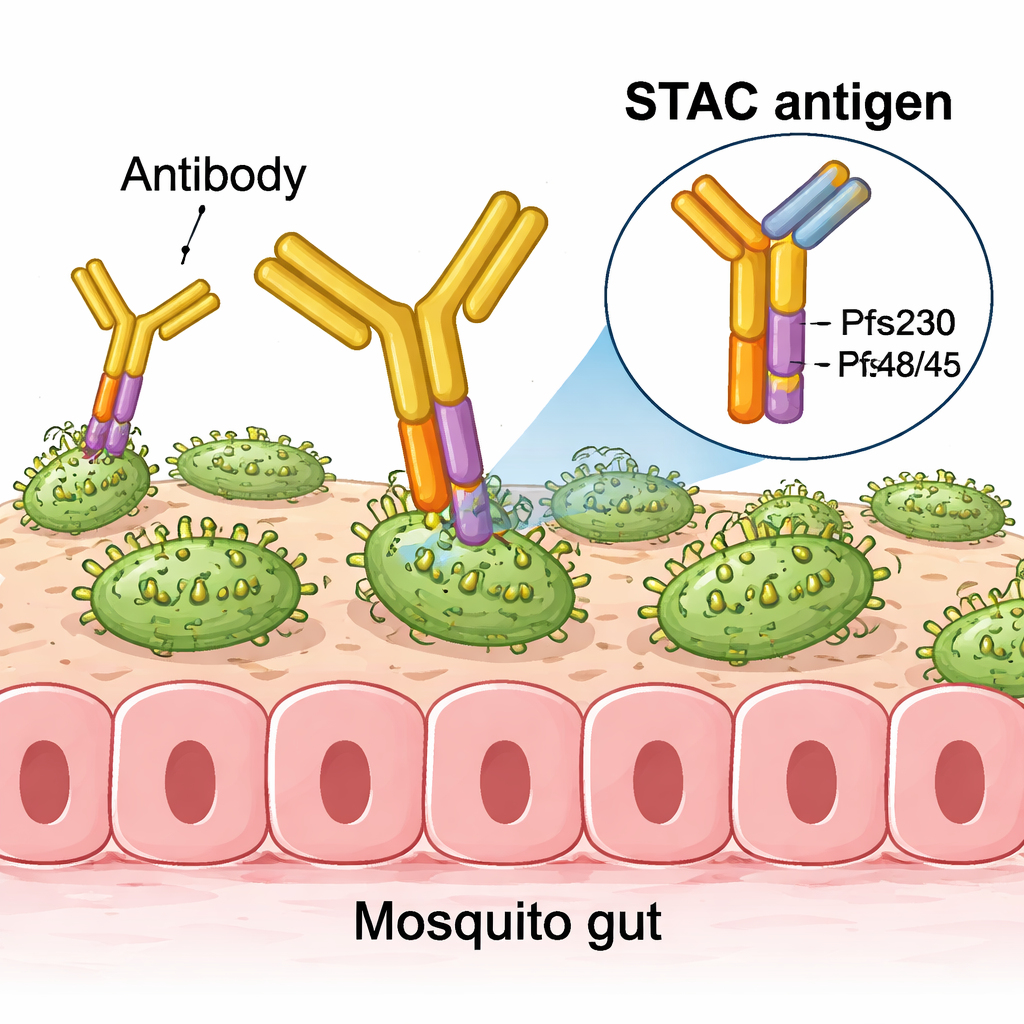
Van enkele moleculen naar krachtige nanodeeltjes
Proeven in muizen toonden aan dat wanneer STAC werd gekoppeld aan gespecialiseerde liposomen of aan zelfassemblerende eiwitnanodeeltjes, het sterke antistofreacties opwekte die de parasietontwikkeling in standaardmuggenvoedingsassays scherp verminderden. Bij gelijke of lagere doses presteerde STAC vaak even goed of beter dan vaccins die Pfs230‑ en Pfs48/45‑fragmenten apart gebruikten, of die nu alleen, gemengd of samen op hetzelfde deeltje werden gepresenteerd. In zeer gevoelige tests waarin muissereum sterk werd verdund, behielden antistoffen opgewekt door STAC‑gedecoreerde nanodeeltjes de transmissie‑reducerende activiteit beter dan die uit andere formuleringen, wat duidt op bijzonder krachtige en gefocuste reacties.
Wat dit kan betekenen voor malaria‑bestrijding
Voor niet‑specialisten is het kernidee dat STAC een op maat gemaakt lokmiddel is dat het immuunsysteem precies de onderdelen van de malariaparasiet laat zien die het meest van belang zijn om verspreiding te blokkeren, terwijl het afleidende regio’s verbergt die niet helpen. In diermodellen levert dit ontwerp antistoffen op die het de parasieten moeilijk maken hun levenscyclus in muggen te voltooien, zelfs wanneer antistofniveaus relatief laag zijn. Als vergelijkbare resultaten bij mensen worden bevestigd, zou STAC een krachtig partner kunnen worden van bestaande malariavaccins: gevaccineerde personen beschermen tegen ziekte en tegelijkertijd het infectieuze reservoir in de gemeenschap verkleinen. Breder gezien laat het werk zien hoe gedetailleerd structureel inzicht en eiwitengineering kunnen worden ingezet om multicomponentvaccins te maken die krachtig, stabiel en mogelijk goedkoper te produceren zijn.
Bronvermelding: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Trefwoorden: malariavaccins, transmissie-blokkering, Pfs230, Pfs48/45, nanodeeltje-immunogeen