Clear Sky Science · nl
Essentiële rol van de NONO‑HOXA1‑Wnt‑as bij differentiatie van cardiomyocyten
Waarom kleine hartcellen voor ons allemaal belangrijk zijn
Elke hartslag berust op miljarden gespecialiseerde spiercellen die tijdens de ontwikkeling in de baarmoeder ontstaan. Als dit proces misgaat, kunnen baby’s met ernstige hartafwijkingen worden geboren. Deze studie gebruikt menselijke stamcellen om een cruciaal controlesysteem bloot te leggen — opgebouwd uit de moleculen NONO en HOXA1 en het bekende signaal Wnt — dat jonge cellen aanstuurt om zich te committeren aan gezond hartspierweefsel. Inzicht in deze verborgen schakeling kan uiteindelijk leiden tot betere diagnose en behandeling van aangeboren hartziekten.
Van blanco cellen naar vroege hartbouwers
De onderzoekers begonnen met humane geïnduceerde pluripotente stamcellen — veelzijdige cellen die zich tot bijna elk celtype laten sturen. Met een standaardprotocol richtten ze deze cellen naar cardiomyocyten, de kloppende cellen van het hart. Wanneer het NONO‑gen werd verwijderd, namen veel minder cellen een hartidentiteit aan. Belangrijke vroege merkers die normaal verschijnen wanneer cellen hun primitieve staat verlaten en de hartlijn ingaan, werden sterk gereduceerd. Enkel‑cel RNA‑sequencing toonde dat veel NONO‑deficiënte cellen vastliepen halverwege, en bleven steken in een onrijpe mesendoderm‑achtige staat in plaats van door te ontwikkelen naar volgroeid hartspierweefsel.
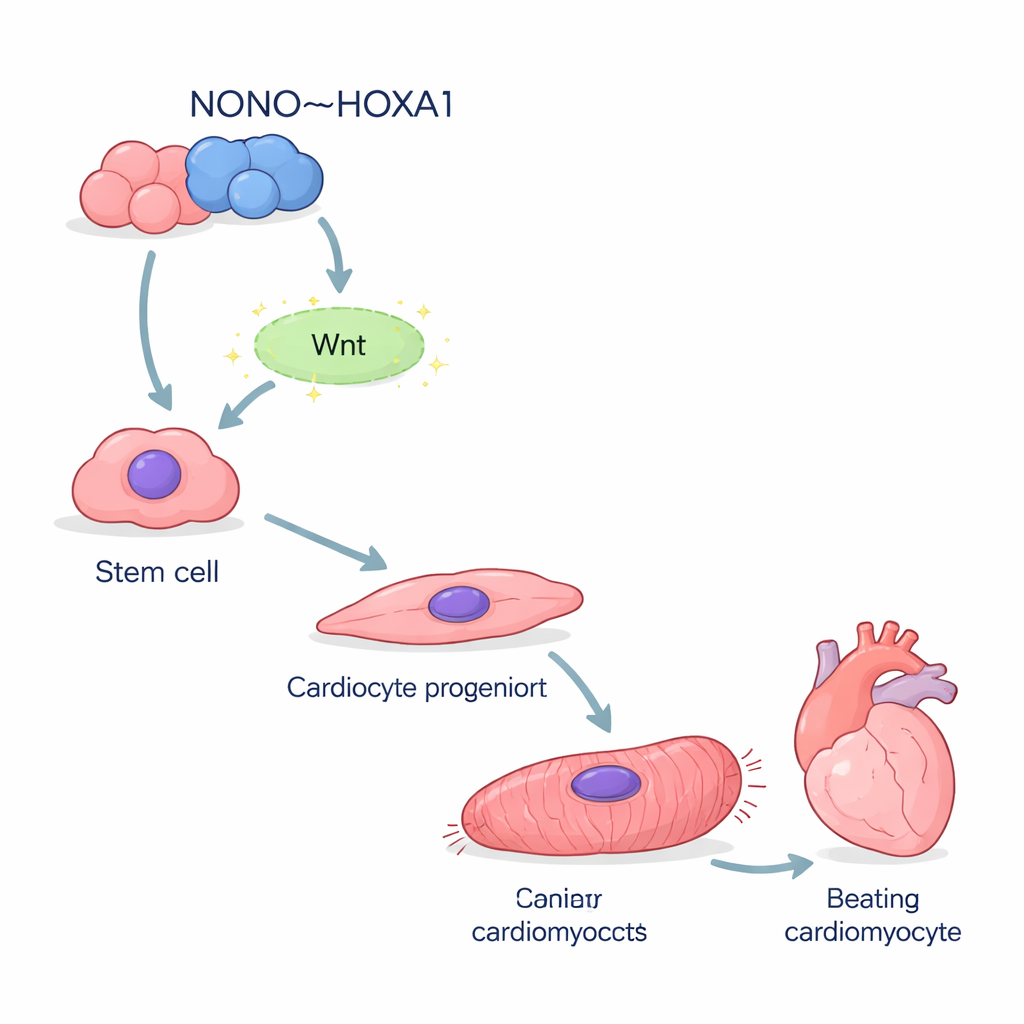
Als het ondersteunende skelet ontbreekt, haperen hartcellen
De cellen die zonder NONO toch in cardiomyocyten ontwikkelden, waren verre van gezond. Ze brachten veel lagere niveaus tot expressie van structurele eiwitten die het sarcomeer vormen, de microscopische machine die contractie aandrijft. In de microscoop vertoonden de meeste mutante cellen gedesorganiseerde, gefragmenteerde contractiele vezels in plaats van de nette strepen die bij normale cellen zichtbaar zijn. Elektronenmicroscopie bevestigde dat de gebruikelijke Z‑schijf “treden” van de contractieladder ontbreekten of misvormd waren. Functioneel klopten deze cellen langzamer en onregelmatiger. Metingen van calciumsurges — elektrische gebeurtenissen die elke hartslag triggeren — toonden grillige golven met vertraagde pieken en trage herstelperioden, wat overeenkomt met de genexpressiedefecten in calciumregulerende kanalen.
Ontwikkeling herstellen en het NONO–HOXA1‑partnerschap onthullen
Om te testen of deze problemen echt voortkwamen uit het verlies van NONO, introduceerde het team NONO opnieuw op een gecontroleerde, medicijninduceerbare manier tijdens de eerste twee dagen van differentiatie. Deze korte NONO‑puls herstelde grotendeels de opkomst van vroege cardiogene genen, vergrootte het aandeel kloppende hartcellen en bouwde georganiseerde sarcomeren en Z‑schijven opnieuw op. Genexpressieprofielen bevestigden dat veel genen voor spiercontractie en hartontwikkeling terug naar normale niveaus gingen. Daarentegen konden patiëntafgeleide gemuteerde varianten van NONO de ontwikkeling niet redden, wat ondersteunt dat dergelijke varianten ziekte veroorzaken door dit vroege programma te verstoren. Eiwit‑interactie‑experimenten toonden vervolgens aan dat NONO fysiek bindt aan een transcriptiefactor genaamd HOXA1, en dat dit contact HOXA1 stabiliseert en helpt bij het vormen van de dimeren die nodig zijn om DNA vast te houden.
Het Wnt‑signaal inschakelen om voor een hartbestemming te kiezen
Kaarten van de genoombindingsplaatsen van deze eiwitten lieten zien dat NONO en HOXA1 vaak dezelfde regulerende regio’s bezetten, waaronder diegenen die belangrijke vroege hart‑ en Wnt‑padgenen controleren. Wanneer NONO ontbrak, verzwakte HOXA1’s binding op veel van deze locaties, vooral bij genen die het vroegste precardiacale mesoderm aansturen — het eerste hartvormende weefsel. De daaropvolgende Wnt/β‑catenine‑route, die normaal helpt bij het opstarten van mesoderm‑ en hartontwikkeling, werd ook afgezwakt: er stapelde zich minder β‑catenine in de kern op en Wnt‑gevoelige rapportagetests namen af. Het versterken van Wnt‑signalen met een hogere dosis van een Wnt‑activerend middel in de vroegste dagen van differentiatie kon het ontbreken van NONO deels compenseren, waardoor meer hartcellen ontstonden en de expressie van hartgenen toenam.
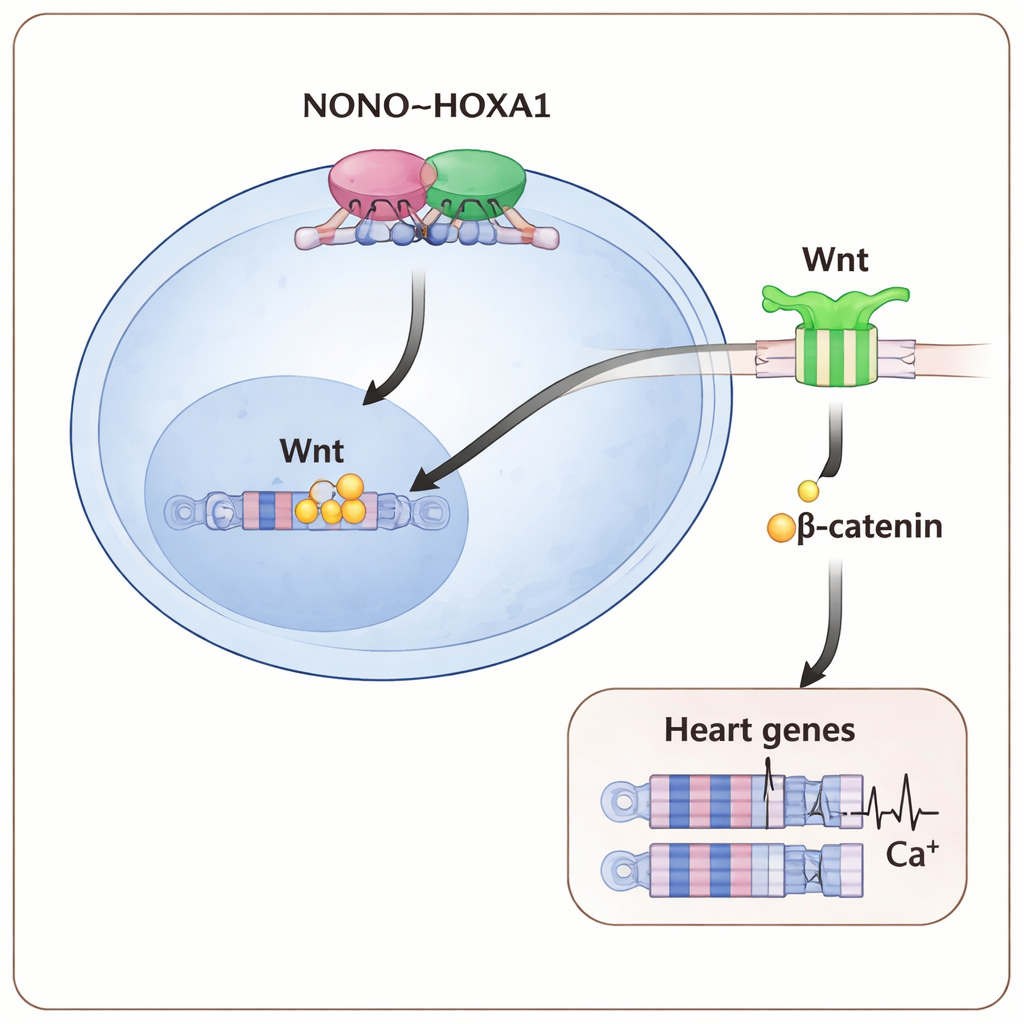
Wat dit betekent voor het begrijpen van aangeboren afwijkingen
Voor niet‑specialisten is de kernboodschap dat een klein moleculair team — NONO in samenwerking met HOXA1 om Wnt‑signalen fijn af te stemmen — fungeert als een vroege “verkeersleider” die jonge cellen vertelt hartspier te worden en ze toelaat goed te kunnen kloppen. Wanneer een onderdeel van deze NONO–HOXA1–Wnt‑as verstoord raakt, aarzelen cellen, blijven cruciale hartgenen uit, en zijn de resulterende cardiomyocyten structureel en elektrisch kwetsbaar. Deze inzichten bieden een duidelijker moleculair verklaringsmodel waarom mutaties in NONO worden geassocieerd met aangeboren hartziekten, en wijzen op mogelijkheden om dit pad te manipuleren in stamcelmodellen of — op termijn — in therapieën gericht op het voorkomen of herstellen van hartmalformaties.
Bronvermelding: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Trefwoorden: aangeboren hartafwijking, differentiatie van cardiomyocyten, Wnt‑signalering, hartmodellen met stamcellen, genregulatie