Clear Sky Science · nl
Electrografische cue‑reactiviteit lokaliseert samen met diepe hersenstimulatie van de nucleus accumbens in een geval van opioïdeverslaving
Waarom dit verhaal ertoe doet
Opioïdeverslaving blijft een dodelijke epidemie, en veel mensen blijven worstelen met krachtige drugshunkeringen ondanks medicatie en begeleiding. Dit artikel vertelt het verhaal van een jonge man van wie het behandelteam een hersenimplantaat niet alleen gebruikte om zijn hersenen te stimuleren, maar ook om naar ze te luisteren. Door een specifiek elektrisch signaal te vinden dat samenhing met zijn opioïdehunkering, konden ze zijn diepe hersenstimulatie verfijnen zodat die beter werkte, met minder vermogen, en hem hielp drugsvrij te blijven.
Meeluisteren bij hunkering
De patiënt was een 25‑jarige man met een lange voorgeschiedenis van ernstige opioïdeverslaving, begonnen in de vroege adolescentie, samen met depressie, angst en andere complicaties. Standaardbehandelingen, waaronder zeer hoge doses methadon, hadden zijn hunkeringen niet onder controle gehouden. Jaren eerder had hij diepe hersenstimulatie (DBS) gekregen in een diep gelegen hersengebied dat de nucleus accumbens heet, een belangrijk knooppunt in motivatie en beloning. Met die stimulatie aan namen zijn hunkeringen af en bleef hij enkele jaren onthouding van opioïden behouden. Toen bij een chirurgische complicatie echter zijn batterij moest worden verwijderd, schoten zijn hunkeringen binnen enkele weken weer omhoog en nam het risico op terugval sterk toe. Dit creëerde een zeldzame kans: zijn hersenelektrode kon tijdelijk worden aangesloten op externe opnameapparatuur, waardoor onderzoekers rechtstreeks hersenactiviteit konden meten terwijl hij hunkering ervoer.
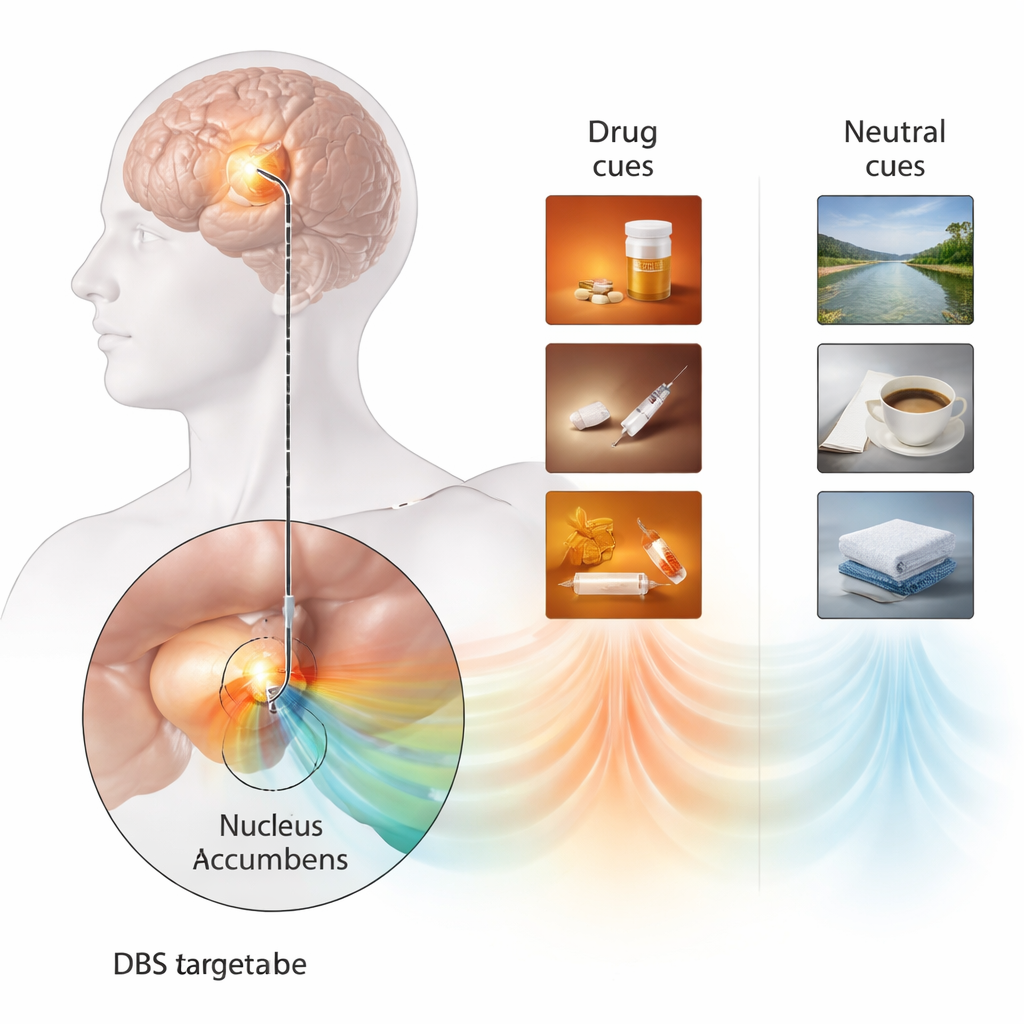
Gepersonaliseerde triggers onthullen een hersensignaal
Om vast te leggen hoe hunkering er in de hersenen uitziet, bouwde het team een sterk gepersonaliseerde cue‑reactiviteitsopdracht. In plaats van algemene drugafbeeldingen maakten ze korte video's die nauw aansloten bij zijn eigen vroegere druggebruik—zijn voorkeursopioïde, injectieapparatuur en voorbereidingsrituelen—en zetten die af tegen rustige natuurscènes. Na elke zes seconden durende clip beoordeelde hij hoe sterk zijn drang om opioïden te gebruiken voelde. Tegelijkertijd werd de DBS‑lead in zijn nucleus accumbens gebruikt als een klein microfoontje, dat de lokale elektrische ritmes van zijn hersenen opnam. Wanneer de drugvideo's werden afgespeeld, verscheen er in het ventrale deel van de nucleus accumbens een karakteristiek laagfrequent ritme (in het bereik van 1–6 Hz), een gebied waarvan men denkt dat het overeenkomt met de zogenaamde “shell” subregio. Dit signaal was veel zwakker bij neutrale video's en werd niet gezien in andere delen van de elektrode. Belangrijk is dat een hogere amplitude in dit ritme samenhing met sterker zelfgerapporteerde hunkering, wat suggereert dat het een direct hersenmerk van drugcue‑reactiviteit was en geen algemene aanwijzing van opwinding of aandacht.
Stimulatie omzetten in een gericht instrument
De cruciale volgende vraag was of stimulatie op precies die plek het hunkeringgerelateerde hersenritme en de ermee samenhangende drang kon dempen. Het team testte systematisch verschillende contactparen van de elektrode en vroeg in realtime naar hunkering, stemming en bijwerkingen terwijl ze de stimulatiesterkte geleidelijk verhoogden. Het ventrale contactpaar dat in de nucleus accumbens‑shell zat, bleek de ideale plek: het gaf sterke verlichting van hunkering en verbetering van de stemming bij relatief lage stroomsterkte, met minimale bijwerkingen. Meer dorsale contactparen, in een nabijgelegen vezelbundel genaamd de anterior limb van de internal capsule, hielpen ook maar vereisten veel sterkere stimulatie en gaven onaangename sensaties. Geleid door deze tests herhaalden de onderzoekers vervolgens de cue‑reactiviteitsopdracht terwijl ze korte stoten shell‑stimulatie gaven vóór elke video. Onder deze “gestimuleerde” conditie werd het eerder verhoogde 1–6 Hz‑ritme tijdens drugcues teruggedrongen richting neutrale niveaus, en daalden zijn gemiddelde hunkerbeoordelingen met meer dan de helft.
Blijvende verandering met een lichtere aanraking
Gewapend met dit convergerende bewijs—van anatomie, hersensignalen en gedrag—programmeerden de clinici zijn geïmplanteerde apparaat permanent opnieuw om gericht te stimuleren in de nucleus accumbens‑shell met veel lagere stroom dan voorheen. In de zes maanden daarna rapporteerde hij aanhoudende verminderingen in zowel de frequentie als de intensiteit van zijn opioïdehunkeringen, bleef hij onthouding behouden en voldeed hij aan de criteria voor vroege remissie, zonder grote veranderingen in stemming, angst of energie. Modellering van hersennetwerken liet zien dat de nieuwe instellingen een kleiner, meer gefocust weefselvolume activeerden terwijl ze een belangrijke baan tussen de nucleus accumbens en een onderliggend gebied onder de frontale lobben betrokken bij emotie en waardering aanspraken. Omdat de stimulatie efficiënter was, nam de batterijbehoefte aanzienlijk af—een belangrijk voordeel voor een jonge patiënt die waarschijnlijk langetermijntherapie nodig heeft.
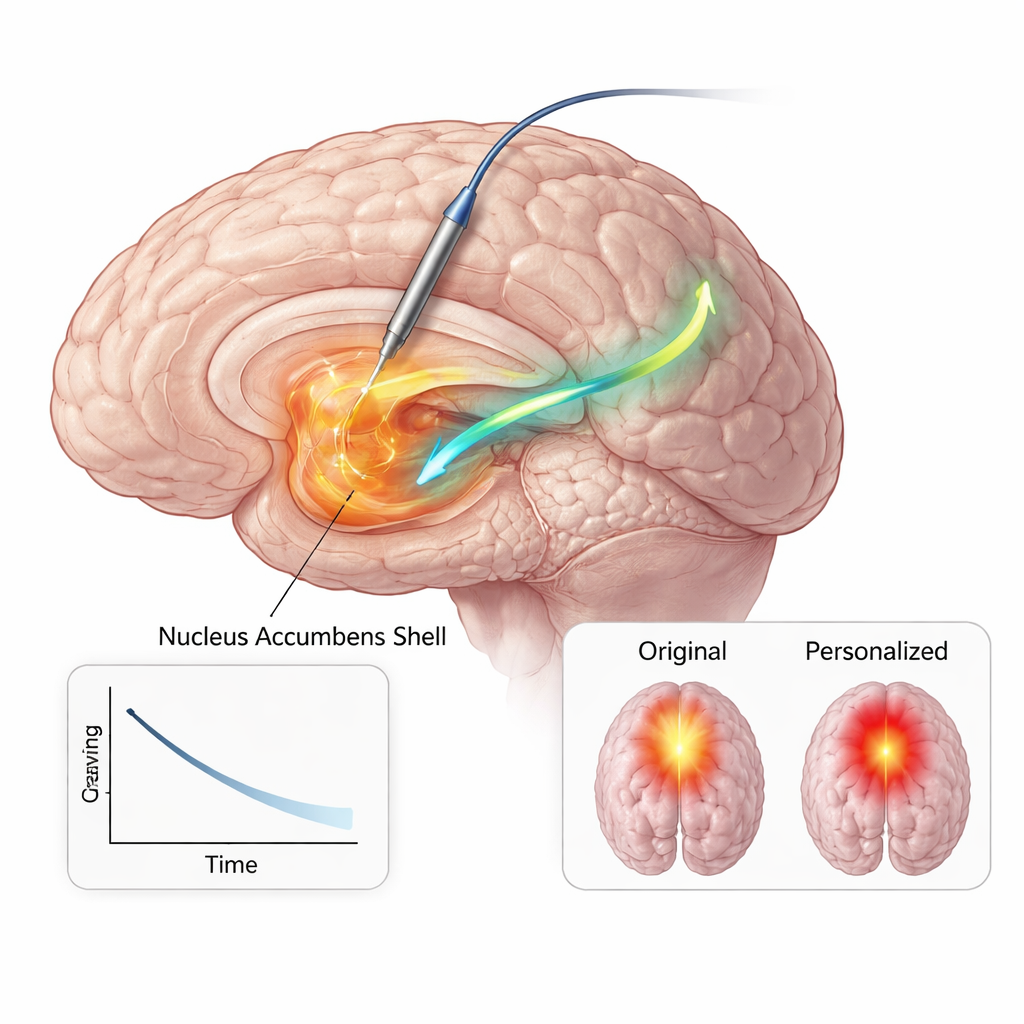
Wat dit kan betekenen voor toekomstige zorg
Dit N‑of‑1‑geval bewijst niet dat dezelfde benadering voor iedere persoon met opioïdeverslaving zal werken, maar het dient als bewijs van principe. Het toont aan dat bij ten minste één individu een specifiek elektrisch ritme in een beloningsknooppunt van de hersenen nauwkeurig samenviel met opioïdehunkeringen en door precies gerichte stimulatie kon worden gedempt, wat leidde tot duurzame symptoomverlichting met een lagere elektrische dosis. In eenvoudige termen leerde het team de stimulator ‘afstemmen’ op het eigen hunker‑signaal van de patiënt. Als vergelijkbare hersenmarkers bij meer mensen kunnen worden gevonden en gevolgd, en als apparaten die zowel kunnen meten als stimuleren breder beschikbaar worden, zouden toekomstige behandelingen diepe hersenstimulatie voor verslaving kunnen personaliseren—reagerend wanneer hunkeringcircuits opvlammen en mogelijk mensen helpen terugval voor te blijven.
Bronvermelding: Qiu, L., Nho, YH., Seilheimer, R.L. et al. Electrographic cue-reactivity co-localizes with accumbens deep brain stimulation in a case of opioid use disorder. Nat Commun 17, 1708 (2026). https://doi.org/10.1038/s41467-026-68758-w
Trefwoorden: opioïdeverslaving, diepe hersenstimulatie, nucleus accumbens, hersenbiomarkers, drugshunkering