Clear Sky Science · nl
Structurele basis voor fork-omkering en RAD51-regulatie door het SCF-ubiquitine-ligasecomplex van F-box helicase 1
Hoe cellen een vastgelopen DNA-kopieermachine herstellen
Elke keer dat een cel deelt, moet zij miljarden DNA-lettertekens snel en nauwkeurig kopiëren. Maar deze kopieermachine loopt vaak tegen problemen aan—DNA-schade, moeilijk-kopieerbare sequenties of medicamenteuze behandelingen kunnen het proces laten vastlopen. In zulke gevallen vertrouwen cellen op noodreparatieteams die de replicatievorks stabiliseren en opnieuw op gang brengen. Dit artikel onthult, met ongekende structurele details, hoe één van die teamleiders—een eiwitcomplex rond de helicase FBH1—vastgelopen DNA hervormt en een andere sleutelreparatie-eiwit, RAD51, strak onder controle houdt. Inzicht in deze choreografie helpt verklaren hoe cellen gevaarlijke genoombreuken vermijden en waarom verstoringen in deze factoren met kanker worden geassocieerd.
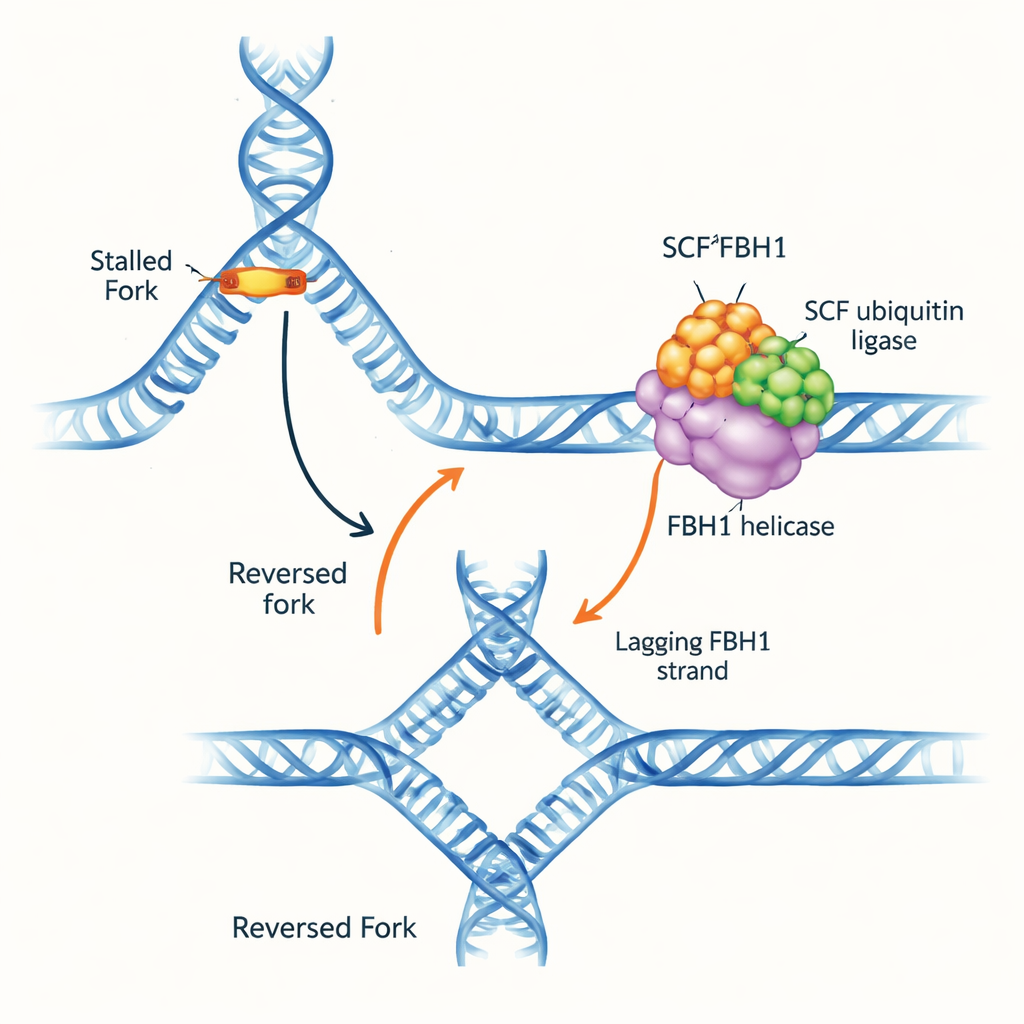
Een verkeersopstopping op de DNA-snelweg
DNA-replicatievorks zijn Y-vormige structuren waar de dubbele helix wordt ontwonden en gekopieerd. Wanneer de fork obstakels tegenkomt, kan deze van richting veranderen: de ouderlijke strengen slaan opnieuw aan elkaar, en de nieuwgevormde strengen paaren met elkaar, waardoor een vierweg-DNA-kruising ontstaat. Deze “fork-omkering” kan tijd kopen om schade te herstellen en replicatie veilig te hervatten, maar als het verkeerd wordt afgehandeld creëert het ook broos DNA dat kan breken. Meerdere moleculaire motoren zijn bekend die forks achteruit duwen door het dubbelstrengs DNA voor de fork vast te grijpen. FBH1 stak echter af doordat het zich anders gedraagt en vaak veranderd is in tumoren, wat suggereert dat het via een onderscheidend en medisch relevant pad werkt.
Een fork-specialist met een favoriete kant
De auteurs zuiverden het humane SCFFBH1-complex, dat de FBH1-helicase combineert met een ubiquitine-etiketteringsmodule (SCF). Ze onderzochten eerst welke DNA-vormen FBH1 prefereert. Met bindings- en ontwindingsexperimenten toonden ze aan dat SCFFBH1 sterk de voorkeur geeft aan echte fork-achtige structuren, met name waar een korte stretch enkelstrengs DNA aanwezig is op het “lagging” malstreng—de kant die in kleine fragmenten wordt gekopieerd. Op deze structuren ontwindt FBH1 DNA honderden malen sneller dan aan een eenvoudige losse uiteinde, wat aangeeft dat juiste betrokkenheid bij de fork-junctie zijn motoractiviteit enorm versterkt. Enkel-molecuul magnetische tangen bevestigden dat het complex DNA kan ontwinden en vervolgens over enkelstrengs DNA duizenden basen kan reizen zonder los te laten, en zich zo gedraagt als een krachtige, processieve motor.
De fork omkeren door van achteren te trekken
Om te achterhalen hoe deze motor forks daadwerkelijk omkeert, testte het team kunstmatige fork-substraten met of zonder enkelstrengs gaps. In tegenstelling tot andere fork-remodellers kon SCFFBH1 niet werken op een volledig gepaarde fork; het vereiste een gap op de lagging-malstreng en bewoog in 3′–5′ richting langs die enkelstreng. Deze “van achteren trekken”-beweging drijft de ouderlijke strengen om opnieuw aan elkaar te hechten terwijl het enzym geklemd blijft bij de fork-junctie. Een cryo-elektronenmicroscopiestructuur van SCFFBH1 gebonden aan een vastgelopen fork laat zien hoe: een speciaal positief geladen oppervlak, een “junction binding motif” in een subdomein van FBH1, nestelt zich precies op het takpunt waar de drie DNA-armen samenkomen. Toen de onderzoekers twee sleutelaminozuren in dit motief muteerden, daalde fork-omkering in proefbuisjes ongeveer 25-voudig, terwijl de basale ontwindingsmotor redelijk bleef functioneren. In cellen verhinderde diezelfde mutatie de normale vertraging van replicatievorks in reactie op een stressinducerend middel, een kenmerk van mislukte fork-omkering.
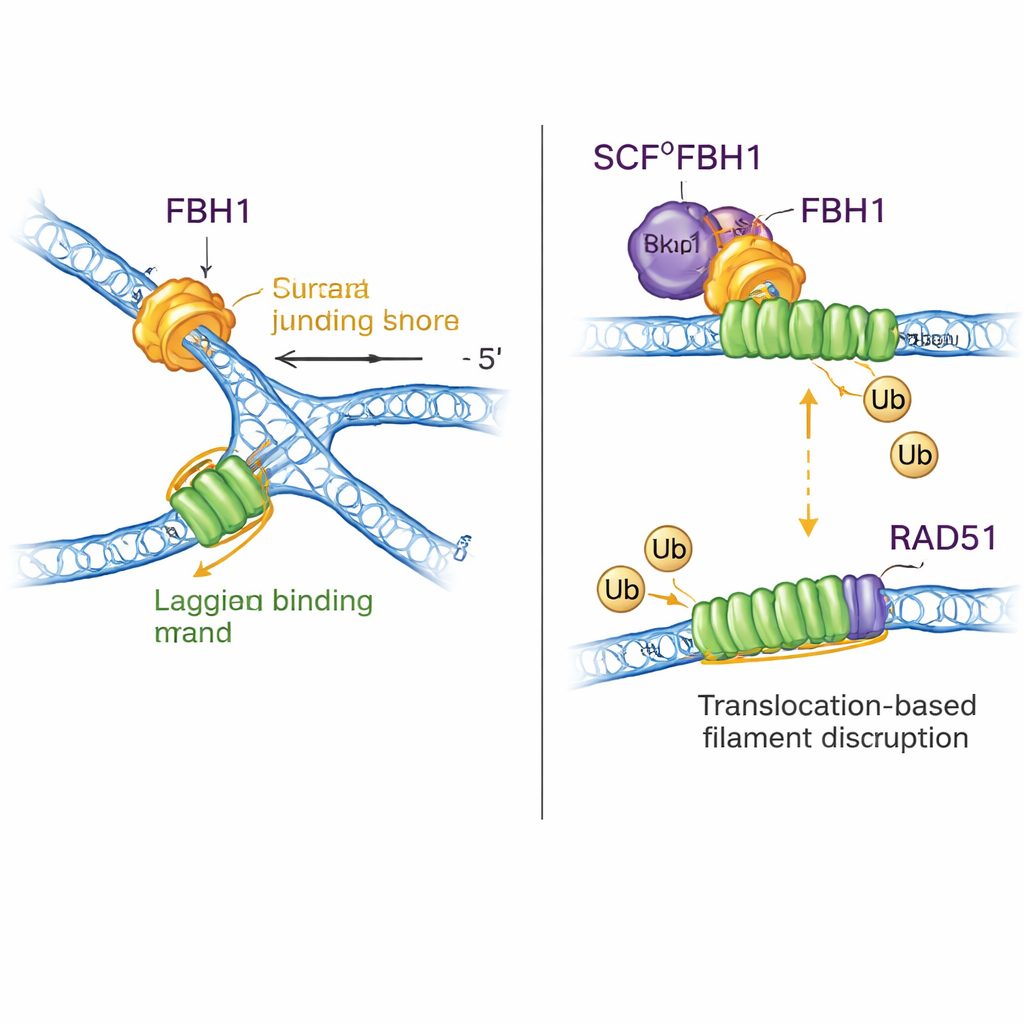
Een dubbele rol: DNA hervormen en RAD51 verwijderen
FBH1 is niet alleen een motor; via het SCF-complex helpt het ook kleine ubiquitine-tags aan eiwitten te hangen. De nieuwe structuren assembleren vrijwel het gehele SCFFBH1–DNA-complex en tonen dat de ubiquitine-overdrachts"kop" van het ligase minder dan 45 ångström verwijderd zit van het lagging-streng-DNA dat uit FBH1 naar buiten komt. Door bekende structuren van andere ubiquitine-ligases te docken, stellen de auteurs voor dat deze geometrie RAD51 positioneert—een enzym dat filamenten op DNA vormt om recombinatie te bevorderen—recht in het vizier op de lagging-streng van een vastgelopen fork. Eerder werk toonde aan dat FBH1 RAD51 mechanisch van DNA kan strippen en het ook kan markeren met ubiquitine zodat het niet makkelijk opnieuw bindt. Het nieuwe model verenigt deze ideeën: terwijl FBH1 langs de lagging-streng trekt om de fork te hervormen, kan de nabijgelegen SCF-module RAD51-subunits labelen, wat helpt bij het ontmantelen of voorkomen van excessieve RAD51-filamenten die anders de juiste forkverwerking zouden blokkeren.
Wat dit betekent voor genoomstabiliteit en kanker
Samen genomen laat de studie zien dat SCFFBH1 vastgelopen DNA-replicatievorks omkeert met een mechanisme dat verschilt van andere bekende fork-remodellers: het grijpt het takpunt stevig vast terwijl het zich van achteren over het lagging-malstreng verplaatst, wat veilige herwikkeling van ouderlijk DNA bevordert zonder een langlevende, mobiele vierwegkruising te vormen. Tegelijkertijd is het ingebouwde ubiquitine-ligase strategisch gepositioneerd om RAD51 van diezelfde streng te verwijderen en zo ongecontroleerde recombinatie tijdens replicatiestress te voorkomen. Omdat FBH1 vaak verloren gaat of gemuteerd is in kankers, helpen deze structurele en mechanistische inzichten verklaren hoe zulke tumoren DNA-schade accumuleren en waarom ze mogelijk anders reageren op middelen die replicatiestress opwekken of gerelateerde routes targeten.
Bronvermelding: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Trefwoorden: DNA-replicatiestress, fork-omkering, FBH1 helicase, RAD51-regulatie, genoomstabiliteit