Clear Sky Science · nl
Een proteogenomische atlas van 1032 hersenmetastasen identificeert moleculaire subtypes, immuunlandschappen en therapeutische kwetsbaarheden
Waarom kankers zich in de hersenen vestigen
Nu de kankerzorg verbetert, leven steeds meer mensen lang genoeg dat hun tumoren zich naar nieuwe plaatsen verspreiden, waaronder de hersenen. Deze hersenmetastasen zijn een veelvoorkomende en vaak verwoestende complicatie, maar artsen behandelen ze nog grotendeels op basis van waar de oorspronkelijke tumor vandaan kwam—long, borst, huid, dikke darm—in plaats van op hoe de kanker zich heeft aangepast aan het leven in de hersenen. Deze studie bouwde een gedetailleerde “atlas” van meer dan duizend hersenmetastasen om hun verborgen biologie te doorgronden, hoe ze interageren met de eigen cellen en het immuunsysteem van de hersenen, en waar nieuwe behandelopties mogelijk liggen.
Het bouwen van een groot kaartwerk van hersentumoren
De onderzoekers verzamelden gegevens van 1.032 hersenmetastasen die waren ontstaan uit verschillende primaire kankers, samen met tientallen overeenkomstige primaire tumoren en enkele agressieve primaire hersentumoren ter vergelijking. Ze combineerden meerdere geavanceerde benaderingen: DNA- en RNA-sequencing, grootschalige eiwit- en metabolietmetingen, single-cell en ruimtelijke kaartlegging van tumor- en immuuncellen, en miniatuuroperganoïden afgeleid van patiënten die in het laboratorium werden gekweekt. Door al deze lagen te integreren, wilden ze niet alleen genen opsommen, maar zien hoe hele biologische systemen zich gedragen binnen hersenmetastasen.
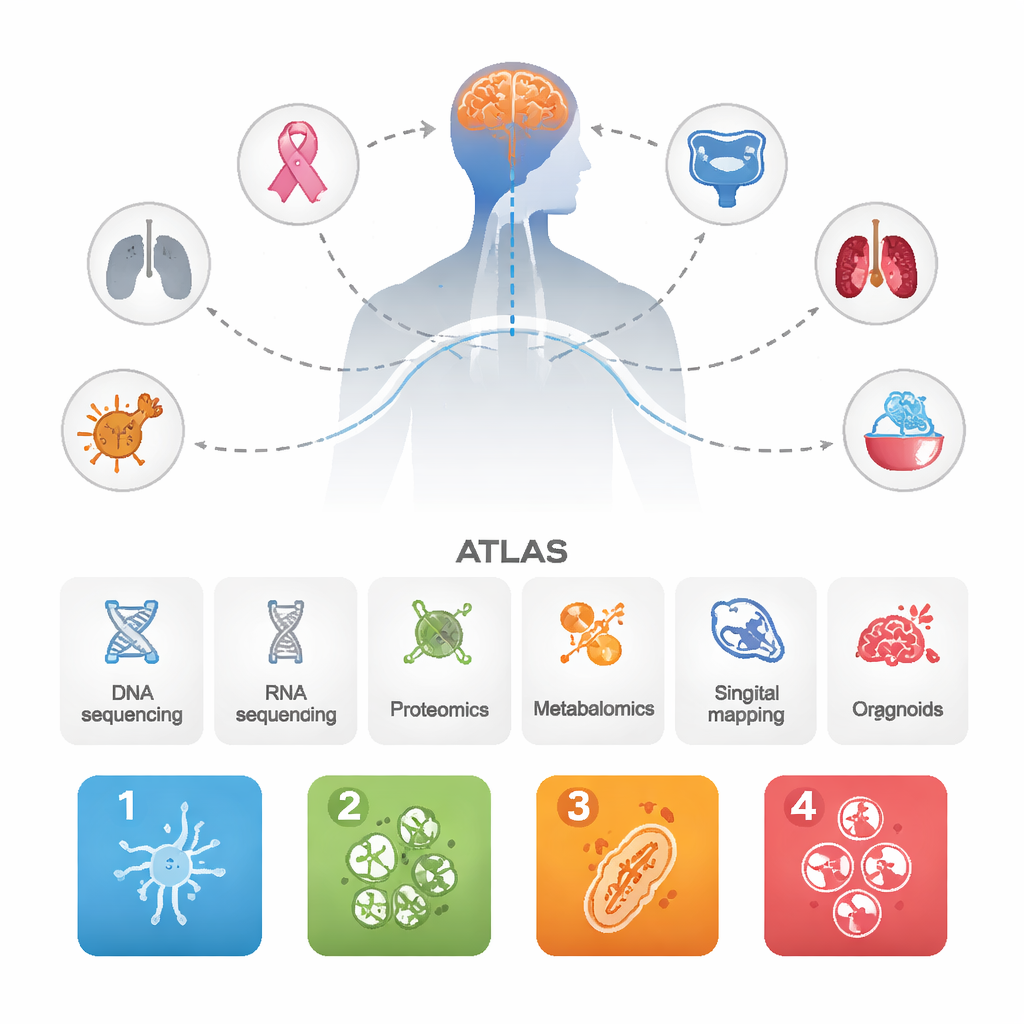
Vier terugkerende “persoonlijkheden” van hersenmetastasen
Ondanks hun uiteenlopende herkomst vielen de hersenmetastasen herhaaldelijk in vier grote moleculaire subtypes. Het eerste, BrMS1 genoemd, lijkt “neuraal-achtig”: tumorcellen en het omliggende weefsel tonen veel hersen- en zenuwcelprogramma’s en vertonen relatief actieve immuurbewaking. BrMS2 is “immuun-ingedrongen”, vol met immuuncellen, met name T-cellen, en toont een programma dat bekendstaat als epitheliale–mesenchymale overgang, dat celverbindingen versoepelt en de lokale omgeving herschikt. BrMS3 is “metabool”, gedomineerd door zeer actieve kankercellen die hun energiegebruik herprogrammeren—brandend via paden zoals vetzuurmetabolisme en oxidatieve fosforylering. BrMS4 is “proliferatief”, gekenmerkt door snelle celdeling, stamcelachtige eigenschappen en hoge genomische instabiliteit, maar opvallend weinig immuuncellen.
Wat de omgeving van de tumor onthult
Door in te zoomen op single-cell- en ruimtelijke resolutie liet het team zien dat elk subtype in een eigen buurt binnen de hersenen leeft. BrMS1-laesies zijn rijk aan hersensteuncellen zoals astrocyten en neuronen, wat suggereert dat de tumor normaal hersenweefsel nabootst en benut. BrMS2-tumoren daarentegen zijn bezaaid met dichte clusters van T-cellen, inclusief veel “uitgeputte” T-cellen die checkpointmoleculen zoals PD-1 tot expressie brengen, en hebben geactiveerde bloedvaten en ontstekingssignalen. BrMS3-laesies bevinden zich in metabolisch drukke zones, terwijl BrMS4-laesies eilanden van snel delende cellen vormen omringd door relatief immuinarme gebieden. In het algemeen vond de studie dat in hersenmetastasen—maar niet in primaire tumoren—sterke activering van epitheliale–mesenchymale overgang vaak samenhangt met hogere T-celinfiltratie, wat suggereert dat dit programma mogelijk helpt de deur te openen voor immuuncellen.
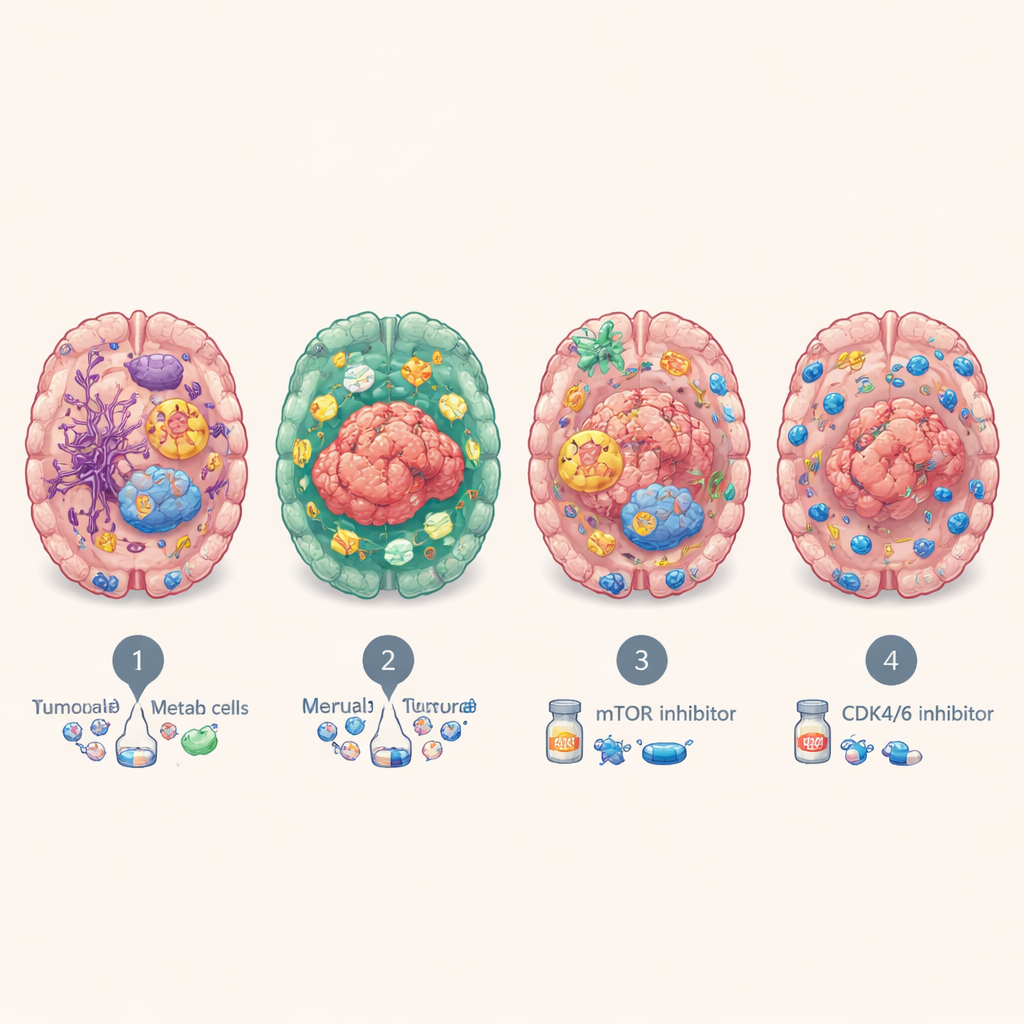
Aanwijzingen voor behandeling en patiëntuitkomsten
Deze moleculaire persoonlijkheden waren niet louter theoretisch. Patiënten met het immuun-ingedrongen BrMS2-subtype leefden over het algemeen langer dan die met het proliferatieve BrMS4-subtype, dat consequent de slechtste uitkomsten vertoonde. Door medicijnen te testen op patiënt-afgeleide organoïden, vonden de onderzoekers dat de metabole BrMS3-tumoren bijzonder gevoelig waren voor het remmen van het mTOR-signaleringspad, dat helpt bij het regelen van celgroei en stofwisseling, en dat de snel delende BrMS4-tumoren meer kwetsbaar waren voor CDK4/6-remmers, geneesmiddelen die de celcyclus vertragen. Aparte analyses suggereerden dat BrMS1-tumoren mogelijk beter op radiotherapie reageren, terwijl BrMS2’s ontstoken, checkpoint-rijke omgeving het waarschijnlijker maakt dat ze baat hebben bij immunotherapieën die uitgeputte T-cellen heractiveren—hoewel dit nog bevestigd moet worden bij patiënten met hersenmetastasen.
Wat dit betekent voor mensen met hersenmetastasen
Deze atlas toont dat zodra kankercellen de hersenen bereiken, ze de neiging hebben samen te vloeien naar een paar gedeelde biologische toestanden die losstaan van hun oorspronkelijke herkomst. Weten of iemands hersenmetastase neuraal-achtig, immuunrijk, metabool of sterk proliferatief is, zou uiteindelijk kunnen helpen bij het kiezen van meer gerichte behandelingen—zoals de keuze tussen radiotherapie, immunotherapie of medicijnen die de stofwisseling of celdeling aanpakken. Hoewel dit werk de standaardzorg nog niet verandert, biedt het een gedetailleerde routekaart voor toekomstig onderzoek en klinische trials die gericht zijn op het omzetten van deze moleculaire kwetsbaarheden in betere, meer precieze therapieën voor patiënten met hersenmetastasen.
Bronvermelding: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Trefwoorden: hersenmetastase, tumorsubtypes, tumormicroomgeving, kankerimmunotherapie, kankerstofwisseling