Clear Sky Science · nl
De fosfolipidesamenstelling beïnvloedt sterk de assemblage van β‑barrel‑eiwitten in gezuiverde bacteriële buitenmembranen
Waarom bacteriële bekledingen ertoe doen
Door geneesmiddelen resistente “superbugs” vormen een groeiende bedreiging omdat veel antibiotica eenvoudigweg niet door de robuuste buitenste verdediging dringen. Deze studie bekijkt nauwkeurig één cruciaal onderdeel van die verdediging bij Gramnegatieve bacteriën zoals E. coli: een beschermende buitenlaag vol loopvormige eiwitten en gespecialiseerde vetten. Door te onderzoeken hoe de samenstelling van deze vetten het bouwen van de buitenlaag regelt, onthullen de auteurs zwakke plekken die benut kunnen worden bij het ontwerpen van toekomstige antibiotica.
Het tweevoudige schild
Gramnegatieve bacteriën zijn bijzonder omdat ze twee membranen hebben. Het binnenmembraan verzorgt de dagelijkse celprocessen, terwijl het buitenmembraan fungeert als een robuuste regenjas die veel toxines en antibiotica buiten houdt. Deze buitenste laag bestaat uit twee typen lipiden: gewone fosfolipiden aan de binnenzijde en een stijve suiker‑vetverbinding genaamd lipopolysaccharide (LPS) aan de buitenzijde. Door deze schaal zijn talloze “beta‑barrel” eiwitten geweven—holle cilinders die poriën en poorten vormen voor voedingsstoffen. Een moleculair apparaat genaamd BAM (barrel assembly machine) is verantwoordelijk voor het vouwen van deze eiwitten in de juiste vorm en het inbrengen ervan in het buitenmembraan.
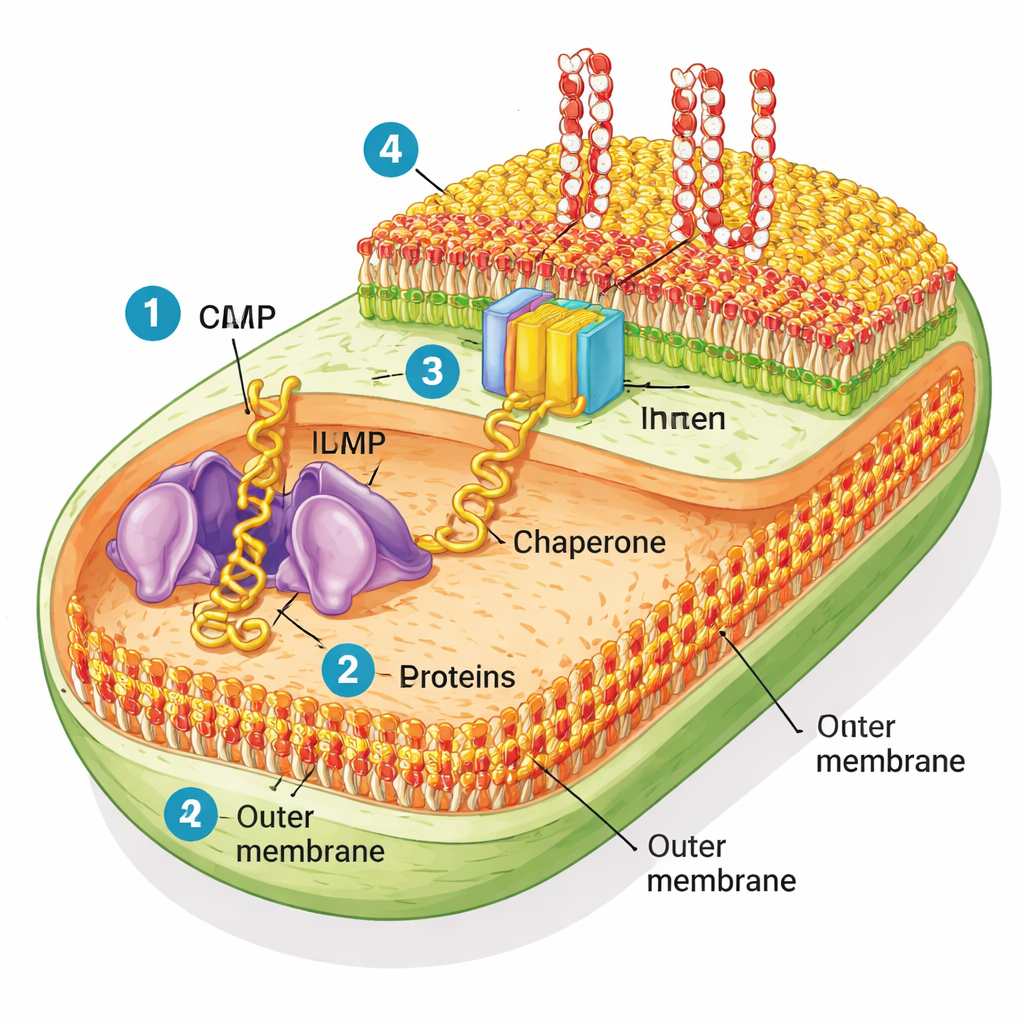
De bacteriële bekleding nabootsen in een reageerbuis
Om te zien hoe goed BAM werkt in een realistische omgeving, zuiverden de onderzoekers delen van het E. coli‑buitenmembraan en creëerden kleine blaasje die ze “native OMs” noemen. In tegenstelling tot eenvoudige kunstmatige membranen die in veel laboratoriumstudies worden gebruikt, behouden deze native membranen hun volledige mengsel van eiwitten en lipiden. Het team gebruikte vervolgens een celvrij eiwitfabriekje om nieuwe buitenmembraaneiwitten vanaf nul op te bouwen en observeerde of BAM in deze native blaasjes ze kon vouwen en inbrengen. Ze concentreerden zich op een model beta‑barrel eiwit genaamd EspP, samen met enkele anderen. Wanneer het helper‑eiwit SurA aanwezig was, vouwde BAM in de native membranen EspP efficiënt, en dit proces werd geblokkeerd door een bekend BAM‑richtend antibioticum genaamd darobactine—duidelijke aanwijzing dat het natuurlijke apparaat actief bleef.
Wanneer de vetmix verkeerd loopt
De auteurs vroegen vervolgens wat er gebeurt wanneer de lipidenbalans van het buitenmembraan verstoord is. Ze bestudeerden mutante stammen van E. coli die belangrijke systemen misten die normaal verkeerd geplaatste fosfolipiden in de buitenste bladzijde corrigeren. Eén systeem, MlaA, sleept weggerukte fosfolipiden terug naar het binnenmembraan; een ander, het enzym PldA, knipt ze in stukjes. Met behulp van native membranen uit deze mutanten ontdekte het team dat BAM‑gedreven assemblage van EspP duidelijk afnam in stammen zonder MlaA en ernstig verzwakt was wanneer PldA ontbrak. Deze effecten waren niet het gevolg van het verlies van BAM zelf of andere belangrijke eiwitten, die nog in normale hoeveelheden aanwezig waren, wat wijst naar de gewijzigde lipideomgeving als de boosdoener.
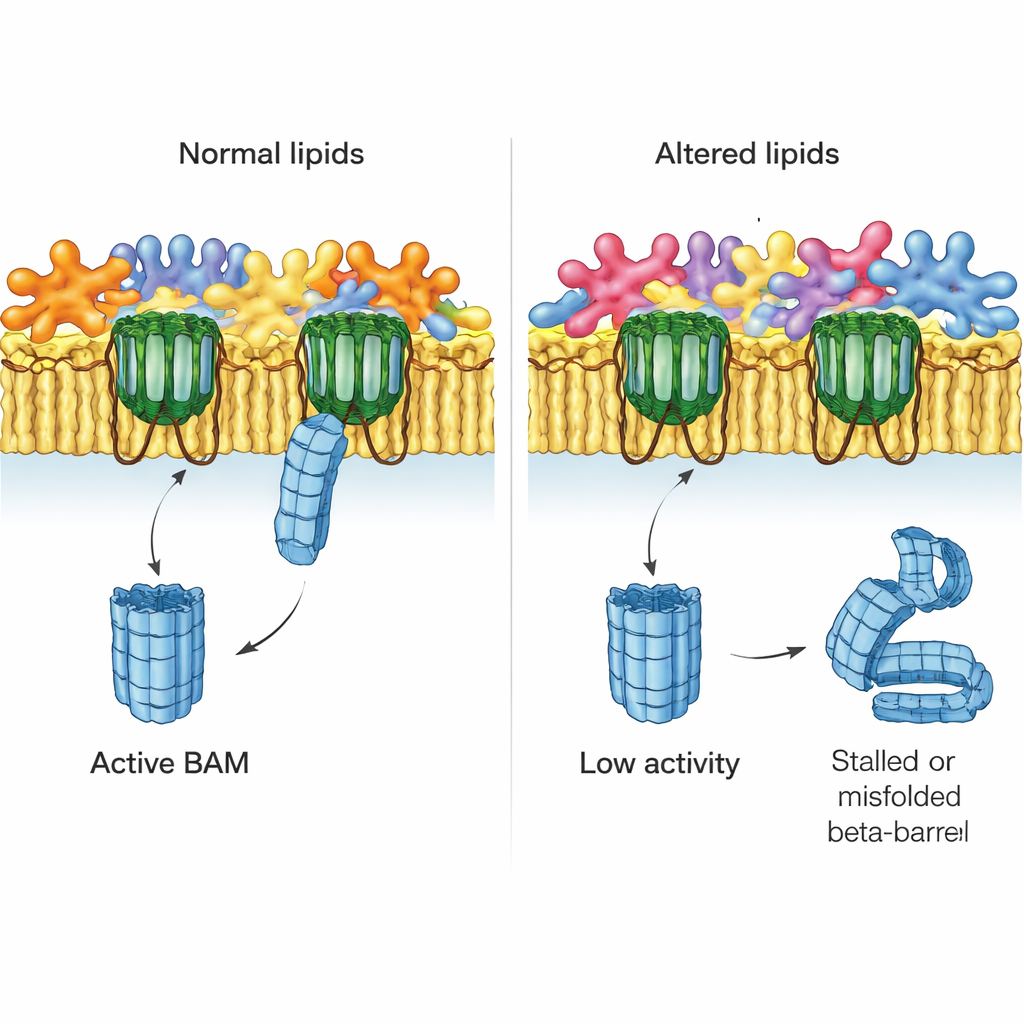
Het lipidenlandschap in detail in kaart brengen
Om functie aan chemie te koppelen ontwikkelden de onderzoekers een gevoelige massaspectrometriemethode om honderden individuele fosfolipiden in hele cellen en in gezuiverde buitenmembranen te catalogiseren. In normaal E. coli bevestigden ze dat één lipidentype (phosphatidylethanolamine, of PE) verrijkt is in het buitenmembraan, terwijl anderen (phosphatidylglycerol en cardiolipine) daar relatief uitgeput zijn. Ze vonden ook dat “lyso‑lipiden”, die slechts één vetstaart hebben en de neiging hebben membranen te buigen, verrassend geconcentreerd zijn in het buitenmembraan. In mutante stammen, vooral die zonder PldA, raakten deze patronen verstoord: de gebruikelijke verschillen tussen binnen‑ en buitenmembraan krompen of keerden zelfs om, en de lengtes en types van vetstaarten verschoofden. Stammen met de meest verstoorde lipideprofielen waren dezelfde waarin BAM het slechtst werkte.
Gevolgen voor antibioticastrategieën
Samengevat laat het werk zien dat het buitenmembraan niet slechts een passief skelet voor eiwitten is. De precieze fosfolipidesamenstelling beïnvloedt sterk hoe goed BAM de beta‑barrelporiën kan bouwen die de bacterie in leven houden. Wanneer de lipidenbalans verstoord raakt, functioneren minder BAM‑complexen correct en werken sommige langzamer. Hoewel levende bacteriën zich op manieren kunnen aanpassen die een reageerbuis‑systeem niet kan nabootsen, benadrukt deze studie hoe het afstemmen of ontregelen van specifieke lipiden de bacteriële bekleding kan verzwakken. Die inzicht biedt nieuwe mogelijkheden voor geneesmiddelen die ofwel BAM direct targeten of subtiel het lipidenevenwicht van het buitenmembraan verstoren, waardoor zelfs de sterkste Gramnegatieve bacteriën kwetsbaarder worden.
Bronvermelding: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Trefwoorden: Gramnegatieve bacteriën, buitenmembraaneiwitten, beta‑barrel assemblage, bacteriële lipiden, antibioticaresistentie